小児脳腫瘍の治療について
小児脳腫瘍のジレンマ
自分の子どもが脳腫瘍だと告げられると,親は動揺します。 どうしたら命を助けられるんだろうか? 診てくれているお医者さんは,この病気に詳しいのだろうか? 信用できるんだろうか? どこの病院に行ったらいいんだろう? お金はいくらかかるんだろうか? 病気が治ってもひどい後遺症が残るんだろうか? お医者さんに何を聞いたらいいのだろうか,素人が質問したら失礼にはならないんのだろうか? 学校をどのくらい休んだらいいんだろう? 子どもが痛くて苦しい思いをしないのだろうか? 誰に聞いたら最善の情報が得られるんだろう?
いろいろな疑問が突然,頭をよぎります。でも,親には何もわかりません。でもやっぱり主治医の先生を信頼しましょう! 以前と比較すれば,中規模な病院で治療されることはほとんどなく,大学病院やそれに匹敵する大きな病院に小児脳腫瘍の患者さんは集まっています。
治療法が複雑すぎて,ガイドラインやマニュアルやプロトコールに書いてあるとおりで最善の治療ができるような病気ではありません。担当する医師も,いろいろな専門医に知識や助力を求めて,治療に当たらなければなりません。もし,それができなければ,自分より小児脳腫瘍に詳しい医師がいたら,自分で治療しないで転院させることをためらわないで下さい。
ここをクリックすると,ソフィーの選択のページに飛びます。
ここから下は専門的な記述になります
- 小児脳腫瘍の頻度と死亡率
- 治療を考える上での脳腫瘍の特徴
- 病理診断がたくさんあること
- 良性脳腫瘍とは
- できた場所による予後の違い
- 年齢による治療法の違い
- 小児脳腫瘍の臨床研究は難しい
- 代表的脳腫瘍の治療方針
- 小児科医と脳外科医の役割
- まとめ
小児脳腫瘍の頻度と死亡率
発生数:米国のNCIの2012年統計では,15歳未満小児10万人あたり3.5人発生するとされています。2015年CBTRUSの推計によれば,米国で14歳以下の小児に4,630例発生しますので,人口比から推計すると日本には2016年に1,900例の小児脳腫瘍が発生しています。上記の統計のデータは2000年すぎくらいのものです。一方,日本の出生数は激減しています。2000年が119万人,2022年は79万人です。34%減少しおよそ3分の2になっています。それに伴って小児脳腫瘍の発生数も減少し,ますます珍しい病気となっています。
死亡数:米国小児脳腫瘍基金 PBTFUSによれば,小児の脳腫瘍は小児がんの中で最も死亡率が高くて,34才までの癌死の最も大きな原因だということです。米国NCIの2005年統計(SEER)では,14歳までの小児で,白血病 の人口10万あたりの死亡率(0.7)と悪性脳腫瘍の死亡率 (0.7) はほぼ同値でした。白血病の方が発生数そのものが多いので,脳腫瘍の方が治る確率が低い癌であることがわかります。2007年SEER統計で,19歳以下の悪性腫瘍による死亡数の第1位は白血病,2位が脳腫瘍でした。2016年のNCHS (United States National Center for Health Statistics)の統計では,19歳までの小児ガンの死亡数の29.9%が脳腫瘍死,24.9%が白血病死でした。小児脳腫瘍の死亡数は白血病の1.2倍に相当します。この悪性腫瘍死というものにどの程度の良性脳腫瘍が含まれているのかはわかりませんから,良性脳腫瘍を加えれば脳腫瘍死の方がかなり多いと考えられます。
しかし一方米国で1995年以降,5年生存割合の明らかな改善があります。
有病率:2007年11月に,米国のCBTRUS (The central brain tumor registry of the united states) の事務局に直接尋ねたところ, 2000年の時点での19歳以下の悪性と良性を併せた小児脳腫瘍の発生率は,人口10万人あたり4.3人だそうです。有病率は9.5人くらいで,少なくとも26,000人の子供が脳腫瘍の診断を受けて生きているそうです。
この事実は日本ではあまり知られていません。腫瘍ができる臓器別でみれば,日本でも小児に発生する固形癌の中では脳腫瘍は最も頻度が高くて,白血病による死亡率の低下とともに19才以下の癌死の中では脳腫瘍が最大の原因です。白血病の治療が注目されてどんどん進んでいるのに,脳腫瘍は置き去りの感があります。
平成18年度厚生労働科学研究(子ども家庭総合研究事業) 「小児慢性特定疾患治療研究事業の登録・管理・評価・情報提供に関する研究」平成16、17年度全国登録状況というのがネットで公開されています。脳腫瘍の発生実数を把握するのに全く役には立ちませんが,白血病に次いで脳腫瘍の発生が多いかな?くらいは理解できます。厚労省の人口動態年報平成12年では,15歳未満の原因別死亡数は不慮の事故(933人)に次いで,悪性新生物が2番目(403人)です。
日本で小児脳腫瘍の正確な統計はとられていません。いま日本でそれを知る手段はありませんし,今後も期待できません。髄芽腫は,小児の悪性脳腫瘍として最も有名です。髄芽腫の年間発生率は10万人あたり0.06-0.07人くらいでしょうから,発生数は全国で1年あたり80例強と推定されます。髄芽腫は15歳未満の小児脳腫瘍の約10%を占めるので,小児脳腫瘍の発生率は全人口10万あたり年間1人弱なのかもしれません。米国と同様に考えれば,小児人口10万あたり4.3人なのですが,全く推測できない状況です。米国の人口は日本の2.2倍なので,同じように推測すれば少なくとも12,000人の子供たちが脳腫瘍の診断を受けて生きていることになります。
後で述べるように小児脳腫瘍の治療の選択肢はとても複雑ですから,最も有名な髄芽腫においてさえも単純に判断できて選べる標準的治療というものがありません。ですから小児脳腫瘍の治療方針という問題を簡単に書くことはできませんが,良性腫瘍の治療も含めて,最新の治療指針とは何かを考えるための参考となることを記載します。
治療を考える上での脳腫瘍の特徴
1. 腫瘍の病理診断がたくさんあること
他の臓器に発生する小児の腫瘍と比べたとき,小児の脳腫瘍の最大の特徴は,病理組織が実に多彩なことです。日本脳腫瘍統計による14歳以下の脳腫瘍の病理組織型別頻度は,星細胞腫グレード2が19%で,髄芽腫 (11.9%),胚腫(ジャーミノーマ)(9.5%),頭蓋咽頭腫(8.9%),星細胞腫グレード3(5.7%),上衣腫 (4.5%),膠芽腫(3.5%)などが続きます。でも,毛様細胞性星細胞腫が一番多いはずですから,この統計はほとんど信用できません。
その他の脳腫瘍の頻度はとても低くてまれなものになります。上記以外で放射線や化学療法を用いるものに,毛様細胞性星細胞腫,びまん性橋膠腫/びまん性正中グリオーマ,乏突起膠腫,退形成性上衣腫,胎児性癌,未熟奇形腫,悪性奇形腫,混合性胚細胞腫瘍,卵黄嚢腫,絨毛上皮癌,中枢神経原発リンパ腫(PCNSL),松果体芽腫,中間型松果体実質腫瘍 (PPTID) ,大脳神経芽腫,嗅神経芽腫,異型中枢神経細胞種,神経節膠腫,脈絡叢乳頭癌,非定型奇形腫様/ラブドイド腫瘍(AT/RT),ETMR/ETANTR,ロゼット形成性グリア神経細胞腫瘍 RGNT,髄芽腫,悪性末梢神経鞘腫(MPNST),軟骨肉腫,髄膜黒色腫,非定型髄膜腫,退形成性髄膜腫,ランゲルハンス細胞組織球症(LCH)などがあります。
手術摘出が主として行われる小児腫瘍に,各種機能性腺腫を含む下垂体腺腫,シュワン細胞腫(神経鞘腫),神経線維腫,髄膜腫,血管芽腫(VHL フォン・ヒッペル・リンドウ病),海綿状血管腫,単純性(若年性)血管腫,ラトケのう胞,類表皮のう胞,類皮のう胞,成熟奇形腫,松果体細胞腫,上衣下巨細胞性星細胞腫 (SEGA),上衣下腫,脈絡叢乳頭腫,中枢性神経細胞腫,神経節細胞腫,神経節膠腫,胚芽異形成性神経上皮腫瘍(DNT),線維形成性乳児神経節膠腫(DIA/DIG),レルミット・ダクロス病/小脳異形成性神経節細胞腫,血管外皮腫,脊索腫,乳児先天性血管腫,骨腫,軟骨腫,線維性異形成症,内胚葉性のう胞,神経腸のう胞,第3脳室コロイド嚢胞,松果体のう胞,視床下部過誤腫,異所性灰白質,脂肪腫、NF-1とNF-2関連過誤腫,星芽細胞腫(アストロブラストーマ)などがありますが,さらに細分類をすれば限りがありません。
ですから小児の脳腫瘍を治療する医師は,これらの全てを理解していなければならないので,途方もない知識を求められます。例えば小児の白血病の治療ができるからといって,小児の脳腫瘍の治療ができるとは限りませんし,脳腫瘍の手術が上手だからといって脳腫瘍の化学(薬物)療法がわかるとはいえません。治療を始める前に,小児脳腫瘍にとても詳しい先生に巡り会えるかどうかが重要になります。
ちなみに私は,上に書いた全ての小児脳腫瘍を治療した経験がありますが,それぞれの組織型を数多く見ている訳ではありません。現実には患児が来るたびに病名が変わります。例えば乏突起膠腫の患児の次は星細胞腫,その後に神経節膠腫などといった具合です。これらの神経膠腫(グリオーマ)と呼ばれる腫瘍は,症候性てんかんなどとてもよく似た症状で発症して,MRI画像所見もとても似ていますが、それぞれの治療法は異なっているので,初診時の画像所見をみ誤れば,治療計画全体にあやまりを生じて治す機会を失ってしまうこともあります。
手術をするかどうかを含めて、はじめて治療を決めるときの初期判断が最終的な予後を決めてしまうといっても言い過ぎではありません。もう一つ決定的に重要な診断は病理診断です。しかし,経験を積んだ病理診断医でも星細胞腫と乏突起膠腫の鑑別には困ってしまうことがあり,遺伝子診断が必要です。時に致命的な誤診があり,悲しいことですが,毛様細胞性星細胞腫の子供たちが,病理誤診で膠芽腫や上衣腫として治療されたという事実も知っています。脳腫瘍の治療方法の選択は限りなく複雑なのです。
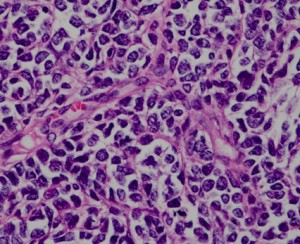
これは髄芽腫の組織像(HE染色)なのですが,これだけみても病理診断はつきません。最近は,遺伝子診断でWNT, SHHなどを見ることになっていますが,それも判然としないことも多いです。髄芽腫ではきつい放射線治療をしないで治るタイプもあります。
2. 良性脳腫瘍とは
上衣腫の治る確率は60%くらいで,頭蓋咽頭腫は8割強です。そんなに高いはずがありません。これらは良性腫瘍とされるものですが,上衣腫では4分の1が5年以内に死亡することとなりますし(>_<),頭蓋咽頭腫においては手術の数ヶ月から数年後の再発や再燃も多くて,何度も手術を受けたり,大きな後遺症をかかえてなんどか生存する子供たちが多いのです。
頭蓋咽頭腫は,視床下部と神経下垂体という脳の深くて重要な機能をもつところにできて,そこにくっついているために,熟練した脳神経外科医にとっても手術がとても難しいので,統計に載らないところでの手術死亡例も少なくないと想像されます。また頭蓋咽頭腫の手術ではできる限り下垂体の機能を守ることを考えますが,現実には間脳下垂体機能不全症と視力視野障害を残して生存する例が大多数です。さらに手術で完全摘出できないとき、とくに小さな子供たちに放射線治療おこなえば精神発達遅滞(認知機能障害)の可能性が残ります。
他にも良性脳腫瘍といわれる例を挙げれば,海綿状血管腫や神経節膠腫などが中脳に発生してゆっくり大きくなった時には,有効な治療法はほとんどなくて生き残る機会は少ないといえます。このように病理組織学的に良性といわれる脳腫瘍でも,少なからず重篤な内分泌不全や神経脱落症状(後遺症)を残しますし,かつ子供たちを死に導く可能性のある病気です。多くの脳腫瘍において教科書に書かれている組織学的な良性度というのは必ずしも治りやすいということを示しません。良性というべき生易しいものはほとんどないのです。
3. 腫瘍ができた場所による予後の違い
星細胞腫 (WHOグレード2)全体の5年生存割合は70%ですが,一方で,脳幹部に発生した組織学的びまん性星細胞腫 (WHOグレード4,びまん性橋膠腫)の死亡割合はほぼ100%です。この様に組織診でびまん性星細胞腫(diffuse astrocytoma)と病理診断される腫瘍はできる場所によって生命予後に大きな開きがあります。現在ではこの違いは遺伝子変異の違い (IDH mutantとH3K27M mutant) ということがわかっています。
さらに例を挙げれば,右前頭葉の前の方に発生した同じ星細胞腫グレード2でも,類円状で限局性に発育する(固まりになっている)ものとグリオマトーシスのように強い浸潤性格(しみ込むように広がっている)を示すものでは予後は大きく異なります。前者は完全手術摘出のみで治癒しますが,後者は生検術と放射線治療を行っても治ることはほとんどありません。
小脳に発生した毛様細胞性星細胞腫 (グレード1)と星細胞腫 (グレード2)では,32%に増殖停止(大きくならないでそのままいること)が14%に自然退縮(何もしないでも腫瘍が小さくなる)が生じるという報告もありますから,手術の後で取り残した腫瘍があっても何もしないでそのまま様子を見た方がいいこともあるのです。これらの違いは,組織学的な診断(病名)が同じであっても,発生した脳の場所によってそれぞれ治療法を変えなければならないということを示しています。
欧米の1,000例を越えるランダム化臨床試験では,成人のテント上星細胞腫への放射線治療の有効性(生存期間の延長)は証明されませんでした。従ってエビデンス・レベル1(科学的にしっかりした事実)でテント上星細胞腫への放射線治療の適応はありません。腫瘍学の常識では同じ組織型であれば放射線治療の効果は同様であるはずなので,小児の星細胞腫へ放射線治療をしても効かないと推定されます。加えて高いエビデンス・レベルをみれば,星細胞腫グレード2に有効な化学療法剤はなくて,結局,予後に最も大きな影響を与える因子は手術できちんと取れたかどうかということになります。
従ってテント上星細胞腫で理論的に勧められることは完全手術摘出のみです。腫瘍のできた場所によってのみ治療の適否が決まります。でも脳という臓器はこの単純性を許しません,脳のたいせつな場所をまきこむ星細胞腫の完全摘出を計画することはできませんので,多くの星細胞腫では生検術後に放射線化学療法を用いて治療されます。ここには理論的に正しい治療と実際の治療が全然違うというとても大きな矛盾があります。しかし,現実的に臨床の場では,星細胞腫 IDH mutantグレード2に放射線化学療法を行うと,腫瘍が縮小して10年以上変化がないということもめずらしくはありません。
4. 年齢による治療法の相違
脳腫瘍の治療後遺症として知能の発達は大きな問題です。成人の喪失性の認知障害とは異なり,小児の精神発達遅滞あるいはIQ(知能指数)の低下は学習獲得能力の低下によって生じます。少し難しいかもしれませんが,忘れるのではなくて新しいことが学習できないから知能が低下すると考えて下さい。最近では認知機能障害ということばがよく使われます。
認知障害は,脳白質の発達障害が原因とされます。後遺症を大きくする危険因子として,治療されたときの低い年齢,治療からの経過期間,放射線の線量と範囲と部位、手術摘出の部位,水頭症の存在があります。
発達しつつある乳幼児の脳は放射線治療に対してとても弱くて,特に3才未満の小児の大脳に放射線治療を行えば重度の中枢神経発達障害(重い知能低下)を招く確率が高いのです。また3才になってからも成人と同じ放射線治療ができるわけではありません。
年齢が低ければ放射線量を少なくするように微調整するために,小さい子供には治療に必要な放射線を十分使うことができません。ですから低年齢児ほど放射線治療の代わりの化学療法の役割は大きいのですし,またそれによって治療期間が長期になります。
1990年にHoppe-Hirschという人は,髄芽腫の治療を受けた120人の子供たちを追跡して、治療5年後には42%の患児でIQ(知能指数)は80を下回り,治療10年後には85%の患児でIQは80を下回るというとても恐ろしい結果の報告をしました。
2001年のRisらの報告によれば,23.4Gyの低線量脳脊髄照射によっても知能低下は明らかではあるが,旧来の放射線治療と比較すれば知的機能の温存率は改善の傾向があったとしました。彼らの報告でも,患児のIQは1年あたり4.3低下していって,7歳以下で治療を受けると低下率は著しくて,3年以上経過した15症例の平均FSIQ(知能指数)は75.7であり更に低下の傾向をたどるとされています。さらに,5歳以下に脳脊髄18Gyという低い線量も用いられましたが,内分泌機能障害と知能の低下は避けられなかったと報告されました。
放射線治療ばかりが後遺症を大きくする訳ではありません。放射線治療以外の治療方法でも小さな子供たちは障害を強く受けます。低年齢児でのメソトレキセートの髄腔内注入が認知障害を大きくすることも知られていて,よほどの必要性がなければこの化学療法は使用されるべきではありません。でも実際には,髄芽腫やジャーミノーマの治療でメソトレキセートを使っているグループもあります。
PNETは大脳に発生するので認知障害は小脳に発生する髄芽腫より重くなります。治療を受けて生き延びて何年もたってから起る後遺症として,脳血管障害と二次腫瘍の発生リスクは,これも低年齢児の方が明らかに高くて,脳腫瘍の場合においては放射線治療と関連する遅発性合併症であるといわれます。
5. 小児脳腫瘍の臨床研究はむずかしい
全ての小児脳腫瘍は稀少腫瘍(珍しい腫瘍)ですから,統計理論的にはランダム化第II相試験,第III相試験というきちんとした臨床試験を成立させるための登録症例が集められません。そのために確かな事実に基づいた標準プロトコール(治療計画)を作ることが困難なのです。
もちろん,髄芽腫を100例以上あつめて臨床研究ができればよりよい治療の方法が見えてくるのですし,小児脳腫瘍でも設定根拠のある対象集団に対して根拠のある計画治療を行う集学的治療の第II相試験でレベル3の有効性と安全性を検証することは可能でしょう。(ちょっと理解できませんか?) 要するに小児の脳腫瘍研究は大規模にはできないのです。この脳腫瘍の特徴を踏まえて,世界脳腫瘍会議では小児も含めた脳腫瘍の第I相と第II相試験のためのガイドラインを作成しています。
学会でlow-grade glioma(悪性度の低いグリオーマ)の治療という発表を聞くことがあります。ある日本の研究グループに登録された”low-grade glioma”に一定の化学療法を用いて治療した成績の発表などです。でも,このlow-grade gliomaという呼び名は治療方法を検証するために一つに括ることができる設定根拠のある単一対象集団ではありません(違ったものを十葉一絡げにして研究してはいけないという意味です)。だから,このような学会発表には意味がありませんが,学会で発表された成績というと一般の人には本当のことのように思えてしまいます。
逆に病理学的に悪性度の低いグリオーマの治療方針は個々の患者さんにおいて千差万別です。ヘテロな対象集団にヘテロ(個々においては適切)な治療を施すことを許容することが認められなければならない腫瘍に,研究プロトコールに基づいた治療を安易に設定することには危険があります。これは治療方針がきちんと立てられているからといってその治療が正しいということではなくて,逆に一つの方針でおおざっぱにまとめて治療しているから間違っているということです。
小児脳腫瘍治療の最終目標はこどもの病気を治すことです。しかし,効果的な治療には少なからず代償があります。ですから,効果的な治療とその治療毒性の間のバランスをとても慎重に取らなければなりません。例えば,大量の化学療法や放射線治療あるいは積極的な外科摘出が,高い治癒率をもたらすのと同時に,重い後遺障害を残すことがあります。逆に,治療の毒性(有害事象・副作用)を最低限にしようとすれば,腫瘍の再発率を高める結果にもなるのです。例を挙げて言えば,こどもの髄芽腫に放射線治療を全くしないで大量化学療法だけで治そうという方針を,よく検討もせずにいきなり立てたとしましょう。これは治療不可能な再発を招く確率を高める可能性のある挑戦です。広範囲な脳への放射線治療が有害なので,ガンマナイフでジャーミノーマを消してしまおうという方針を立てたとしましょう。腫瘍は確かに一度は消えるのですが,容認できないほどの再発に遭遇します。治療法の改善は何年もかけてゆっくり進歩するのですから,副作用を避けるためとはいえ,思い切った挑戦というものは治療方針の中には含めてはなりません。
小児の脳腫瘍は標準化して治療計画を立てることが難しいし、科学的な画一性を求める臨床研究の発展は小児脳腫瘍の極めて高い多様性との背反の中にあることも逆に認識されなければなりません。一見きちんとした治療方針で治療しているということが,それぞれの子供たちにとっては正しいことではなくて,きめ細かな治療計画がないがしろにされていているということもあるのです。
2016年にWHO分類が改訂され,脳腫瘍は分子診断されることになりました。毛様細胞性星細胞腫,髄芽腫,上衣腫,びまん性中心性リオーマなどの小児腫瘍も例外ではなく,それでなくとも希少腫瘍である個々の小児脳腫瘍がさらに細分類されました。一方で,やエビデンスレベルが低いながらも信頼しうる文献情報を基に行われてきた治療は,分子診断による差別化により頼るべき微かな情報さえも失った感があります。ガイドラインの作成には数年の時間を要し,新たな治療プロトコール作成には症例集積が見込めず,小児がん拠点病院が決定された後も拠点化が進まない,本邦の小児脳腫瘍治療の方向性を決める組織構築が課題となっています。組織構築とは忙しい臨床医が兼務してできる業務ではなく,多くの専従職員を有する体制が不可欠です。
代表的脳腫瘍の治療方針
ほとんどの腫瘍の治療方針は左枠の小児脳腫瘍サブメニューに書いてありますから探して下さい
髄芽腫(ここをクリックして下さい)
胚細胞腫瘍(ここをクリックして下さい)
乳幼児の毛様細胞性星細胞腫(ここをクリックして下さい)
上衣腫(ここをクリックして下さい)
悪性神経膠腫とテモゾロマイド(ここをクリックして下さい)
小児科医と脳神経外科医の役割
多くの腫瘍型において外科摘出が予後を決定する最も重要な因子ですから,特に治療初期では脳神経外科医が果たす役割が最も大きく,外科手術の成績が予後を左右します。またいうまでもなく,従来から間脳下垂体不全の治療,精神発達遅滞・認知機能障害や症候性てんかんへの対処は小児科医に依存しています。近年では,前述のように腫瘍型によっては化学療法が重要な役割を果たすことが明らかとなってきていますから,悪性度の高い小児脳腫瘍では診断時からの小児腫瘍医の関与が重要です。
日本においての小児脳腫瘍症例は多施設に分散していて,小児脳腫瘍の治療体制と水準は望むべきレベルにはありません。小児脳腫瘍の治療を行うためには,小児の中枢神経系に造詣の深い放射線治療医と神経病理診断医の協力,眼科と耳鼻科の存在,稀少疾患治療ゆえの施設内倫理委員会の認証,保健審査と医療費対策,看護師教育,調剤の安全確保と無菌管理のための設備,多彩な予後に応じたインフォームド・コンセント,患者・家族教育と精神的支援,小児慢性疾患の迅速な手続き,家族の宿泊施設斡旋,院内学級教育,病棟内での患児と母親のストレス解消の援助など様々な対応をしなければなりません。だから地域ごとの小児脳腫瘍治療施設のセンター化が強く望まれている時代です。
上述したように全ての小児脳腫瘍は稀少腫瘍(数が少なくて珍しい)で治療方法はいちいち異なるものです。治療長期予後を慎重に考えた上での成績向上と日本においての小児脳腫瘍学の発展のためには,例外をなくして全ての症例を登録して検証する体制の整備が不可欠なのだと私は考えています。小児がん学会の努力はこれを目指してはいますが,残念ながら脳神経外科学会の中でのこの問題の認識はとても低いです。
ある米国の小児神経腫瘍医(pediatric neuro-oncologist)が,小児脳腫瘍の治療法の選択は常にcase-to-case decisionであるといった演説を聞いたことがあります。ひとりひとりの子供で違う治療を考えなくてはいけないし,まとまった治療方針で単純に治療できるものではないという意味です。残念ながらcase-to-case decisionできる経験が豊かな小児神経腫瘍医は日本にはいません。私自身も脳神経外科医としての少ない知識と経験の中で患児を治療しているのが日常ですし,日本での小児神経腫瘍医の育成を急がなければならないでしょう。
新しい分子標的治療の開発
遺伝子診断の発達で小児脳腫瘍の発生原因はかなり解明されてきました。でも長い間,それに対応した治療法が見つかりませんでした。しかしわずかながらも発展はあり,BRAF v600 mutationを有する小児グリオーマには,ダブラフェニブ (Tafinlar) と トラメチニブ (Mekinistの有効性が確認されました。2023年に米国FDAが承認し一般的に使用できるようになりました。多型黄色星細胞腫 PXAや神経節膠腫,毛様細胞性星細胞腫などが対象です。
まとめ
 脳腫瘍は小児に発生する固形癌の中では最も頻度が高く,かつ死亡率の高い疾患です。脳腫瘍は他の臓器の腫瘍と比べて病理組織が多彩で,全ての脳腫瘍は稀少疾患(とてもまれな病気)といえます。さらに病理組織診断が同じであっても発生する部位と患者さんの年齢によって予後が変わるために治療法の選択が複雑になります。低年齢児の脳は放射線治療でとても障害を受けやすいので,化学療法が重要な治療手段となっています。髄芽腫や胚細胞腫瘍などの悪性腫瘍では脳神経外科医と小児科医の協力が欠かせません。
脳腫瘍は小児に発生する固形癌の中では最も頻度が高く,かつ死亡率の高い疾患です。脳腫瘍は他の臓器の腫瘍と比べて病理組織が多彩で,全ての脳腫瘍は稀少疾患(とてもまれな病気)といえます。さらに病理組織診断が同じであっても発生する部位と患者さんの年齢によって予後が変わるために治療法の選択が複雑になります。低年齢児の脳は放射線治療でとても障害を受けやすいので,化学療法が重要な治療手段となっています。髄芽腫や胚細胞腫瘍などの悪性腫瘍では脳神経外科医と小児科医の協力が欠かせません。

現在日本では小児脳腫瘍の症例はたくさんの施設に分散していて,全ての子供たちに高い水準の治療ができていないこともあり,地域ごとの治療センターを確立することが望まれています。また,複雑な治療法の選択は常にcase-to-case decision(個々の患者で逐一異なること)であり,深くてレベルの高い知識をもち経験豊かな小児神経腫瘍医の育成が求められています 。
雑多な知識
2020年の段階で,小児脳腫瘍の全ての遺伝子を調べたら利益があるのか?
Wong M: Whole genome, transcriptome and methylome profiling enhances actionable target discovery in high-risk pediatric cancer. Nat Med 2020
全ての腫瘍と生殖系列ゲノム,RNAがシークエンスにかけられました。要するに腫瘍に関して全ての遺伝子変異が調べられたということです。76例の中枢神経腫瘍でDNAメチル化を調べて見たところ,71%で診断が確定でき,2.6%(2例)で診断が変わりました。というくらいの成果が得られたそうです。遺伝子検査が小児脳腫瘍の治療の成果を向上させるには,まだまだ遠い道のりがありそうです。

