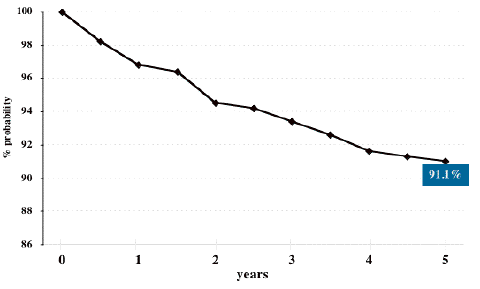ジャーミノーマ(胚腫)germinoma
intracranial germinoma, CNS germinoma
ジャーミノーマの再発の相談を受けることがあります
放射線治療の領域が狭い(局所照射)ために生じることがほとんどです
全脳室もしくはより広い照射野を選ばないと、高率に再発する腫瘍です
大切なこと
- ジャーミノーマは脳にできる胚細胞(はいさいぼう)腫瘍の70%を占めます
- 平均年齢は15歳,男の子に多い腫瘍です
- 下垂体,視床下部,松果体,大脳基底核という場所にできます
- 松果体ジャーミノーマは性差があり,男児に多いです
- ジャーミノーマは悪性腫瘍ですが,きちんとした治療をすれば95%以上は治ります
- 診断はMRIでほとんど分かります
- 診断に影響が出るので,脳血管撮影やCTなどのX線検査を避けます
- 手術は無理のない生検術(ちょっと取る)以外に必要ありません
- 手術でたくさん取るのは手術の危険が高くなるだけで何の利益もありません
- ジャーミノーマを疑って手術をするのならできるだけリスクの少ない手段を選ぶべきです
- 水頭症にはシャントは必要ありませんし,行ってはいけません
- 内視鏡による第3脳室開窓術で水頭症を治すことができますが,ある程度のリスクがあります
- シャントをどうしてもしなければならないと判断したら,そうしないで長期留置型の脳室ドレナージを設置します
- MRIで見えるより,実際には腫瘍は周囲に隠れて広がっています
- 脳室の解剖図の壁に沿って広がっていく性質をもっています
- 化学療法と放射線治療をうまく組み合わせて治すのが世界標準になりました
- 1-2コースの化学療法(制がん剤)でほとんど無くなります(消失)します
- 化学療法は3から4コースしますから,3から4ヶ月くらいかかります
- 放射線治療は低い線量(23.4から25.2グレイ)で全脳室をカバーできるようにかけます
- ジャーミノーマの治療に局所照射、拡大局所、定位照射、ガンマナイフを使ってはなりません,再発します
- 30グレイ以上の高い線量では脳の障害(高次脳機能障害・認知機能・知能の低下,下垂体機能低下)が出る恐れがあります
- 後遺症は手術と放射線できまりますから,それをできる限り低侵襲に押さえるのが治療のコツです
- 多い量の化学療法だけで治そうという試みがありましたが失敗に終わりました
- 極めて稀に! 髄液にのって脊髄に播種(転移)することがありますが,治ります
- メソトレキセートMTXの髄腔内注入はしなくても治りますし,有効性は全く示されていないのでしてはいけません
- 内分泌(下垂体ホルモン)障害を持つ患者さんが多いので内分泌の専門家に診てもらう必要があります
- 2023年、私がジャーミノーマを確実に治せると考える治療法は、ICE (IFO/CDDP/VP-16) 化学療法3コースの後で、25.2グレイ14分割の全脳室照射を加えることです
- これで、社会復帰もできますし、遅発性障害もなく、ほぼ治癒します
- 10年長期生存割合は「100%に近い」と期待できる時代になりました
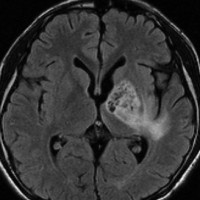
ジャーミノーマの最大の特徴は脳室上衣下浸潤 subependymal infiltration ですからそれを念頭にいろいろ考えます
ジャーミノーマの診断
症状
- 尿崩症(水をたくさん飲む)で発症することが最も多いです
- 視交叉に浸潤するものでは,視力低下と視野欠損がでます
- 松果体にできたものでは水頭症になって頭痛,嘔吐,複視(物が2重にみえる)がでます
- 小学校に入った頃から背が伸びない(低身長)
- ゆっくり手足の麻痺が進んだり,性格変化(多動,ADHDなど)が悪化するのは大脳基底核ジャーミノーマ
MRI
- 治療の前に必ずガドリニウム造影剤を使って全部の脳と脊髄を検査します
CT
- 行う必要がないし基本的に診断のためのX線CTをしてはいけません
- ジャーミノーマかLCHかを疑ったときにCTをすると,それだけの被曝で腫瘍細胞が消えてしまって,生検術で腫瘍が証明されないということがしばしばあるからです
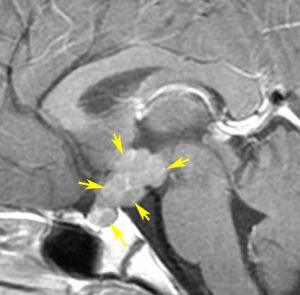
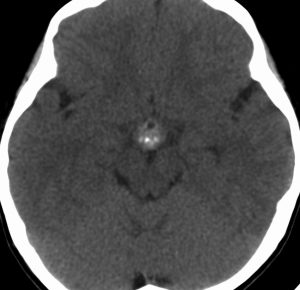
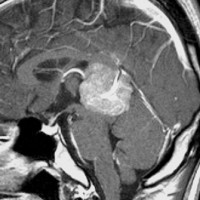
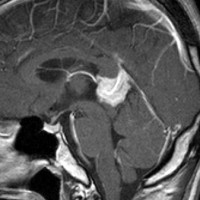
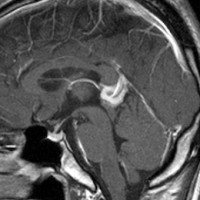
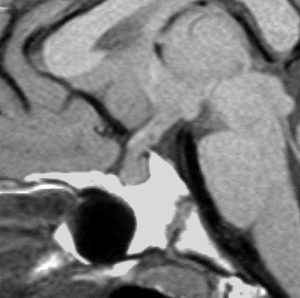
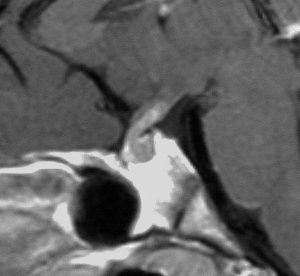
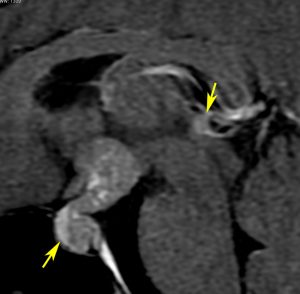
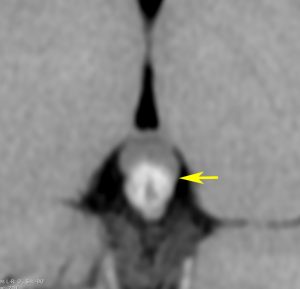
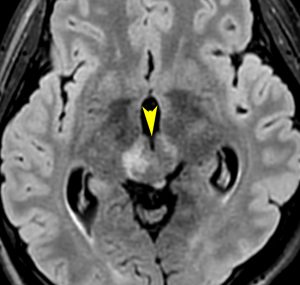
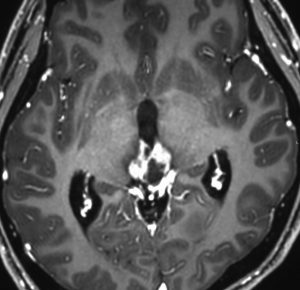
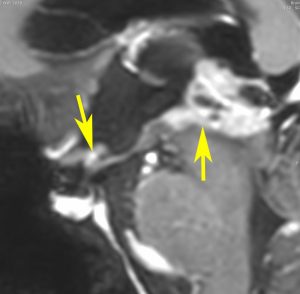
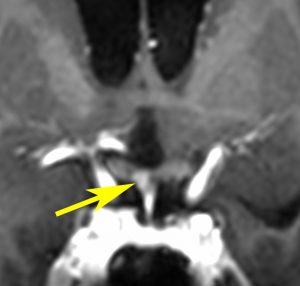
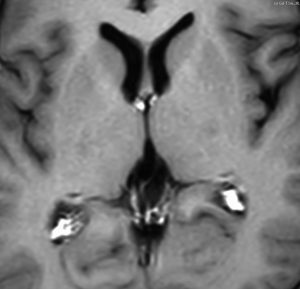
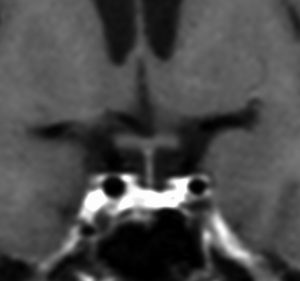
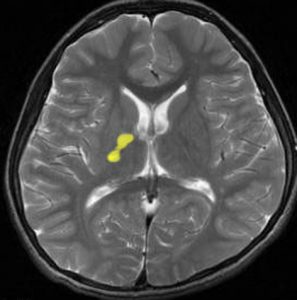
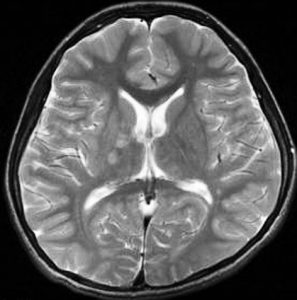
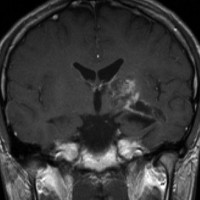
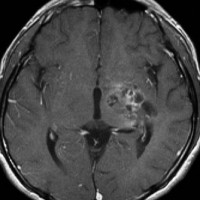
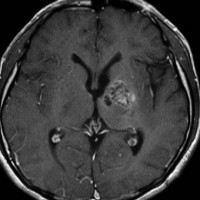
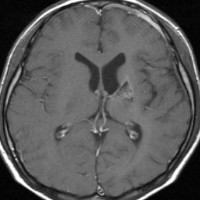
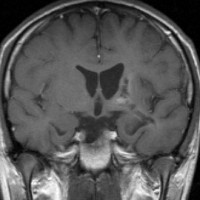
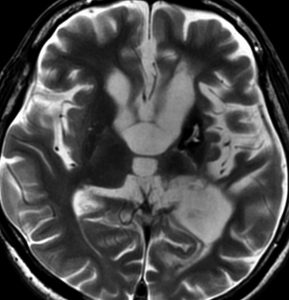
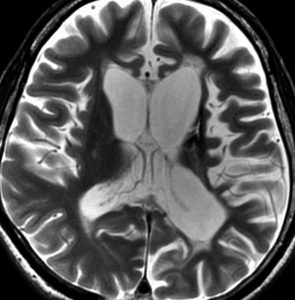
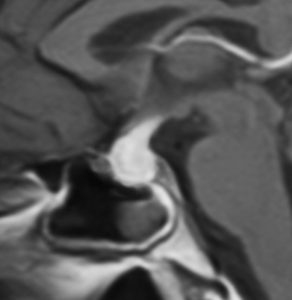
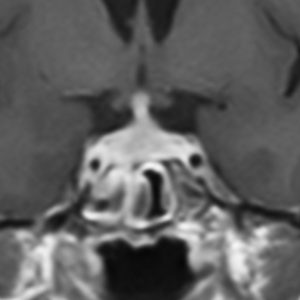
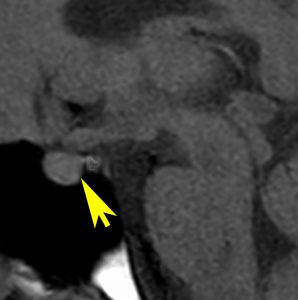
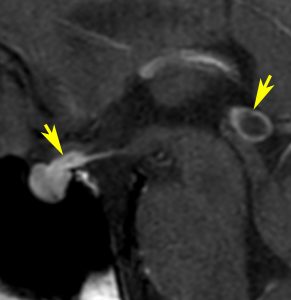
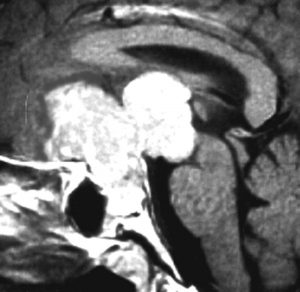
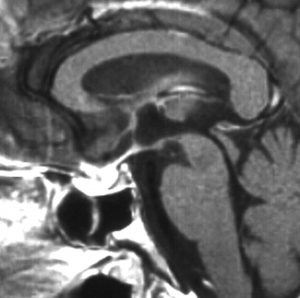
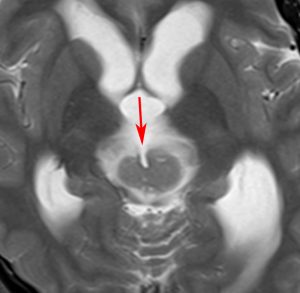
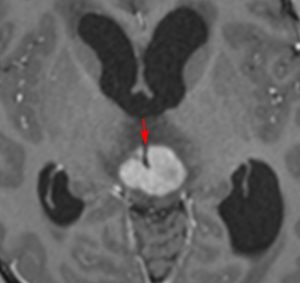
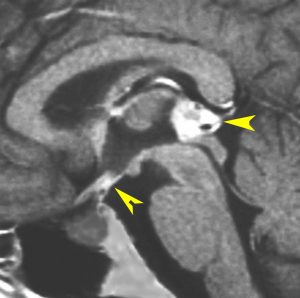
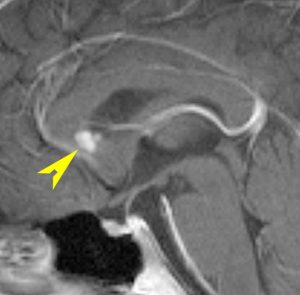
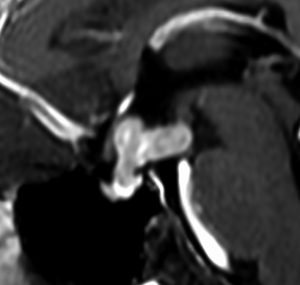
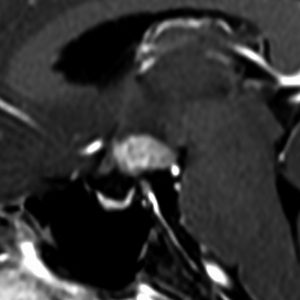
10歳くらいから身長の伸びが遅くなって,12歳で食欲低下と体重減少がありました。左のMRIはガドリニウム造影MRIで,視床下部と下垂体を侵す神経下垂体ジャーミノーマです。CTでは小さな石灰化(白い点)がみえます。CT検査は不必要なものでした。
腫瘍マーカー
- 入院したらすぐに血液のHCG-β (ベータ)とAFPは必ず調べます
- とても精密な方法で測定するとすべてのジャーミノーマでHCGは陽性になります
- 髄液のPLAPを調べます,髄液HCG-betaはできれば測定した方がいいです
- 小さなジャーミノーマでは,通常検査のHCG-betaは陽性になりませんから要注意
- 髄液と血清を検体として,超高感度HCG-beta測定,PLAP測定という検査をすると陽性値にでます
手術
- 画像だけでは間違うことがありますから生検術(腫瘍をちょっとだけ取る手術)をします
- なるべく開頭手術をしないで内視鏡手術,経蝶形骨洞手術,定位脳手術を選びます
- 手術が危険な場合には生検術をしないで画像診断だけで治療に入ることもあります
- 松果体のジャーミノーマで閉塞性水頭症を合併している時には,生検術と同時に,第3脳室開窓術をすれば改善することができます
- でも内視鏡を使うのでリスクもあり無理をしないことが肝要です
- 化学療法を1コースすれば数日で閉塞性水頭症が改善することが多いので,水頭症に対しては,まずはシャントをしないで外ドレナージで回避するという選択肢が有力です
髄液細胞診
- 髄液細胞診は必要ありません
- 髄液細胞診は擬陽性が多いので,陽性という結果でも安易に髄液播種として治療をしてはなりません
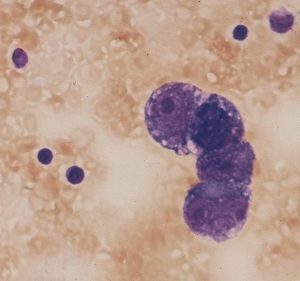
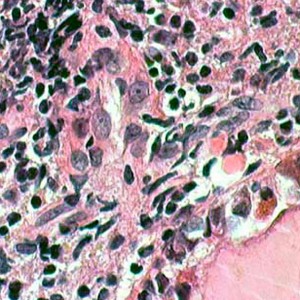
これは1994年の脳室液細胞診で,大型の核小体を有する腫瘍細胞があります
しかし,ジャーミノーマの髄液播種は実際にはほとんど無いといえるくらい珍しいものです
多くの場合,MRIで播種と読影されても,脳室壁上衣下伸展を播種と読み間違えているだけなのです
ジャーミノーマの髄液播種という診断は,「脳室外の脳脊髄表面に結節状の腫瘍」がMRIではっきり認識できた時のみです,細胞診では決まりません
内分泌検査
- 尿崩症で発症したら,下垂体前葉機能も調べておきます
- 低ナトリウム血症で発症する例では,間脳下垂体機能低下があります
- 低身長で発症すれば,内分泌検査は詳細になされているのが通常です
- 腫瘍が下垂体に見えなくても,下垂体機能が低下していることがあるので調べておきます
- 松果体腫瘍だけMRIでみえても,間脳下垂体機能低下がありえます,画像では見えない視床下部浸潤を生じているからです
- 特に隠れ尿崩症 occult DIがあるかどうか見極めておくことが大切です
- コートリル(副腎皮質ホルモン)を投与すると隠れ尿崩症が顕在化することがあります
- 手術前に高度の下垂体機能低下があっても,治療で改善することがあります
- ですから,腫瘍が治ってからも下垂体機能がゆっくり改善するかどうか,また内分泌検査を続けなければなりません
視力と視野検査
- 意外に気づかれないのですが,特に視床下部と下垂体のジャーミノーマでは視力と視野が低下することが多いです
- まだらな視野欠損になることがあります
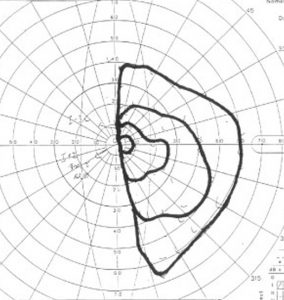
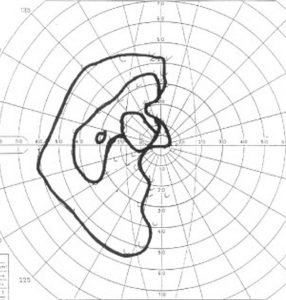
10歳の女の子が視力視野障害と尿崩症で発症しました。視力がとても低くて両耳側半盲ですが,まだらな視野欠損になっています。ジャーミノーマが視交叉を圧迫するのではなくて視交叉組織を破壊性に浸潤するから,視野障害が治らないことがあるので治療を急ぎます。
ジャーミノーマにおすすめの化学療法(1コースにつき)
CARE化学療法(ケアーと呼びます)
- カルボプラチン(商品名パラプラチン) 450mg/sq.m 1日のみ
- エトポシド(商品名ベプシド,ラステット) 150mg/sq.m 1日目から3日目まで
- 最近,CARE化学療法と23.4グレイの脳室照射で治療された患者さんの再発の相談を受けます。この組み合わせの治療強度が弱いという恐れがあります。全国で共同研究がなされてずいぶん経っているのですが,raw dataの公開と正式なinterium reportが出されていません。
EP化学療法
- シスプラチン(商品名ランダ,ブリプラチン) 20mg/sq.m 1日目から5日目まで
- エトポシド(商品名ベプシド,ラステット) 100mg/sq.m 1日目から5日目まで
PE化学療法
- シスプラチン(商品名ランダ,ブリプラチン) 90mg/sq.m 1日目
- エトポシド(商品名ベプシド,ラステット) 150mg/sq.m 1日目から3日目まで
ICE化学療法(アイスと呼びます)
最も確実で有効性が高い化学療法です
- イフォスファミド(商品名イホマイド) 900mg/sq.m 1日目から5日目まで
- シスプラチン(商品名ランダ,ブリプラチン) 20mg/sq.m 1日目から5日目まで
- エトポシド(商品名ベプシド,ラステット) 60mg/sq.m 1日目から5日目まで
-
- シスプラチンの代わりにカルボプラチンCBDCA が使用されることもありますが,シスプラチンの方が奏功率は高いです。
- 小児科病棟で,これらの薬剤を点滴で落とします
- ケアーの方がお医者さん(脳外科医)は楽にできるかもしれません,しかし,より化学療法強度が高いのはICE化学療法です
- 血液腫瘍を扱う小児科医にとっては,ICE化学療法は簡単なとても軽い治療法とも言えます
- 大きなもの,非常に広範囲なもの,大脳基底核のもの,播種などがある症例,あるいは再発ではICE化学療法(クリックで内容)を使った方がいいでしょう
- 尿崩症のある例ではデスモプレッシンを中断しないで使いながら化学療法をします
- 化学療法中にデスモプレッシンを中止すると低ナトリウム血症になることがあります
- 1コースの化学療法でほとんど消失します,そうでない場合は混合性胚細胞腫瘍の疑いがあります
- 予定の化学療法は3コースです
- 予定の化学療法が終わったらすぐに全脳室の照射に入れます
- もし脳脊髄照射を使う時には最後の化学療法の骨髄抑制が過ぎてからします
- MTXメソトレキセートの髄腔内投与はしてはいけませんし,する根拠は全くありません
ICE化学療法投与開始から数日で小さくなります
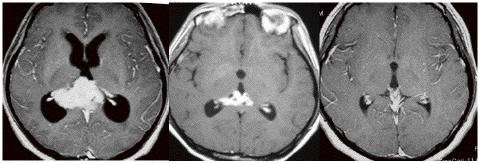
この例は古いので第3脳室開窓術 ETV をしていません。左はICE化学療法前。中央は9日後。右は25日後です。閉塞性水頭症があっても1週間くらいで中脳水道が通って水頭症は改善します。ジャーミノーマであれば,ICE化学療法1コースでかなり縮小するはずです。このような顕著な効果がない時には,逆にジャーミノーマ以外の胚細胞腫瘍が混在していると考えた方がいいでしょう。多くは奇形腫の混在です。
化学療法後残存腫瘍に局所照射を追加しない
- ジャーミノーマの化学療法はうまく行っても,とても小さな残存腫瘍のようなものが残ることがしばしはあります (nealy CR)。これはgranulomatous reactionと呼ばれる瘢痕様の組織が残るからです。ですから,ジャーミノーマが消えていないからといって,全脳室照射や全脳照射の後に,さらに局所照射をする必要はありません。またこの残渣のような小さな病変から再発することはありません。
ただし,奇形腫が混じっている場合には,はっきりした残存腫瘍が残りますから,放射線治療開始前に,手術をして残存腫瘍を摘出する必要があります。病理診断を決定して放射線治療の線量と可否の決定をしますので,放射線治療の前なのです。この判断は時として難しいものですが,できます。
ジャーミノーマの放射線治療
- 化学療法が進むとジャーミノーマであればかなり小さくなりますから,それから放射線治療をします
- 放射線治療は,化学療法の反応性がジャーミノーマだと確定できてから行います。
- ですから,化学療法が終了して,画像変化でほとんどの腫瘍が消失しているのを確認してから開始するべきです。
- 原則として全部の脳室をカバーできるような全脳室照射 WVI whole ventricle irradiation をします
- 脳室上衣がある部分すべてと下垂体をカバーします,特に延髄下端 ovexを外してはなりません
- 標準的に線量は24グレイという量を12回(1回線量2グレイ)に分けるか,25.2グレイを14回(1回線量1.8グレイ)に分けてかけます
- 最近は23.4グレイ/13分割も試験されていますが,完全治癒割合が確実に高いかどうかはまだ証明されていません,脳が脆弱な7歳以下の年少児では検討されるべき線量でしょう
- 18グレイで治るという根拠はありません,行うときは試験です
- 1週間に5回かけるのが通常の方法です
例外に注意
- 髄液播種と脊髄播種などの転移がある例では全脳脊髄照射 craniospinal RTが必要です(線量は同じ)
- 大脳基底核ジャーミノーマでは全脳照射 whole brain RTが必要です(線量は同じ)
放射線が外れやすい部位は再発源となります
側脳室先端(前角,後角,側頭角,閂),下垂体と大脳基底核に放射線が入らないとその部位から再発します。
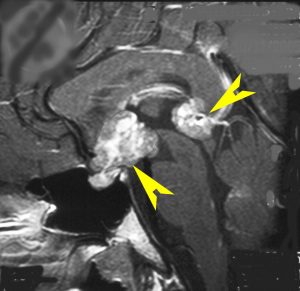
再発ジャーミノーマの画像です。延髄背側の閂 ovexという部位に再発しています。
このパターンはとても多いです。なぜかというと,全脳室照射の時に,第4脳室下端のovexの上衣 ependyum を照射野に入れない放射線治療医の先生がいるからです。放射線科の先生にもちょっとした知識が必要なのです。
これは再治療で腫瘍が消えても不可逆的な重症の延髄障害を残してしまいます。
初期治療では定位照射を使わない
- ジャーミノーマは浸潤性の腫瘍(しみ込んで広がる)ですから,ガンマナイフ,サイバーナイフなどの定位放射線治療を使って治療すると,放射線がかかっていない場所から高率に再発します。MRIで見えない脳室壁にもジャーミノーマ細胞がいます。
化学療法後残存腫瘍に局所照射を追加しない
- ジャーミノーマの化学療法はうまく行っても,とても小さな残存腫瘍のようなものが残ることがしばしはあります (nealy CR)。これはgranulomatous reactionと呼ばれる瘢痕様の組織が残るからです。ですから,ジャーミノーマが消えていないからといって,全脳室照射や全脳照射の後に,さらに局所照射をする必要はありません。またこの残渣のような小さな病変から再発することはありません。
ただし,奇形腫が混じっている場合には,はっきりした残存腫瘍が残りますから,手術をして残存腫瘍を摘出する必要があります。この判断は時として難しいものですが,できます。
IMRTで海馬を避けると側頭角からの再発がある
- 認知機能低下を防ぐために海馬を避けてIMRTで治療をしようという試みがあります。そうすると側脳室側頭角の脳室壁に不十分な線量しか入りません。側頭角からの再発の頻度は高いのです。IMRTでは,大脳基底核からの再発例もあります。脳室上衣をすべてカバーするのは大原則ですし,大脳基底核にある程度の線量が入る従来型の放射線治療のほうがよいのかもしれません??
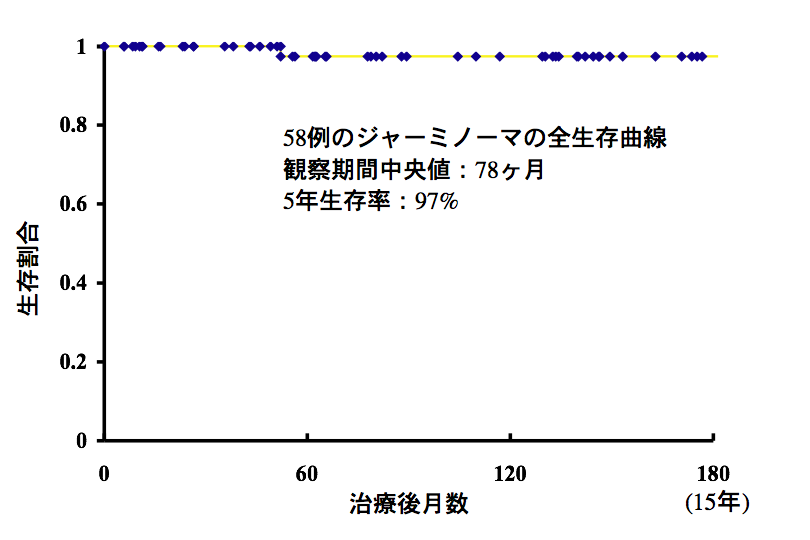
ジャーミノーマの生存率
このグラフは私の手元で1992年から新たに治療した58人の患者さんの2008年までの生存割合を表しています。上に書いたような化学療法を先にして,あとから24〜25.2グレイの放射線治療をする方法です。ジャーミノーマが直接の原因となって1人の患者さんが亡くなっています。また,10人の患者さんが再発しました。でも再発時の治療がうまく行ってこの結果になっています。再発率(17%)がとても高かったのですが,それは初期(2000年以前)に放射線治療の領域 (field) を絞りすぎた(involved field irradiation)ことが原因です。全脳室以上の照射野では再発はほとんどありません。この生存率は例外的であり,現在の治療法を用いても10年生存割合は90-95%くらい,10-20人に一人くらいの患者さんは死亡すると考えなければなりません。多くの原因は初期治療のミスや視床下部下垂体不全です。実際に私は2000年以降で治療したジャーミノーマの患者さんで死亡した方をみたことがありません。治療は進歩しています。
ジャーミノーマの日本での臨床研究 JCCG CNSGCT2021
初発中枢神経原発胚細胞腫瘍に対するランダム化比較試験
京都大学の荒川先生が中心となって行われている臨床研究です。化学療法は、CE療法(carboplatin 560 mg/m2 day1, etoposide 150 mg/m2 day1-3)、PE療法(cisplatin 90 mg/m2 day1, etoposide 150 mg/m2 day1-3)の交代療法を計4コース実施する。放射線治療は、1コース目の化学療法開始日から2コース目の化学療法開始日までに開始する。病巣に応じて全脳照射もしくは全脳室照射23.4 Gy/13回を実施する。B1群は,照射線量を18 Gy/10回まで落とします。全脳室照射18グレイでジャーミノーマが治るかどうかということをみるがための試験です。
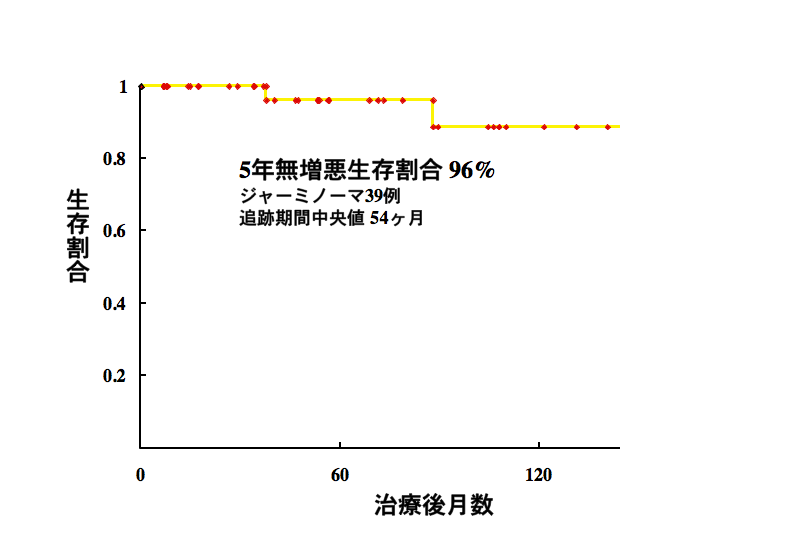
ジャーミノーマの再発のない生存割合(無増悪生存割合)
前のデータで、狭い範囲の放射線治療では再発率が高いと書きました。このデータは全脳室以上の広い領域で24〜25.2グレイの放射線治療を行ったジャーミノーマの患者さんの再発がない状態での経過を示します。全脳室以上の放射線治療を用いれば再発する確率は5%くらいと見ることができます。
このデータをまとめた2009年以降から2020年まで,私の手元で23例のgerminomaを治療しました,主としてICE化学療法3コース,25.2グレイ14分割の全脳室照射です。1例 (4%)で治療6年後に再発がありました。この例の初期治療を調べ直したら,第4脳室下半部 (ovex)に放射線が入っていませんでした。放射線治療の担当先生には照射の前に念を押してお願いしたのですが,聞いていただけなかったためです。とても残念です! きちんと治療すれば,100%治る腫瘍だと今は考えています。
もし再発してしまったら
再発治療でも放射線治療を加えないと,またすぐに再発します
大量化学療法でも治しきれないことがほとんどです
- ほとんどは照射野外再発です
- 原則として,上に書いてあるような初発の時と同じ治療をします
- まず化学療法をします(ICE化学療法がいいでしょう)
- それで腫瘍がほとんど消えたら,あと2コース追加します
- それからまた放射線治療をします(24グレイを12回か25.2グレイを14回)
- 初回治療での放射線量によって追加照射の量が25グレイまで使えない時は18グレイとか20グレイくらいに落とすこともあります
- 最後の治療になるでしょうから,可能であれば照射の範囲はできれば全部の脳と脊髄にかけます,知能予後を考えながらもできるだけ広く
- 早期照射野外再発あるいは極小の再発病変で,広範囲照射を用いることにリスクが高い場合は,marginを広めに取った局所照射を選択します
- 初回治療で放射線がたくさんかかっていて,追加照射ができない時にはとても困ります
- そのような場合は最初から末梢血幹細胞救援を使う大量化学療法を計画しますが,抑えきれないことが多いです
- 私が経験した25例の再発ジャーミノーマの無増悪5年生存割合は70%でした
- 初回治療で低線量照射が使われていた再発例では,再照射が応用できるので再発治療に失敗することはほとんどありませんでした
ここから下は難しい
ジャーミノーマには脳室を全部含むかそれ以上の照射野が必要
Calaminus G: SIOP CNS GCT 96: final report of outcome of a prospective, multinational nonrandomized trial for children and adults with intracranial germinoma, comparing craniospinal irradiation alone with chemotherapy followed by focal primary site irradiation for patients with localized disease. Neuro Oncol, 2013
2013年の報告です。190例の患者さんが脳脊髄照射のみの治療を受け,65人の患者さんが2コースの化学療法 (CBDCA/VP-16 alternating with VP-16/IFO)と局所放射線治療を受けました。5年の時点のEFSとOSは有意差はありませんでしが,PFSは0.97と0.88 (P<0.04)で差が認められました。化学療法と局所照射で治療された65人のうち7人で再発があって成績が悪かったのですが,その内の6人は照射野外かつ脳室内での再発でした。結論として,照射野に脳室を含むべきであると述べています。脳脊髄照射を受けた125例中 4例 (3%) で再発が生じています。
「解説」2013年になって,何を今さら!という論文です。そもそもジャーミノーマは脳室壁全体を侵す腫瘍なのです。ヨーロッパの人々もようやくのことでそれに気づいたのかも。日本の小児科医の一部分ははまだ気づいていません。
この報告では,脳脊髄照射で治療された場合,CSI 24Gy/15fr と boost 16Gy/10frが原発巣に入っています。神経下垂体ジャーミノーマだと視床下部下垂体が40グレイも被爆しています。その線量が入ると視床下部下垂体障害,認知機能低下,ウィリス動脈輪閉塞症,2次腫瘍ができるから線量を落とそうというのが20年前からの日本でのコンセンサスです。
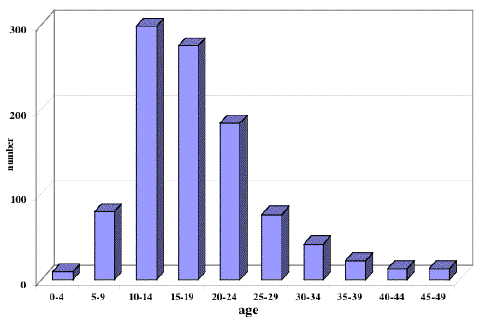
発生する年齢
germinomaは中枢神経系原発胚細胞腫瘍の3分の2強を占める頻度の高い腫瘍です。図2に見られるように15歳をピークとして小児期から思春期に多いものです。注目しなければならないのは10歳以下の小児にも稀ではないことです。同様の治療を全年齢層に行った場合,10歳以下の年齢層に対しては放射線治療による遅発性認知機能障害はより大きいと考えなければなりません。
ジャーミノーマの年齢別発生頻度
ジャーミノーマ(胚腫)のMRI診断
germinomaのMRI所見は,ガドリニウム像強T1強調画像で強く増強されることです。しかし,嚢胞性変化を伴うことも少なくないし,大きな多房性の腫瘍となることもあります。MRI上では一見境界明瞭に見えますが,実際には画像でみえなくともかなり広範に周囲へ浸潤していることが多いので限局性腫瘍とは考えてはいけません。それが手術摘出だけあるいはガンマナイフなどの定位照射で治らない理由です。
germinomaが好んで発生し浸潤する部位は,松果体,視床下部,下垂体柄,下垂体後葉,下垂体前葉,視床,終板,第3脳室壁,側脳室壁の特に前角,前交連,大脳基底核,脳梁膝部,中脳視蓋,第4脳室壁 (obex),海綿静脈洞,蝶形骨洞斜台などです。これらは直接浸潤であり,播種あるいは転移ではありません。
時に脳室上衣に沿って脳室壁へ広範に浸潤する特徴があります。この脳室上衣下浸潤 subependymal infiltration は,初期には高解像度 3-tesla MRIでも描出できませんが,進行すると脳室壁に結節状の多発病変として描出されてきます。
一方,脊柱管内に認められる病変は髄液播種であり,上衣下浸潤 subependymal infiltration と髄液播種 CSF dissemination/seeding を混同してはいけません。診断時には脊髄のMRIも必ず撮影します。でも,ジャーミノーマの髄液播種というのは,実際にはほとんど無いといえるくらい頻度の低いものです。
germinomaの画像診断で注意しなければならないものに,occult (neurohypophyseal) germinomaと呼ばれるものです。一つは,尿崩症で発症する小児例にみられるものであり,発症時にMRIを撮像しても腫瘍陰影が捉えられません。この場合には,突発性尿崩症と診断されて治療を受けることが多いのですが,MRIを反復するうちに発症から数ヶ月あるいは数年を経て神経下垂体に腫瘤が出現します。初発時のMRIをよく観察すると後葉のbrightness (ADH) が消失していたり,下垂体柄が腫大していたりする初期像を見逃している場合が多いでしょう。MRIで松果体の単発germinomaと診断された例で,下垂体機能を検査してみるとGHDがあったりmasked DIを認めることがありますが,この場合にはocult germinomaが併存しています。とても重要な所見として,CT検査をすると病変が消えてしまうことです。CT検査の後では下垂体は萎縮像となり経過することがあります。これはgerminomaが放射線感受性が高いために一度のCT検査で使用するガンマ線量だけで腫瘍消失が生じるためです。でもまた数年後に再発します。
もう一つは,高次脳機能障害や緩徐進行性の片麻痺で発症する小児の大脳基底核ジャーミノーマ basal ganglia germinomaです。この腫瘍も腫瘤陰影が全く見えず,大脳半球の委縮像のみが画像上の所見であることがありますが,この大脳基底核germinomaの画像所見は特有なものです。CT/MRIガイド定位的生検術によりgerminomaの確定病理診断をつけることはできますが,大脳基底核germinomaは出血しやすくて脳内血腫という合併症を生じることが稀ならずあるので,T2/FLAIR画像で内包に限局するような小さな病変のみの場合は生検術は避けた方がよいです。メチオニンPETで高集積が認められ,この検査は診断的価値が高いといえます。血清髄液のHCG値がごく微量に陽性値となります。
尿崩症にて発症した2年後にようやく小さなneurohypophyseal germinomaを発見された9歳女児例です。術前のT1強調画像では下垂体後葉のbrightnessが消失し,下垂体柄が腫大しています(左側)。ガドリニウムで腫瘍部分が増強されますが前葉よりは低信号となっています(右側)。経蝶形骨洞生検術で確定診断を得た後に,シスプラチンとエトポシドを1コース投与したところ腫瘍は完全消失しました。3コース後に24Gy12分割の放射線治療を加え再発はありません。残っていた下垂体前葉機能は治療後に少し改善しました。生検術では,トルコ鞍底を開けて下垂体後葉の下部を目標にして小さな組織採取をします。GHDがあっても前葉にはmassとしての腫瘍が無いと考えた方がいいでしょう。
bifocal tumor
松果体と神経下垂体同時発生
synchronous tumor, tandem lesion
- 同時といっても脳室上衣でつながっていますから,どちらかが浸潤病巣で組織環境的に増大しやすかったのかもしれません
- 組織型は,ほとんどがgerminomaです,極めて稀に奇形腫が混在します
- でも,HCGが極端に高ければ絨毛癌,AFPが極端に高ければ卵黄嚢種が混じっています
- bifocal tumor に,尿崩症で発症する,HCGβが5mIU/mlを超えない,AFPが正常範囲,奇形腫を示唆する画像所見がない,という項目を加えるとまず間違いなくgerminomaです
- ですからこの条件を満たせば生検手術は必要ないということになります
- もちろん,世の中には例外もありますが,生検術といっても全ての腫瘍部分を見るわけではないので,混合性胚細胞腫瘍の極めて低い可能性は,生検をしてもしなくても完全排除できないから同じなのです
- 鼻腔からのトルコ鞍内腫瘍の生検術は,30分くらいで済むし,なんの侵襲もないので,生検するという考えもあります(そうしています)
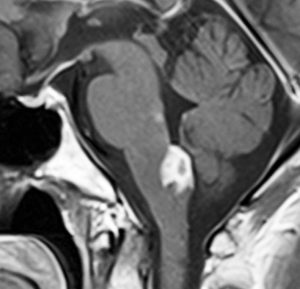
血清HCGが2.1mIU/ml,尿崩症で発症した思春期男児です。石灰化はありませんし,脂肪組織なども混在しません。生検術をしなくてもgerminomaと診断できます。でも簡単なので,経鼻的な生検術を行った方がいいです。
この例は18歳,HCG 0.1mIU/ml,尿崩症で発症しました。神経下垂体ジャーミノーマなので,下垂体前葉のみが残って後葉から視床下部が腫瘍化しています。よくよく見ると松果体にもごく小さな腫瘍があります。右のCISS画像で松果体の腫瘍化が明瞭です。
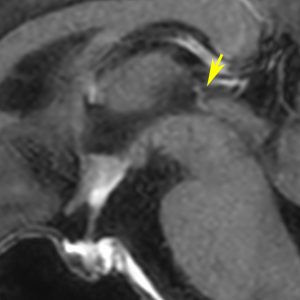
経鼻生検術で下垂体後葉部分がgerminomaということを確認してからICE (IFO/CDDP/VP-16)を1コース加えて3週間後の画像です。腫瘍は灰白隆起の部分を残してほぼ消失しています。松果体部の腫瘍も消えています。典型的なgerminomaの化学療法反応性を示しています。下垂体前葉機能は正常,尿崩症も少し良くなりました。
ジャーミノーマの内視鏡生検術のビデオ (endoscopic biopsy of germinoma) ここをクリックすると動画が見えます(3分46秒)
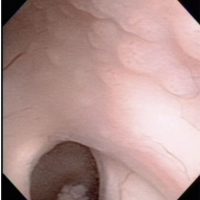
Peroperative view during endoscopic surgery in a boy with neurohypophyseal and pineal germinoma. There are numerous tiny nodules on the wall of right lateral ventricle.
These lesions are neither tumor CSF seeding nor dissemination. Germinoma cells always invades into subependymal glial tissue and spread to the whole ventricular system including the ovex. This has been called as subependymal infiltration (extension) of germinoma. Third ventriculostomy at the tuber cinereum in front of the mammillary bodies and tumor biopsy at the pineal lesion were shown.
ジャーミノーマに生検術をしないという選択肢はあるか?
答え:あります
軽度の複視のみで発症した20代前半男性です。右上のように松果体腫瘍の前に割れ目が入るように第3脳室があり,両側視床に浸潤するために軽度の視床浮腫があり,ガドリニウムで強く増強され一部にのう胞があります。これだけでもgeriminomaにかなり特有の所見です。さらに,灰白隆起(矢印)のところに小さな神経下垂体germinoma腫瘍があります (bifocal tumor)。HCGは測定限界以下,AFP 2.5で,水頭症はありません。全ての臨床所見がgerminomaであることを示しています。
生検病理診断をしないでICE化学療法を1コース終えた後の画像です。腫瘍は消失しています。これでgerminomaであることが確認できたので,ICE化学療法を2コース追加して,25.2グレイの全脳室照射をして治療を終了しました。
大脳基底核ジャーミノーマ
- むずかしいジャーミノーマです
- 男児に多いです
- 症状がわかりにくいのが特長です
- ゆっくり(数ヶ月から2年くらい)片方の手足の動きが悪くなる(緩徐進行性片麻痺)
- ゆっくり性格変化が生じるため,特に多動症,自閉症,AD/HD,注意欠陥障害と診断を受ける子どもたちは多いです
- MRIで脳腫瘍らしく見えないと言われます
- 視床下部下垂体に隠れたジャーミノーマ occult germinoma を合併することがあります
- 視床下部下垂体に隠れたジャーミノーマがある場合には,低身長や尿崩症で発症してから,数年かかって麻痺や注意欠陥障害などで発症します
MRIの特徴は2つのタイプがあります
1. 大脳基底核に腫瘍としての塊を作って大きくなるもの
- はっきりした腫瘍があり,ガドリニウム増強されます
- 大きさの割にmass effectが少ないかもしれません
- 腫瘍周囲浮腫も見られます
- 悪性神経膠腫(退形成性乏突起膠腫や膠芽腫)のように見えます
2. 腫瘍が隠れてしまってほとんど見えないもの
オカルト・タイプ occult type
- お化けのような腫瘍で見えません
- 神経下垂体ジャーミノーマでもオカルト・タイプはありますので同じようなものです
- 1980年代では,原因不明の大脳半球萎縮はジャーミノーマであると言われていました
- 片側の大脳基底核を中心に脳萎縮だけがみえるというものです
- 現在はそこまで進行する例がなく,半球萎縮に至る前に発見されます
- MRIでよく見えない,はっきりしない,と言われるのが逆に特長とも言えます
- レンズ核,内包あたりに,T2/FLAIRでボッとした影がみえます
- ガドリニウム増強されません
10代の男児で,非常にゆっくり1年くらいかけて左片麻痺が進行しました,痙性片麻痺です。落ち着きのない性格でもありました。血清HCG-beta 0.1で陽性でした。この病変は内包後脚の小さなものですから,定位生検術でさえもリスクが高いので行いません。出血のリスクというわけではなく,組織採取で内包高脚のcompactな白質を損傷して症状を悪くするからです。ご両親とよく話し合って病理診断なしで治療を開始します。ICE化学療法4コースと全脳照射25.2Gy/14fr で治療しました。ICE化学療法開始後からは片麻痺の悪化傾向が停止して,症状が改善傾向に向かいました。やがて,走れるようにもなりました。
意外に危ない生検術
澤村自身の経験です,定位脳手術で大脳基底核ジャーミノーマを生検して,2例で脳出血を生じました,1例では左の大脳基底核出血で開頭手術を要し,失語と片麻痺を生じました(でも今は元気ですけど)。その後,学会などでいろいろな脳外科医に聞いて回ったのですが,大脳基底核ジャーミノーマの生検術で脳出血を経験した脳外科医は多数いました。この情報は,おそらく学会発表や論文に現れることはないと考えますので,参考にしてください。
PET検査
- MRIでみえないような大脳基底核ジャーミノーマが Met-PET メチオニンペットで取り込みがみられることがあります
- 病変の中心部だけがわずかにMet uptakeが上昇して,ぼーっと光ったような画像になります
- 重要な補助診断となります
Sudo A1, Shiga T, Okajima M, Takano K, Terae S, Sawamura Y, Ohnishi A, Nagashima K, Saitoh S: High uptake on 11C-methionine positron emission tomographic scan of basal ganglia germinoma with cerebral hemiatrophy. AJNR Am J Neuroradiol 24:1909-1911, 2003
病状の進行
大脳基底核ジャーミノーマは,性格変化(多動症,学習障害,自閉症)で発症するとかなり悪化するまで気づかれません。片麻痺で発症してもそうです。症状が進行しすぎると治療しても元に戻りません。精神症状も片麻痺も残ったままで,精神身体の障害児として生き残っていかなければなりません。ですから,病理確定診断ができない場合でも治療を開始しなければなりません。
治療の順序
- 治療の考え方は,一般的なジャーミノーマより治りにくいし再発例が多いということです
- 化学療法は,ICE (CDDP, VP-16, IFO)化学療法を4コースします
- 化学療法を終えてから全脳照射をします
大脳基底核ジャーミノーマの放射線治療
- ジャーミノーマは,標準的な全脳室照射 whole ventricle irradiation WVIではカバーし切れません
- 大脳基底核ジャーミノーマは初発時と反対側の脳に再発することがあります
- ですから下垂体を含めた全脳照射 whole brain irradiation WBIになります
- 線量は25.2グレイを14分割なら確実でしょう
- 7歳以下の小さい子には認知機能を守るために23.4グレイ13分割も選択肢です
悪性神経膠腫と間違えそうなジャーミノーマ
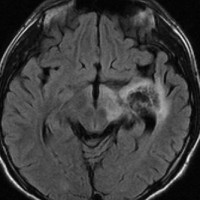
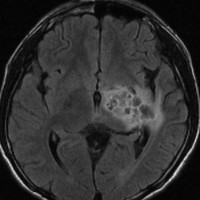
14歳で右の片麻痺と学力の低下で発症しました。ガドリニウム造影がまだらで最初は膠芽腫かな?と思いましたが,mass effectが軽いことが解ります。geminomaとしては珍しいのですがperifocal edemaがあります。
定位生検術で病理組織診断をして化学療法を加えた後の画像です。germinomaのお約束どおり,化学療法できれいに消失します。ちょっとした小さな増強される部分が残るのですがこれはstromal reaction (gliofibrosis)をみているので,残存腫瘍ではありません。余分な追加の放射線治療をしないように気をつけます。
局所照射で再発して再照射した例:左大脳基底核ジャーミノーマ
9歳で知的機能の低下と徐々に進行する右片麻痺,失語症で発症しました。MRIでは左大脳半球萎縮の所見だけで,11歳まで診断がつかずに来院しました。当時の方針で化学療法と左大脳基底核に局所放射線治療24グレイがなされましたが,4年後に左側頭葉に再発して化学療法と脳脊髄照射24グレイの再照射を行なった例です。
再発治療から17年後のMRIです。左大脳基底核の萎縮と高度の全脳萎縮が認められほぼ寝たきりの生活です。この例では,初発時に腫瘍塊形成がなく診断が遅れたこと,初回治療で腫瘍のある部位とその周辺だけの局所照射が用いられたことが誤りでした。
正確な早期診断と初回治療での全脳低線量照射をしていれば,良い状態で治癒したものでしょう。

ジャーミノーマ(胚腫)の病理
(ここをクリックするともっとたくさん見えます)
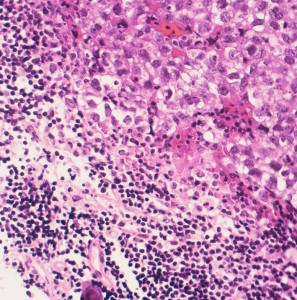
病理診断は困難ではありません。左側の写真のように,多くの場合にHE染色でtwo-cell patternと呼ばれる, 大型の腫瘍細胞と小型のリンパ球浸潤の特徴的な病理像で診断がつきます。大型の腫瘍細胞は楕円形の大きな核に大きな核小体が特徴です。
ジャーミノーマ(胚腫)の治療の歴史
1990年代までgerminomaに対しては,拡大局所,全脳室あるいは全脳脊髄を含む広範囲な領域に,45~55Gyほどの高線量を用いる放射線治療が行われました。10年生存割合は90%程度と満足すべき結果は得られていましたが,長期生存例において,精神発達遅滞,認知機能(知能)低下,間脳下垂体機能低下,放射線誘発二次腫瘍,脳主幹動脈閉塞などの遅発性放射線障害の発生が問題となりました。これらは治療後20年を経てから生じることもあるのです。 1990年初頭までの私の経験では,放射線治療を受けた長期生存85症例(観察期間中央値88ヵ月)のうち,58名が下垂体ホルモンの補充を受けており,26名が日常生活に支援を要し,結婚をして子供を設けることのできたのはただ1名のみでした (Sawamura Y, et al. Eur J Cancer: 1998)。
germinomaの長期生存者で,自立してまともな社会生活を送れている患者さんがほんとうに少ないことをこの時期に痛感しました。
そのため1990年代半ばからは,治療後の患児の生存の質を向上させるために,化学療法を併用して照射線量を減少せしめる努力を行いました。germinomaは,CARE, EP, ICE化学療法などへの感受性が非常に高く,組織診断確定後に化学療法を行えば,大きなものであっても腫瘍は例外なくほぼ完全にMRI画像上で消失します (Sawamura Y, et al. J Neurosurg: 1997, 1998)。 化学療法を始める時点で,水頭症を管理するための脳室ドレナージを留置すれば1週間程度で水頭症は改善するので,V-Pシャント術やリスクを侵してまでの第3脳室開窓術の必用はありません。
2000年頃の例です。閉塞性水頭症を併発する松果体部germinoma:左のMRIは発症時のものです。定位的生検術で確定診断して脳室ドレナージを留置しました。1コースのICE化学療法直後,生検術から6日目のMRI(中央)では腫瘍はほぼ消失し,水頭症は改善したのでドレナージを抜去しました。4コースの化学療法後(右側)に24Gyの全脳室照射を加えました。
化学療法単独治療では再発がかなり高頻度 (40%以上) に生じるので,最低でも23~25Gy程度の低線量放射線照射を加えることが必須となります。
1992年からは,化学療法を行なった後に24Gy/12分割の腫瘍拡大局所に対する放射線治療を用いていましたが,40例を治療した時点で20%程の再発に遭遇しました。再発例の分析では,照射野が狭かったため照射野外再発を招いたことが明らかとなり,1998年からは全脳室領域(25.2Gy/14分割)に照射野を拡大しました。また,とても稀なのですが診断時より髄腔内播種を呈する症例では同じ線量での全脳脊髄照射を,大脳基底核germinomaでは全脳照射を用いました。この治療法を開始してからは,「再発という懸念がほとんどない」と患者さんに説明できるくらいに治療成績は向上しました。
2022年基本的に,ICE化学療法3コースで腫瘍がほぼ消失したことを確認してから,全脳室 25.2Gy/14分割,8歳以下の低年齢層には23.4Gy/13分割を使用しています。でも23.4Gyでの多数例の経験はありません。
germinomaの生存割合
古いデータです,日本脳腫瘍統計に1991年から1996年の間に登録されたgerminoma458症例の累積生存曲線で,10年生存割合はさらに低下して行きます。
完全治癒が期待できる小児悪性脳腫瘍の代表格とされます。しかしながら,腫瘍が治癒しても後遺症を残さず社会復帰できる患児は現実には多くはありません 。迅速な診断と最低侵襲度かつ必用十分な治療によって,神経脱落症状や下垂体機能不全の進行を少しでもくい止めることが求められます。また,上記の生存割合曲線は登録され長期追跡されたものであるので,登録されない例や追跡がされてない例を鑑みれば実際の10年生存割合はこれより確実に低いのでしょうし,また再発割合はかなり高いものと推定されます。2000年以降の診断と治療技術の進歩を考えあわせても10年生存割合はおそらく90%ほどであろうと考えています。もちろん正確なデータはどこにもありません。それを得るには臨床試験を開始してから15年という歳月を要するからです。日本においての2021年時点で治療されるgerminomaの推定5年全生存割合は95%程度でしょう。
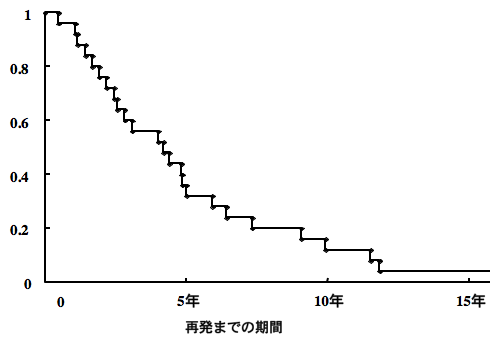
再発までの期間と経過観察の必要性
再発はどのくらいの期間で生じるか,という問いに明確な解答はありません。でも,多くの場合は5年以内と考えてよいです。しかしながら,以下のグラフに示すように,澤村が経験した25例の再発germinomaの初期治療から再発までの期間をみると,3割程度の再発は5年以降に生じていました。初期治療から10年以上たってからの再発例もあります。germinomaの治療後の外来経過観察は,2次腫瘍の発生への警戒も含めて10年以上を要することが明らかです。
ジャーミノーマの豆知識(生検術のあれこれ)
生検術の前にCT scan や脳血管撮影 DSA をしてはいけません。わずかな放射線被曝で,腫瘍細胞が消失してしまってリンパ球浸潤のみの病理所見となりbiopsy failureになる可能性があります。下垂体内の小さなジャーミノーマだとCT撮影1回だけでも消失してしまうことがあります。結果的に生検術が無駄になるということです。大きなジャーミノーマでも,治療開始前にMRI上で縮小してビックリすることがあります。
術前CTで小さくなって生検術が不成功になったジャーミノーマ
- ジャーミノーマは,放射線感受性が極めて高い腫瘍です
- ほんの少しのX線被曝で小さくなったり消えてしまったりします
- 18グレイくらいの局所放射線だけで消失して完全治癒した例なども知られています
- CT検査だけで消失することがあります
- もちろんカテーテルを用いる血管撮影 DSAでも消えることがあります
- ですから,ジャーミノーマを疑った場合にはX線を用いる検査を行いません
下にお見せするのは実例です。11歳で尿崩症で発症,初潮が発来せず,18歳で低身長を指摘され下垂体機能不全とMRIにてLCHを疑われました。HCGは測定限界値以下で経過しました。
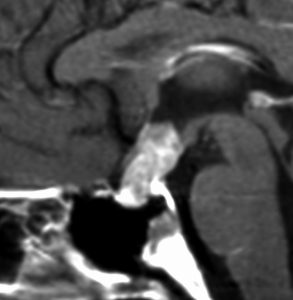 左側のMRIは21歳時のものです。発症後10年が経過していました。
左側のMRIは21歳時のものです。発症後10年が経過していました。
腫瘍性病変が増大したために,経蝶形骨洞手術 TSS で生検術を計画しました。経鼻手術でしたので,受け持ちの若い先生が,入院後に3Dやらthin sliceやら濃厚なCT検査を2度行いました。
予定どおり生検したのですが,大学病院病理部から帰ってきた返事は「免疫染色を含めて腫瘍細胞はなく,小型リンパ球を中心とした多彩な炎症細胞浸潤を認めることからlymphocytic hypophysitisの可能性は考えられます」という返事でした。
私は,生検術が終わってから初めて,手術前にCT検査が繰り返されたことを知りました。
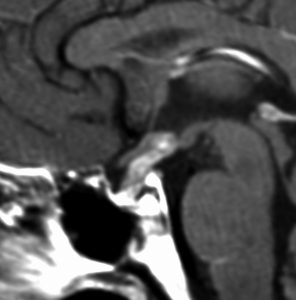
「生検」術直後のMRIです。腫瘍がかなり縮小しています。手術ではトルコ鞍底部の腫瘍をごくわずかに摘出しただけなので,手術前の頭蓋CT,胸部写真などのX線被曝によって腫瘍細胞が消失してしまったと考えられます。
また経過観察を続けました。患者さんは部分的汎下垂体機能低下症があったもののホルモン補充で元気に暮らしていました。
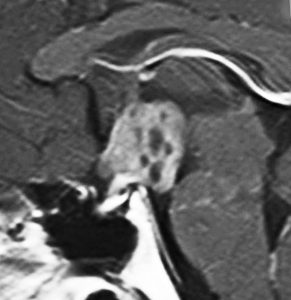
その2年後24歳の時のMRIです。発症後13年。
トルコ鞍内部の腫瘍はほぼ消失してしまって,視床下部から第3脳室に急激に腫瘍増大しました。仕方がないので,開頭手術ですぐに生検術をしました。
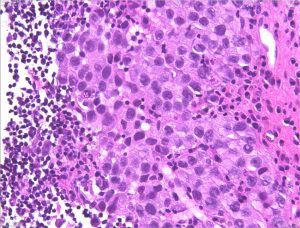
病理所見です。典型的な germinoma でした。治療は,ICE (IFO/CDDP/VP-16)化学療法を3コースの後で全脳室照射 25.2Gy/14分割を加えました。治療後8年ほど経ちますが,幸い患者さんは元気でごく普通の社会生活ができています。
神経下垂体ジャーミノーマ neurohypophyseal germinoma
神経下垂体ジャーミノーマ neurohypophyseal germinoma : 神経下垂体から発生します。大きな腫瘍は経蝶形骨洞手術 transsphenoidal surgeryで生検することになんら問題も難点もありません。一方,かなり小さなものであってもtranssphenoidal surgeryによる生検が適切です。後葉が腫瘍化するのでトルコ鞍底面を開けて鞍背の方向へ向かって生検術を行います。非常に小さな腫瘍片しか採取できないので,バイオプシー鉗子は細く鋭いものがないとこの手術はできません。病歴の長いジャーミノーマは線維結合組織を含んで非常に硬いことがあるので,そんな時は引っぱってちぎることができないためにハサミで切り取ります。
下垂体柄のみが腫れているような一見トルコ鞍内に腫瘍がないようなジャーミノーマでも後葉内に腫瘍は見つかるし証明できます。理由は,ジャーミノーマが発生すると下垂体組織は侵されて萎縮し,その容積分の腫瘍が下垂体内に存在するからで,治療を終えれば下垂体の委縮像が観察できます。LCHとの鑑別のために,開頭術で下垂体柄を部分的に切り取るような生検術を行えば,下垂体機能を低下させる可能性が大きいが大きいので行いません。また開頭術で,鞍隔膜を切開して前葉を損傷しないで後葉部分のジャーミノーマ組織を摘出するというとはできません。
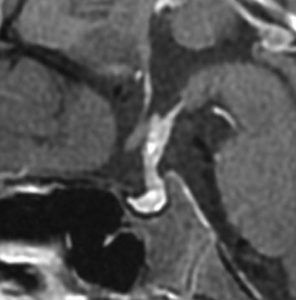
2000年に発症した女の子です,4歳の時に夜間の水分摂取と夜尿。5歳の時にさらに飲水量が増えて,1日排尿回数18回という症状がありました。6歳でようやく,尿崩症と低身長 105cm (-1.47SD)と診断され,MRIで下垂体柄の腫大が発見されました。
低年齢だったのでCDDP/VP-16化学療法4コースと全脳室照射23.4Gy/13分割で治療しました。
治療後はGHDは改善して尿崩症だけ,20歳をすぎてとても元気に暮らしています。
LCHはhit-and-runで,一気に症状が悪くなります。また同じ神経下垂体に何度も病変は出ません。ゆっくり症状が進行するのがgerminomaです。
幼児期に低身長で発症する例がある(ここをクリックで見れます)
松果体ジャーミノーマ pineal germinoma
松果体実質から発生します。中脳水道閉塞による水頭症で発症することが多いので,近年では神経内視鏡による第3脳室開窓術と生検術が行われることが圧倒的に多いです。実例をビデオに提示するので参照してください (click here)。小さなものでは松果体部を内視鏡で観察しても変色した腫瘍らしきものが見えないことがあり,手綱交連と後交連の白質がみえpineal recessらしいところが見えるだけということもありますが,隆起の状態を観察して標本採取します。生検鉗子でジャーミノーマの組織片を採取するとわずかな出血が生じるのが常であるので,脳室内洗浄を十分できるようにしておきます。多くの場合は止血操作などせずとも自然に止血しますが,髄液が混濁して観察が困難にならないように注意しなければなりません。内視鏡観察下で,卵黄のう腫や絨毛上皮癌などの発達した腫瘍血管が見えるようならば,無理して生検を遂行しない方が良いでしょう。わずかでも腫瘍内の動静脈シャント (red veinsがある) を損傷すれば止血することができないからです。松果体腫瘍の生検術では学会発表では知ることができない多くの合併症が起こっているのも事実ですし,内視鏡手術の術前にも開頭よりリスクが低いとは説明しない方が良いでしょう。
大脳基底核ジャーミノーマ basal ganglia germinoma
大脳基底核おそらく視床下部から発生します。片麻痺,認知機能障害,性格変化・多動が数ヶ月から数年にわたって進行しても,MRIで腫瘍が捉えられないことがあります。CT/MRIガイド定位脳生検術が適切ですが,生検部での脳出血の合併症の可能性があります。生検時の脳出血のリスクは決して低い確率ではないし,大脳基底核出血のために高次脳機能障害を悪化させることがあるので,メチオニンペットでのuptakeが高いなどを傍証に画像診断のみで治療開始することもしばしばです。
大脳基底核ジャーミノーマの症例(ここをクリック)
進行して播種を伴ったジャーミノーマ advanced case(ここをクリック)
前頭葉深部白質浸潤・脳室壁だけのジャーミノーマ(ここをクリック)
ジャーミノーマと間違えやすい下垂体後葉炎 neurophypophysitis
40代女性が多飲多尿で発症しました。下垂体と下垂体柄の腫大がみられます。ジャーミノーマとの違いは,ガドリニウム増強が均一で,下垂体後葉全体が前葉と同程度まで増強されることです。もちろん年齢も違いますが,lymphocytic neurohypophysitisは若年女性に好発するので,10−20代だと鑑別が難しいでしょう。この患者さんは生検後にステロイド治療を行って軽度の尿崩症を残したのみです。無治療でも自然寛解することがあります。
ジャーミノーマと間違えやすい下垂体後葉炎 neurophypophysitis
18歳男性が急に多飲になりました,かなり高度の尿崩症でした。発症後2ヶ月のMRIです。左側のT1強調画像では下垂体後葉の高信号(抗利尿ホルモン)が消失しています。右側のガドリニウム増強では下垂体柄が太くなっていて下垂体全体が増強され,松果体にのう胞がみられます。腫瘍マーカーは陰性。ジャーミノーマを疑い経鼻生検術を行いました。
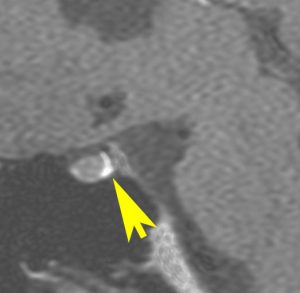 病理診断の結果は,リンパ球,形質細胞浸潤と肉芽腫瘍組織があるのみでした。慢性下垂体炎の所見です。内分泌内科でプレドニゾロン投与が行われました。
病理診断の結果は,リンパ球,形質細胞浸潤と肉芽腫瘍組織があるのみでした。慢性下垂体炎の所見です。内分泌内科でプレドニゾロン投与が行われました。
尿崩症は少し改善して,治療後4年のMRIでは下垂体後葉に高信号が認められています。松果体のう胞はそのままです。
この例は,胚細胞腫瘍と臨床的には区別できません。尿崩症の発症機転が急激だったのが唯一の下垂体炎の特徴でした。生検術が唯一の鑑別方法です。
巨大な前頭底部ジャーミノーマ
少年のものです。数年の経過のゆっくりした認知機能低下で発症しました。学業が不振でしたが気づかれず増大したものです。初診時には,認知機能障害,尿崩症,汎下垂体機能低下症,高度の両側視力低下でした。こんなものでもICE化学療法1コースでほとんど消失します(右側の画像は2コース後かつ放射線治療前のMRI)。ですから,無理して開頭摘出術をしない。
germinomaの視床浸潤:ミッキーマウスの耳

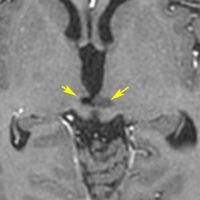 松果体ジャーミノーマは両側視床に浸潤して視床浮腫を生じます。真ん中に第3脳室後半部の割れ目が残っているのが特徴的な所見です。ミッキーマウスの耳みたいになります。かなり特異的な所見であり診断に有用です。右下は治療後です。
松果体ジャーミノーマは両側視床に浸潤して視床浮腫を生じます。真ん中に第3脳室後半部の割れ目が残っているのが特徴的な所見です。ミッキーマウスの耳みたいになります。かなり特異的な所見であり診断に有用です。右下は治療後です。
germinomaの再発の不思議
1996年,18歳男性が尿崩症で発症しました(左MRI)。bifocal tumorで,松果体腫瘍だけを摘出して予想どおりgerminomaの病理診断でした。ICE化学療法4コース行って,tumor bedに24Gy/12frの拡大局所放射線治療をしました。当時は全脳室照射を行っていなかった時期です。10年後の2006年にHCGがわずかに上昇し,脳梁膝部内部に再発を生じました。照射野外再発です。開頭手術で全摘出したら硬い腫瘍で,成熟奇形腫とgerminomaの混合性胚細胞腫瘍となっていました。その後に,CARE 3コースと脳脊髄照射19.2Gy/12frと局所5.4Gy/1frの照射を加えました。その後,17年再発なく社会人として結婚,お子さんがいて普通に暮らしています。
この例が,metachronous germ cell tumorであったのかどうかは不明です。germinomaは少なくとも10年以上の経過観察が必要だということを示しています。
ジャーミノーマの尿崩症は治療で治るのか?
14歳くらいからトイレの回数が増え,中学生の時に夜尿をするようになりました。生理がないので婦人科を受診しました。子宮と膣の発達も悪く,原発性低ゴナドトロピン性無月経と診断されてMRIをして発見されました。重症GHDがありましたがそれほど低身長ではなく,骨端線未閉鎖でした。私のところを受診したのが19歳でした。病歴からは,5年の経過でかなりゆっくり下垂体不全が進行したということがわかります。視床下部に中心があり下垂体柄も侵すジャーミノーマですが,下垂体は著しく萎縮しています。
開頭手術による生検術を選択して病理診断を確定しました。術後にICE化学療法3コースと全脳室照射25.2グレイ14分割で治療しました。その後,無事に大学を卒業して社会人として働いています。驚くことに,抗利尿ホルモン(デスモプレッシン)を使用していません。GHDはやや改善して無症状,副腎皮質ホルモンと甲状腺ホルモンの補充は不要です。治療後6年で,女性ホルモン補充のみで生活できています。ジャーミノーマでは治療で間脳下垂体機能が改善することがあります。
ジャーミノーマとリンパ球浸潤:免疫機能の役割
Occult neurohypophyseal germinomas in patients presenting with central diabetes insipidus. Neurosurg Focus 1998
Sudo A, Sawamura Y: High uptake on 11C-methionine positron emission tomographic scan of basal ganglia germinoma with cerebral hemiatrophy. AJNR 2003
Liu B: PD-1/PD-L1 expression in a series of intracranial germinoma and its association with Foxp3+ and CD8+ infiltrating lymphocytes. PLoS One 2018
- germinomaはとても低い線量のX線検査だけで消失してしまうことがあります
- その後,随分経ってから再発したり,治ったりという報告もあります
- germinomaの組織のなかにはたくさんのリンパ球が浸潤しています
- germinomaは,MIB-1染色で高い腫瘍細胞分裂能と増殖能を示します
- でもそれほど早く腫瘍が大きくなることがありません
- ここには大きな病理学的な矛盾があります
- 慢性炎症性組織が腫瘍内に生じたり,lymphocytic germinal centerが見られることがあります
- 尿崩症や低身長で発症してから,数年間は腫瘍がMRIでみえないこともあります,occult germinomaといいます
- 大脳基底核germinomaも,認知機能低下や麻痺が進行しつつも腫瘍塊が顕在化しないことはしばしばです
- これらを総合的に考えると,患者さん自身の免疫機能がgerminomaの増大を抑制している可能性が強く示唆されます
- 1989年に澤村はこのリンパ球を分離して,腫瘍内浸潤T細胞が腫瘍細胞障害活性を持つことを論文にしたことがあります
- germinoma細胞は高いレベルのPD-L1を発現しています,一方で浸潤リンパ球はPD-1発現がみられます
- これらは,getminomaが増大する時には,リンパ球の細胞免疫反応を抑制できることを示唆しています
文献情報
Phase II trial of response-based radiation therapy for patients with localized germinoma: a Children’s Oncology Group study. Neuro Oncol 2022
PFS3年をみた第2相試験です。カルボプラチンとエトポシドでCRとなれば,全脳室18グレイと腫瘍床に12グレイのboost照射が加えられました。PRの場合は24グレイの全脳室照射と12グレイのboostが用いられました。90例の評価可能な患者さんのうち74例(82%)が18グレイの全脳室照射を受けていました。18グレイの群で3年PFSは94.5%,24グレイの群で93.75%でした。24グレイの群でattention scoreが治療後9ヶ月くらいで生じたようです。noninferiority of the 18 Gy WVIとしては明らかに有意な結果はでませんでした。
「解説」3年のうちに5%くらいの再発が認められたということです。ジャーミノーマの再発は3年以降もとても多いです,ですからもっとPFSの数値は年ごとに低下するでしょう。また,もし神経下垂体に腫瘍があると,視床下部と下垂体が最低でも30グレイ被曝する放射線治療を用いています。意外に悪い成績であるという印象を受けます。もし全脳室照射を18グレイまで低下させるならば,カルボプラチンとエトポシドという併用化学療法の強度が不足しているような気がします。
尿崩症があり松果体と神経下垂体に腫瘍があれば全てがジャーミノーマか?
結論はそれでよいようです
Kanamori M: So-called bifocal tumors with diabetes insipidus and negative tumor markers: are they all germinoma? Neuro Oncol 2021
松果体と神経下垂体の両方に腫瘍が同時に発生するものをbifocal tumorsと呼びます,あるいはsynchronous tumorsとも言います。従来から頭蓋内胚細胞腫瘍特有の画像所見と言われて来ました。この2箇所発生の腫瘍が,尿崩症で発症して腫瘍マーカーもはっきり上昇していない場合,全てgerminomaと言ってよいかどうかが検討されました。132例があてはまり,その内の91例で組織採取がされました。逆に,41例 (31%)では組織採取なしに治療がされたことになります。89例で組織診断がなされ,82例 (92%)がgerminomaでした。成熟奇形腫が2例と炎症が2例認められています。3例でgerminoma以外の胚細胞腫瘍の診断がついています。炎症というのはgranulomatous inflammationであり,CTや血管造影検査をした後でgerminomaを生検した場合によく認められる組織所見です。
「解説』ほぼ全てgermionomaということになります。混在しているものが成熟奇形腫であれば,germinomaに準じた治療をして,その後に残った成熟奇形腫を摘出するしか完治の方法はありません。ですから,すべてgerminomaとして初期治療を開始しても誤りはないということになります。対象から外れる組織診断されなかった41例もgerminomaとして治療されていたのでしょう。成熟奇形腫が混じっていれば,生検術前のMRIとCTでたいていの場合は予測できるものですから,さらに生検術の意義は低くなります。あえて結論で,筆者は生検術を行うべきだと主張していますが,その根拠を導き出すデータとは真逆の結果です。澤村は,経蝶形骨洞手術で生検を行います。
ジャーミノーマの水頭症に対してはあえてリルクを伴う第3脳室開窓術後行う必要がなく外ドレナージですむ例がある
RonslyR: Successful management of symptomatic hydrocephalus using a temporary external ventricular drain with or without endoscopic third ventriculostomy in pediatric patients with germinoma. J Neurusurg 2021
22人のジャーミノーマの患者さんで,外ドレナージ EVD 5, ETV 5, EDV/ETV 7例で,残りの5例は水頭症に対する外科的処置はなされませんでした。カルボプラチンとエトポシドの化学療法が行われ,平均7日間でガイドレナージは抜去されました。最終的に12例中の2例でVPシャンとが必要となりました。10年の追跡期間でPFSは96%でした。結論として,シャントが必要となる患者であっても,FTVとEVDで管理できるであろうと結論しています。
長期生存者で脳血管障害と2次腫瘍が多い
Acharya S et al.: Long-term outcomes and late effects for childhood and young adulthood intracranial germinomas. Neuro Oncol 2014 [Epub]
ジャーミノーマの治療を受け5年以上生存した405人の患者さんの統計データです。20年全生存割合が84%で,30年生存が62%でした。正常人と比較すると脳血管障害による死亡リスクが59倍であり,25年の時点ではガンと2次腫瘍による死亡は16%と6%に達したそうです。
「解説」2008年に,全く同じ命題に関して広島大学杉山一彦先生と一緒に調査したことがあります。 長期生存した203人の患者さんで追跡期間中央値12.5年という詳細な検討をしました。2次腫瘍が22人 (11%)で,脳血管障害が14人 (7%)で発生していました。発症年齢中央値は27.1歳でした。2次腫瘍の中では膠芽腫が5人も発生していて,血管障害はウィリス動脈輪狭窄症が多いものでした。これらが生じた患者さんへの放射線量を調べたところ,32人の患者さんの内,30人で40グレイ以上の線量が用いられていました。40グレイ以下の線量ではこれらの遅発性障害がほとんど発生しないとも言えます。
このような調査は20年あるいは30年前に行われた治療の長期成績をみているものです。現在では30グレイ以上の線量はジャーミノーマの治療に使用されないので,過去のデータとして意味があるものかどうかは解りません。2014年にNeuro Oncologyという権威の高い雑誌に発表されたのでこのまま引用されるのかもしれませんが,注意が必要です。
文献
- Acharya S et al.: Long-term outcomes and late effects for childhood and young adulthood intracranial germinomas. Neuro Oncol 2014 [Epub]
- Aoyama H, Shirato H, Ikeda J, Fujieda K, Miyasaka K, Sawamura Y: Induction chemotherapy followed by low-dose involved-field radiotherapy for intracranial germ cell tumors. J Clin Oncol 20: 857-865 2002
- Balmaceda C, Heller G, Rosenblum M, Diez B, Villablanca JG, Kellie S, Maher P, Vlamis V, Walker RW, Leibel S, Finlay JL: Chemotherapy without irradiation – a novel approach for newly diagnosed cns germ cell tumors – results of an international cooperative trial. J Clin Oncol 14: 2908-2915, 1996
- Balmaceda C, Modak S, Finlay J: Chemotherapy for the central nervous system germ cell tumors. (in) Intracranial Germ Cell Tumors. Sawamura Y, Shirato H, de Tribolet N (eds), Springer-Verlag, Wien, 1998, pp243-281
- Bamberg M, Kortmann RD, Calaminus G, Becker G, Meisner C, Harms D, Gobel U: Radiation therapy for intracranial germinoma: Results of the German cooperative prospective trials MAKEI 83/86/89. J Clin Oncol 17: 2585-2592, 1999
- Phase II trial of response-based radiation therapy for patients with localized germinoma: a Children’s Oncology Group study. Neuro Oncol 2022
- Brain Tumor Registry of Japan (1969-1996), 11th edition, Neurol Med Chirur 43: 1-49, 2003 (Suppl)
- Calaminus G, Andreussi L, Garre ML, Kortmann RD, Schober R, Gobel U: Secreting germ cell tumors of the central nervous system (CNS). First results of the cooperative German/Italian pilot study (CNS sGCT). Klin Padiatr 209:222-227, 1997
- Calaminus G, et al.: SIOP CNS GCT 96: final report of outcome of a prospective, multinational nonrandomized trial for children and adults with intracranial germinoma, comparing craniospinal irradiation alone with chemotherapy followed by focal primary site irradiation for patients with localized disease. Neuro Oncol. Mar 3. [Epub], 2013
- Chen LP, Cai SM, Fan JX, Li ZT: PEBA regimen (cisplatin, etoposide, bleomycin, and adriamycin) in the treatment of drug-resistant choriocarcinoma. Gynecol Oncol 56: 231-234, 1995
- Cho DY, Wang YC, Ho WL: Primary Intrasellar Mixed Germ-Cell Tumor With Precocious Puberty And Diabetes Insipidus. Child Nerv Syst 13:42-46, 1997
- de Wit R: Equivalence of three or four cycles of bleomycin, etoposide, and cisplatin chemotherapy and of a 3- or 5-day schedule in good-prognosis germ cell cancer: a randomized study of the European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group and the Medical Research Council. J Clin Oncol 19: 1629-1640, 2001
- de Wit R: Four cycles of BEP vs four cycles of VIP in patients with intermediate-prognosis metastatic testicular non-seminoma: a randomized study of the EORTC Genitourinary Tract Cancer Cooperative Group. European Organization for Research and Treatment of Cancer. Br J Cancer 78: 828-832, 1998
- Frappaz D: EANO, SNO and Euracan consensus review on the current management and future development of intracranial germ cell tumors in adolescents and young adults. Neuro Oncol 2021
- Freilich RJ, Thompson SJ, Walker RW, et al: Adenocarcinomatous transformation of intracranial germ cell tumors. Am J Surg Pathol 19: 537-544, 1995
- Furuhata S, Yamada F, Fukuda S, Otani M, Toya S: Mixed germ cell tumor of the basal ganglia: a case report. Surg Neurol 41:490-493, 1994
- Haddock MG, Schild SE, Scheithauer BW, Schomberg PJ: Radiation therapy for histologically confirmed primary central nervous system germinoma. Int J Rad Oncol Biol Phy 38: 915-923, 1997
- Hinton S: Cisplatin, etoposide and either bleomycin or ifosfamide in the treatment of disseminated germ cell tumors: final analysis of an intergroup trial. Cancer 97:1869-1875, 2003
- Hinton S: Phase II study of paclitaxel plus gemcitabine in refractory germ cell tumors (E9897): A trial of the eastern cooperative oncology group. J Clin Oncol 20:1859-1863, 2002
- Ikeda J, Sawamura Y, Tada M, Abe H: Metachronous neurohypohyseal germinoma occuring eight years after total resection of mature teratoma. Surg Neurol 49: 205-209, 1998
- Jennings MT, Gelman R, Hochberg F et al: Intracranial germ cell tumors. Natural history and pathogenesis. J Neurosurg 63: 155-167,1985
- Kanamori M: So-called bifocal tumors with diabetes insipidus and negative tumor markers: are they all germinoma? Neuro Oncol 2021
- Kamoshima Y, Sawamura Y, Ikeda J, Aoyama H, Shirato H: Late recurrence and salvage therapy of CNS germinomas. J Neurooncol. 2008 Jul 5
- Kamoshima Y, Sawamura Y: Update on current standard treatments in central nervous system germ cell tumors. Curr Opin Neurol 23: 571-575, 2010
- Kato T, Sawamura Y, Tada T, Murata J, Abe H, Shirato H, Fujieda K: Occult neurohypophyseal germinomas in patients presenting with central diabetes insipidus. Neurosurg Focus 5: 1-6, 1998
- Kawakami Y, Yamada O, Tabuchi K, Ohmoto T, Nishimoto A: Primary intracranial choriocarcinoma. J Neurosurg 53:369-374, 1980
- Kida Y, Kobayashi T, Yoshida J, Kato K, Kageyama N: Chemotherapy with cisplatin for AFP-secreting germ-cell tumors of the central nervous system. J Neurosurg. 65: 470-475, 1986
- Kochi M, Itoyama Y, Shiraishi S, Kitamura I, Marubayashi T, Ushio Y: Successful treatment of intracranial nongerminomatous malignant germ cell tumors by administering neoadjuvant chemotherapy and radiotherapy before excision of residual tumors. J Neurosurg 99: 106-114, 2003
- Koyama S, Tsubokawa T, Katayama Y, Hirota H: Choriocarcinoma of the septum pellucidum: case report. Surg Neurol 35:478-482, 1991
- Meagher-Villemure K: Pathology. Sawamura Y, Shirato H, de Tribolet N (eds), Springer-Verlag, Wien, 1998, pp. 17-36
- Matsutani M, Sano K, Takakura K, Fujimaki T, Nakamura O, Funata N, Seto T: Primary intracranial germ cell tumors – a clinical analysis of 153 histologically verified cases. J Neurosurg 86:446-455, 1997
- Merchant TE, Sherwood SH, Mulhern RK, Rose SR,- Thompson SJ, Sanford RA, Kun LE: CNS germinoma: Disease control and long-term functional outcome for 12 children treated with craniospinal irradiation. Int J Rad Oncol Biol Phys 46: 1171-1176, 2000
- Miyanohara O, Takeshima H, Kaji M, Hirano H, Sawamura Y, Kochi M, Kuratsu J: Diagnostic significance of soluble c-kit in the cerebrospinal fluid of patients with germ cell tumor. J Neurosurg 97: 177-183, 2002
- Murray MJ: Consensus on the management of intracranial germ-cell tumours. Lancet Oncol 2015
- Nichols CR, Catalano PJ, Crawford ED, Vogelzang NJ, Einhorn LH, Loehrer PJ: Randomized comparison of cisplatin and etoposide and either bleomycin or ifosfamide in treatment of advanced disseminated germ cell tumors: an Eastern Cooperative Oncology Group, Southwest Oncology Group, and Cancer and Leukemia Group B Study. J Clin Oncol 16: 1287-1293, 1998
- O’Callaghan AM, Katapodis O, Ellison DW, Theaker JM, Mead GM: The growing teratoma syndrome in a nongerminomatous germ cell tumor of the pineal gland: a case report and review. Cancer 80: 942-947, 1997
- Packer RJ, Sutton LN, Rorke LB, et al: Intracranial embryonal cell carcinoma. Cancer 54: 520-524, 1984
- Piamsomboon S, Kudelka AP, Termrungruanglert W, Vanbesien K, Edwards CL, Lifshitz S, Schomer DF, Champlin R, Mante RP, Kavanagh JJ, Verschraegen CF: Remission of refractory gestational trophoblastic disease in the brain with ifosfamide, carboplatin, and etoposide (ice) – first report and review of literature. Eur J Gynaecol Oncol 18:453-456, 1997
- Rogers SJ, Mosleh-Shirazi MA, Saran FH: Radiotherapy of localised intracranial germinoma: time to sever historical ties? Lncet Oncol 6:509-519, 2005
- Sawamura Y, Kato T, Ikeda J, Tada M, Shirato H: Teratomas of The Central Nervous System: Treatment Consideration Based on 34 Cases. J Neurosurg 89: 728-737, 1998
- Sawamura Y: Strategy of combined treatment of germ cell tumors, Pineal region tumors. Diagnosis and treatment options. Prog Neurol Surg 23: 86-95, 2009
- Sawamura Y: Current diagnosis and treatment of central nervous system germ cell tumours. Curr Opin Neurol 9 (6): 419-423, 1996
- Sawamura Y, Ikeda J, Shirato H, Tada M, Abe H: Germ Cell Tumors of The Central Nervous System: Treatment Consideration Based on 111 Cases and their Long-Term Clinical Outcomes. Eur J Cancer 34: 104-110, 1998
- Sawamura Y, Shirato H, de Tribolet N: Recent advances in the treatment of central nervous system germ cell tumors. Adv Tech Stand Neurosurg 25: 141-159, 1999
- Sawamura Y, de Tribolet N, Ishii N, Abe H: Surgical Management of Primary Intracranial Germinomas: Diagnostic Surgery or Radical Resection ? J Neurosurg 87: 262-266, 1997
- Sawamura Y: Overview for management. in Intracranial Germ Cell Tumors. Sawamura Y, Shirato H, de Tribolet N (eds), Springer-Verlag, Wien, 1998, pp169-191
- Sawamura Y: Prognosis of central nervous system germ cell tumors. in Intracranial Germ Cell Tumors. Sawamura Y, Shirato H, de Tribolet N (eds), Springer-Verlag, Wien, 1998, pp155-168
- Sawamura Y, Shirato H, Ikeda J, Tada M, Ishii M, Kato T, Abe H, Fujieda K: Induction Chemotherapy Followed by Reduced-Volume Irradiation for Newly Diagnosed CNS Germinoma. J Neurosurg 88: 66-72, 1998
- Sawamura Y, Ikeda J, Ishii N, Kato T, Tada T, Abe H, Shirato H: Combined irradiation and chemotherapy using ifosfamide, cisplatin, and etoposide for children with medulloblastoma/posterior fossa primitive neuroectodermal tumor. Neurol Med Chirur (Tokyo) 36: 632-638, 1996
- Schneider DT, Schuster AE, Fritsch MK, Calaminus G, Gobel U, Harms D, Lauer S, Olson T, Perlman EJ: Genetic analysis of mediastinal nonseminomatous germ cell tumors in children and adolescents. Genes Chromosomes Cancer 34: 115-25, 2002
- Schechter NR, Mychalczak B, Jones W, Spriggs D: Prognosis of patients treated with whole-brain radiation therapy for metastatic gestational trophoblastic disease Gynecologic Oncology 168:183-192, 1998
- Shirato H, Nishio M, Sawamura Y, Myohjin M, Kitahara T, Nishioka T, Mizutani Y, Abe H, Miyasaka K: Analysis of long-term treatment of intracranial germinoma. Int J Radiation Oncology Biol Phys 37:511-515, 1997
- Sievers EL, Berger M, Geyer JR: Long-term survival of a patient with primary sellar choriocarcinoma with pulmonary metastases – a case report, Med Pediat Oncol 26:293-295, 1996
- Sudo A, Shiga T, Okajima M, Takano K, Terae S, Sawamura Y, Ohnishi A, Nagashima K, Saitoh S. Links: High Uptake on (11)C-methionine Positron Emission Tomographic Scan of Basal Ganglia Germinoma with Cerebral Hemiatrophy. AJNR Am J Neuroradiol. 24: 1909-1911, 2003
- Tapper D, Lack EE: Teratomas in infancy and childhood. Ann Surg 198: 398-410, 1983
- Ushio Y, Kochi M, Kuratsu J, Itoyama Y,- Marubayashi T: Preliminary observations for a new treatment in children with primary intracranial yolk sac tumor or embryonal carcinoma. Report of five cases. J Neurosurg 90:133-137, 1999
- Yamaguchi S: Long-term consequences of residual lesions after chemoradiotherapy in patients with germinoma at onset. J Neurusurug Pediatr 2022
- Yoshida J, Sugita K, Kobayashi T, Takakura K, Shitara N, Matsutani M, Tanaka R,Nagai H, Yamada H, Yamashita J: Prognosis of intracranial germ cell tumours: effectiveness of chemotherapy with cisplatin and etoposide (CDDP and VP-16) Acta Neurochir (Wien) 120: 111-117, 1993
- Yoshida K, Sawamura Y: Clinical Findings and Diagnosis, Ophthalmological manifestations. Sawamura Y, Shirato H, de Tribolet N (eds), Springer-Verlag, Wien, 1998, pp137-145