遺伝性白質疾患ガイドライン
CQ 3-8. Pol III関連白質ジストロフィー(小脳萎縮と脳梁低形成を伴うび漫性大脳白質形成不全症・失調、歯牙低形成を伴う髄鞘形成不全症)
- Pol III-related leukodystrophies (HDL7, OMIM#607694, HDL8, OMIM#614381, HDL11, OMIM#616494) (Hypomyelination, hypodontia, hypogonadotropic hypogonadism (4H) syndrome, Ataxia, delayed dentition, and hypomyelination [ADDH], Tremor-ataxia with central hypomyelination [TACH], Leukodystrophy with oligodontia [LO], Hypomyelination with cerebellar atrophy and hypoplasia of the corpus callosum [HCAHC])
Pol III関連白質ジストロフィーは、POLR3A, POLR3B, POLR1C遺伝子異常による常染色体劣性遺伝疾患である。臨床的には、痙性あるいは小脳失調による進行性歩行異常、振戦を基本症状として示し、さらに異常な歯牙(歯が少ない、萌出の遅れ、歯列異常)や下垂体性の性腺機能低下症(性成熟の遅延/欠損)などを呈する。MRIで白質低形成(hypomyelination)に加えて小脳萎縮と脳梁低形成を呈する。
現時点では対症的な治療が行われる。
疾患概念
頭部MRIで全般的な大脳白質低形成を認めても特異的診断名をつけることが困難なことがしばしばある。これらの中で、小脳萎縮と脳梁低形成の組み合わせをもつ一群に対して、SasakiらはHCAHC (Hypomyelination with cerebellar atrophy and hypoplasia of the corpus callosum) 1)として報告した。臨床的には運動機能障害(痙性、小脳失調、振戦など)、異常な歯牙(歯が少ない、萌出の遅れ、歯列異常)、下垂体性の性腺機能低下症(性成熟の遅延/欠損)などを呈することが知られ、画像・臨床症状の組み合わせから、4H (Hypomyelination, hypodontia, hypogonadotropic hypogonadism) syndrome2)、ADDH (Ataxia, delayed dentition, and hypomyelination)3)、TACH (Tremor-ataxia with central hypomyelination)4)、LO (Leukodystrophy with oligodontia)5)としても報告されてきた。責任遺伝子(POLR3A, POLR3B, POLR1C)が同定され6-9)、これらが一連の表現型の違いによることが解明され、Pol III関連白質ジストロフィーと呼称されている10)。
疫学
発症率は不明であるが、現在までに150例を超える症例が報告されている。
病因・病態
POLR3AおよびPOLR3B遺伝子は、RNA polymerase III (POLR3) 複合体のコアになるサブユニット (RPC1およびRPC2) をコードする。報告された変異は、複合体の3次元モデルの解析からPOLR3活性を低下させると予想されている。POLR3はtRNAと6SrRNAを含む大多数の低分子RNAをコードする遺伝子を転写する。これらの低分子RNA量が不足することにより髄鞘化不全が起きると考えられるが、詳細な機序は不明である。POLR1CはPOLR1, POLR3に共通のサブユニットであるが、報告されている変異はPOLR3形成を障害し、POLR3の核への転送を阻害する。
臨床症状
運動機能障害、異常な歯牙、性腺機能低下症を3主徴とする。105例(POLR3A 43例、POLR3B 62例)の検討11)では、発症年齢はPOLR3A 4.3歳、POLR3B 3.4歳である。約半数(52%)で発達は遅滞し、19例(POLR3A 4例、POLR3B 15例)で独歩は未獲得である。一方、10歳以上で発症する症例も10例認められる。多くの症例で企図振戦、測定障害、歩行失調、円滑追跡眼球運動異常、注視誘発眼振を認める。垂直方向視制限を20%に認め、しばしば早期症状となる。多くは軽度・中等度の知的障害を呈し、10歳代でゆっくり退行することが多い。てんかんは19%に認められるが、薬剤反応性は良好とされる。感染に伴う退行が53%に認められる。歯数減少、萌出の遅れ、歯列異常などの歯牙異常は87%に、思春期遅発症・無月経症はPOLR3Aで81%、POLR3Bで69%に認められる。低身長を半数(51%)に認め、調べられた症例の半数で成長ホルモン分泌不全を呈する。POLR3A遺伝子異常は、POLR3B 3遺伝子異常に比して臨床的に重篤とされる11)。補助歩行はPOLR3Bでは20歳以降で60%以上可能であるのに対し、POLR3では20歳で40%から進行性に低下(30歳以降10%以下)する。生命予後もPOLR3A遺伝子異常の方が不良(下記)である。
POLR1C遺伝子異常8症例の報告では、神経学的異常(8/8例)、近視(4/8)、歯牙異常(3/8)を認めている9)。
検査所見
POLR3A、POLR3B 遺伝子異常の頭部MRI画像は、T2強調画像で大脳白質の全般的な淡い高信号像(hypimyelination)に加えて小脳萎縮、脳梁の菲薄化を認め、さらに基底核の萎縮がないことが共通所見である。視床腹外側部、視放線、淡蒼球、歯状核にはT2低信号を呈する。POLR3B 遺伝子異常の方がPOLR3A遺伝子異常に比して、小脳萎縮の程度が強い一方で、白質低形成(hypomyelination)は軽度と報告されている12)。髄鞘化の程度は、POLR3B遺伝子異常が臨床的にPOLR3A遺伝子異常に比して軽症であることと関連が想定される。POLR1C遺伝子異常では、hypomyelination(8/8)と脳梁の菲薄化(8/8)は全例に認められ、小脳萎縮は 5/8症例に認められる。
脳病理の報告13)(POLR3A遺伝子異常、36歳男性)では、髄鞘・乏突起細胞は著明に消失し、中等度の軸索消失、軽度のアストロサイト・ミクログリアの増生を認める。正常に見える乏突起細胞を巻き込むマクロファージの存在から免疫学的な機序が示唆される。大脳皮質1, II層にはアストロサイトの増生が認められる。
遺伝子診断
POLR3A, POLR3B, POLR1C遺伝子の複合ヘテロ接合変異が報告されている。
治療・ケア
現時点では対症療法に限られる10)。神経症状(痙性、てんかん)に対しては内科的治療、リハビリテーションが施行される。歯科、眼科、内分泌代謝科、リハビリテーションなど総合的な治療・ケアが望まれる。
予後
105例(POLR3A 43例、POLR3B 62例)の検討では、8例の死亡(8-36歳)が報告されている。8例のうちPOLR3B遺伝子異常は1例のみであり、POLR3A遺伝子異常の方が予後不良と考えられる11)。
図の説明
Pol III関連白質ジストロフィー(POLR3B遺伝子異常).
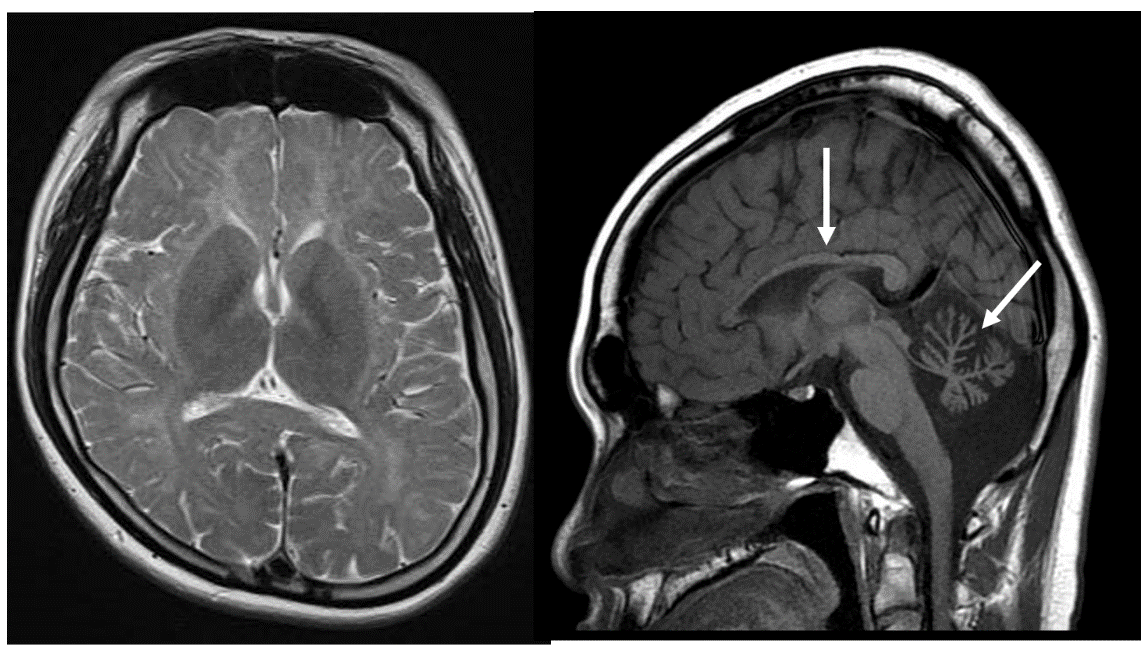
20歳代男性、発達遅滞、性腺機能低下を呈し、POLR3B遺伝子異常を認める。T2強調画像で大脳白質高信号、併せて小脳萎縮、脳梁低形成(矢印)を認める。
文献()内、エビデンスレベル
- Sasaki M, Takanashi J, Tada H, et al. Diffuse cerebral hypomyelination with cerebellar atrophy and hypoplasia of the corpus callosum. Brain Dev 2009; 31: 582-587.(5)
- Timmons M, Tsokos M, Asab MA, et al. Peripheral and central hypomyelination with hypogonadotropic hypogonadism and hypodontia. Neurology 2006; 67: 2066–2069.(5)
- Wolf NI, Harting I, Boltshauser E, et al. Leukoencephalopathy with ataxia, hypodontia, and hypomyelination. Neurology 2005; 64:1461–1464.(5)
- Bernard G, Thiffault I, Tetreault M, et al. Tremor-ataxia with central hypomyelination (TACH) leukodystrophy maps to chromosome 10q22.3-10q23.31. Neurogenetics 2010; 11: 457–464.(5)
- Atrouni S, Darazé A, Tamraz J, et al. Leukodystrophy associated with oligodontia in a large inbred family: fortuitous association or new entity? Am J Med Genet A. 2003;118A: 76-81.(5)
- Bernard G, Chouery E, Putorti ML, et al. Mutations of POLR3A encoding a catalytic subunit of RNA polymerase pol III cause a recessive hypomyelinating leukodystrophy. Am J Hum Genet 2011;89:415–423.(5)
- Tetreault M, Choquet K, Orcesi S, et al. Recessive mutations in POLR3B, encoding the second largest subunit of pol III, cause a rare hypomyelinating leukodystrophy. Am J Hum Genet 2011;89:652–655.(5)
- Saitsu H, Osaka H,Sasaki M, et al: Mutations in POLR3A and POLR3B encoding RNA polymerase III subunits cause an autosomal recessive hypomyelinating leukoencephalopathy. Am J Hum Genet 2011; 89: 644-651.(5)
- Thiffault I, Wolf NI, Forget D, et al. Recessive mutations in POLR1C cause a leukodystrophy by impairing biogenesis if RNA polymerase III. Nat Commun 2015; 6: 7623.(5)
- Bernard G, Vanderver A. Pol III-related leukodystrophies. In: Pagon RA, Adam MP, Ardinger HH, Wallace SE, Amemiya A, Bean LJH, Bird TD, Ledbetter N, Mefford HC, Smith RJH, Stephens K, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2017.
2012 Aug 2.(6) - Wolf NI, Vanderver A, van Spaendonk RML, et al. Clinical spectrum of 4H leukodystrophy caused by POLR3A and POLR3B mutations. Neurology 2014; 83: 1898-1905.(4b)
- Takanashi J, Osaka H, Saitsu H, et al. Different patterns of cerebellar abnormality and hypomyelination between POLR3A and POLR3B mutations. Brain Dev 2014; 36: 259-263.(5)
- Vanderver A, Tonduti D, Bernard G, et al. More than hypomyelination in Pol-III disorder. J Neuropathol Exp Neurol 2013; 72: 67-75.(5)
Pub-med 検索式
- Pol[All Fields] AND III-related[All Fields] AND leukodystrophy[All Fields] 8件
- POLR3A[All Fields] AND leukodystrophy[All Fields] 26件
- POLR3B[All Fields] AND leukodystrophy[All Fields] 19件
- POLR1C[All Fields] AND leukodystrophy[All Fields] 4件














