コステロ症候群
(Costello syndrome)
GeneReviews著者: Karen W Gripp, MD, FAAP, FACMG, Katheline A. Rauen, MD, FAAP, FACMG
日本語訳者:阿部裕,青木洋子(東北大学大学院医学系研究科 遺伝医療学分野)、松原洋一 (国立成育医療研究センター)
GeneReviews最終更新日: 2019.8.29. 日本語訳最終更新日: 2021.6.23.
要約
疾患の特徴
コステロ症候群患者の大多数は多臓器に渡る特徴的な所見を共有しているものの、その表現型スペクトラムは幅広く、軽症なものから早期に致死的となる合併症を伴う重症のものまで存在する。コステロ症候群の典型例では、出生後の哺乳障害に伴う乳幼児期の体重増加不良、低身長、精神発達遅滞、粗な顔貌(分厚い口唇、大きな口、分厚い鼻尖、細くてカールした毛髪、手掌・足底に深いしわを伴う緩く柔らかい皮膚、顔・肛門周囲の乳頭腫、全身の筋緊張低下、手首や手指の尺側偏位を伴う手関節の可動性亢進、アキレス腱拘縮、心合併症(肥大型心筋症による心肥大、肺動脈弁狭窄などの先天心奇形、不整脈:無秩序心房律動/多焦点性心房性頻脈あるいは異所性心房性頻脈)を呈する。大頭症が特徴的で、出生後の小脳過成長によって水頭症や脊髄空洞症を伴うキアリⅠ型奇形を引き起こすことがある。コステロ症候群患者における悪性腫瘍の生涯発生率は約15%で、その内訳は幼少期の横紋筋肉腫や神経芽腫、青年期から成人にかけての膀胱移行上皮癌などである。
診断・検査
コステロ症候群の診断は、本症候群を疑わせる臨床所見と、HRAS遺伝子の病的ヘテロ変異を分子遺伝学的検査で検出することによって確定する。
臨床的マネジメント
臨床症状に対する治療:
成長障害は最もよく認められる症状であるが、臨床的な対応はなかなか困難である。多くの乳幼児では経鼻経管栄養または胃瘻からの経管栄養が必要になる。ニッセン手術(胃底ヒダ形成による噴門形成術)が必要なことも多い。心合併症と悪性腫瘍に対する検査・治療は定期的に行う必要がある。手首や手指の尺側偏位を伴う手関節の可動性亢進に対してはしばしば早期の装具固定、作業・理学療法が必要となる。アキレス腱拘縮に対しては外科的にアキレス腱伸展術が必要になることがある。精神発達遅滞に対しては早期の治療的介入が必要で、個々の症例に応じた教育プログラムが必要である。繰り返す顔面の乳頭腫に対してはドライアイスによる定期的な摘除が必要になる。血行動態学的に問題となるような弁狭窄症に対しては亜急性細菌性心内膜炎予防のために抗生物質の投与が必要である。麻酔は、肥大型心筋症を有する患者や心房性頻拍の素因を持つ患者にとってリスクとなる。
観察:
新生児期の低血糖に対するモニタリングが必要。本症診断時における心エコー検査と心電図検査およびその後の小児循環器専門医(本症における心疾患の特徴と自然歴に精通した医師)によるフォローが必要。横紋筋肉腫や神経芽腫のスクリーニングのため、3〜6ヶ月毎の腹部及び骨盤内超音波検査を8〜10歳になるまで継続することを考慮する。10歳以降、膀胱癌のスクリーニングのため年一回の尿検査で血尿の有無を調べる。
遺伝カウンセリング
コステロ症候群は常染色体優性遺伝形式で遺伝する。これまでの報告によるとコステロ症候群の発端者の大部分は新生突然変異によるものである。発端者の両親が無症状で、親から子へ遺伝した軽症の2家系が報告されている。コステロ症候群は典型的には新生病的バリアントによっておこるので、発端者の同胞が発症するリスクは小さい。しかしながら片親の生殖細胞モザイクが疑われる同胞での発症例が報告されている。通常、コステロ症候群患者自身が子を授かることはない。家族内に患者が存在し、その患者でHRASの病的バリアントが同定されている場合には、出生前診断や着床前診断が可能である。
診断
本症候群を疑わせる臨床所見
下記の所見がみられる場合、コステロ症候群を疑うべきである。
出生前の所見
- 超音波検査
- 後頚部浮腫
- 羊水過多(>90%)
- 特徴的な手首の尺側偏位
- 短い上腕骨と大腿骨
- 胎児頻脈(各種の心房性頻脈)
- 早期産
出生後の所見
- 出生後の著しい哺乳困難が小児期早期まで持続
- 発育障害
- 低身長
- 大頭(相対的)
- 粗い顔貌
- 縮れてまばらで細い毛髪
図1 セントルイスで2005年に開催されたコステロ症候群会議に出席した4人の女児は、コステロ症候群に関連した特徴的な徴候(人懐こく社交的な性格など)を有している。
- 2名の女児(ともに10歳)は、頬、分厚い口唇、眼間解離、眼瞼裂斜下、分厚い鼻尖を有している。左側の女児は縮れた髪を、右側の女児は直毛で細い髪を有することに注意。
- 6歳と9歳の二人の女児は、典型的な手の肢位、大きな口、分厚い口唇を示している。顔が色黒なのは、ひとりがラテン系で、もう一人がアフリカ系アメリカ人のためである。
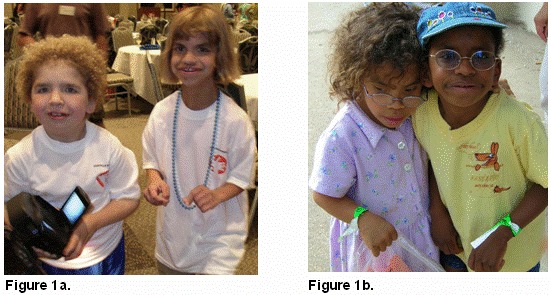
図2 コステロ症候群患者にみられる典型的な顔貌。8歳の北欧系の男児(A)と11歳のヒスパニック系の女児(B)。(Gripp & Lin 2012、Genetics in Medicineからの転載許可取得済)
皮膚
- 緩く柔らかい皮膚
- 色素沈着の増加。
- 手掌・足底の深いしわ
- 顔・肛門周囲の乳頭腫(通常、乳幼児期には認められず、小児期に出現)
- 角化亢進、胼胝
- 早老、毛髪の喪失
筋骨格系
- 全身の筋緊張低下、関節の可動性亢進、筋量低下
- 手首や手指の尺側偏位、特徴的手位となる広がった指
- 平べったい指尖、変形した爪。
- アキレス腱拘縮。しばしば小児期を通じて進行
- 姿勢性足変形
- 垂直距骨
- 脊柱後側弯
- 鳩胸、漏斗胸、左右非対称胸郭
- 発育性股関節形成不全
心血管系
- 心肥大;通常は典型的な肥大型心筋症(すなわち特発性大動脈下狭窄、非対称性中隔肥大)、その他の型(すなわち両心室型)も報告されている。
- 先天心奇形;多くは肺動脈弁狭窄
- 不整脈、通常は上室性・発作性頻脈。最も特徴的なものとして、無秩序の心房性律動/多焦点性心房頻脈あるいは異所性心房頻脈(非リエントリー性頻脈として知られる)
神経系
- キアリⅠ型奇形。時とともに進展することがある。
- 水頭症
- 脊髄空洞症
- けいれん
- 係留脊髄
腫瘍
- 悪性固形腫瘍の発生率の増加
精神運動発達
- 発達遅滞、知的障害
- 社交的、外交的な人格
- 幼児期早期に自閉症スペクトラムを疑わせる所見が4歳までに改善
診断の確定
コステロ症候群の診断は、本症候群を疑わせる臨床所見と、HRASの病的ヘテロ接合性バリアントを分子遺伝学的検査によって検出することで確定する(表1を参照)(Aoki et al 2005, Kerr et al 2008, Grant et al 2018)。
分子遺伝学的検査については、臨床症状によって2種類の異なるアプローチが考えられる。標的遺伝子検査(単一遺伝子検査や複数の遺伝子パネル検査)と包括的ゲノム検査(エクソーム解析や全ゲノム解析)である。
標的遺伝子検査では、臨床医がどの遺伝子が原因となっていそうかを決める必要があるが、包括的ゲノム検査ではその必要がない。コステロ症候群の臨床所見は幅広いため、本症候群を疑わせる臨床所見の項で示された所見を有する患者では標的遺伝子検査で診断される可能性が高い(下記のオプション1を参照)。一方、コステロ症候群が疑われなかった患者では包括的ゲノム検査によって診断される可能性が高い(オプション2を参照)。
オプション1
臨床所見によってコステロ症候群が疑われる場合には、単一遺伝子検査もしくは遺伝子パネル検査が有用である。
- 単一遺伝子検査:HRASのシークエンス解析で、遺伝子内の小さな欠失/挿入/挿入欠失やミスセンスバリアントが検出される。通常はエクソン単位や遺伝子全体の欠失/重複は検出されない。コステロ症候群はHRASの活性化変異が原因となるため、遺伝子を標的とした欠失/重複解析によって病的変異が同定される可能性は低い。
- 複数の遺伝子パネル検査を用いてHRAS及び関連遺伝子群(鑑別診断の項を参照)を解析することにより、VUSや臨床病型とは無関係の病的バリアントの検出を最小限に抑えながら、比較的安価な費用で病因遺伝子変異を同定することが可能である。注意点:(1)パネルに収載された遺伝子の種類と各遺伝子における変異検出感度は検査施設によって異なっており、しかも経時的に変わる可能性が高い、(2)パネル検査のなかにはこのGeneReviewで取り上げた病態とは無関係の遺伝子が含まれている場合がある、(3)検査施設によっては、研究室で独自に開発したパネルや、臨床病型に基づいたエクソーム解析で臨床医から指定された遺伝子を含む解析を行っている場合がある、(4)パネル検査では、シークエンス解析、欠失・重複解析やシークエンス以外の技術が用いられる場合もある。
オプション2
非典型的な表現型であるためにコステロ症候群の診断がなされていない場合は、包括的なゲノム検査(この場合、臨床医がどの遺伝子の異常が疑われるかを決める必要がない)が最良の選択肢である。包括的なゲノム検査としてはエクソーム解析が最もよく行われているが、全ゲノム解析でもよい。
表1.コステロ症候群で用いられる分子遺伝学的検査
| 遺伝子1 | 方法 | この方法による患者での病的バリアント検出率2 |
|---|---|---|
| HRAS | シークエンス解析3,4 | ~100% |
| 欠失・重複解析5 | 適用外6 |
- (略)
- (略)
- シークエンス解析で検出される遺伝子のバリアントは、良性、おそらく良性、不明、おそらく病的、病的のいずれかに分類される。検出されるバリアントは、小さな遺伝子内欠失・重複、ミスセンス変異、ナンセンス変異、スプライシング異常であり、通常、エクソン単位あるいは遺伝子全体の欠失・重複は検出されない。
- コステロ症候群の原因となる病的バリアントの95%以上は、12番目のアミノ酸であるグリシンか13番目のアミノ酸であるグリシンが変異している。
- HRASを対象とした欠失・重複解析は、遺伝子内の欠失または重複を検出するものである。用いられる手法は、定量的PCR、long-range PCR、MLPA、単一エクソンの欠失や重複を検出できるマイクロアレイである。
- コステロ症候群はHRASを活性化させるバリアントによって引き起こされるため、HRASの欠失・重複解析で病的変異が同定されるとは考えにくい。
臨床的特徴
臨床症状
コステロ症候群は多臓器疾患である。典型的な症状は、乳幼児期の全身の筋緊張低下と重度の摂食障害、低身長、発達遅滞、知的障害、特徴的な顔貌、細くてカールした薄い毛髪、手掌・足底に深いしわを伴う緩く柔らかい皮膚、顔・肛門周囲の乳頭腫、手首や手指の尺側偏位を伴う手関節の可動性亢進、アキレス腱拘縮、そして心合併症(肥大型心筋症による心肥大、肺動脈弁狭窄などの先天心奇形、不整脈)である。出生後の小脳過成長によって水頭症や脊髄空洞症を伴うキアリⅠ型奇形を引き起こすことがある。コステロ症候群患者における悪性腫瘍の生涯発生率は約15%で、その内訳は幼少期の横紋筋肉腫や神経芽腫、青年期から成人にかけての膀胱移行上皮癌などである。男性と女性の発症率は同等である。
稀ではあるが、HRASの病的バリアントによっては臨床症状がより重篤で、子宮内胎児水腫、出生後の呼吸器症状を伴う胸水、早期死亡に至る重度の進行性肥大型心筋症が認められる(Lo et al 2008)。他の病的バリアントではより軽症な臨床型を伴うものがあり、軽度発達遅滞、ヌーナン症候群に類似した顔貌、悪性腫瘍の発生リスク低下を示す(Gripp et al 2015, Bertola et al 2017)。
成長
妊娠週数に比して出生体重や頭囲が大きく(しばしば>50パーセンタイル)、コステロ症候群を巨人症と判断し、間違った診断を導くことがある。低身長は必発で骨年齢の遅延がよく見られる(Johnson et al 1998)。部分的ないし完全な成長ホルモン分泌不全が認められることもある。
成長ホルモンを投与されていないコステロ症候群患者の標準成長曲線では、幼児期早期の体重増加不良と低身長(患者の95%は同年齢のこどもの正常範囲の低身長領域)が認められる(Sammon et al 2012)。成人後の身長は135~150 cmと報告されている(Hennekam 2003)
発育障害と重度の摂食障害はほぼ必発で、通常は経鼻経管栄養が必要となる。経験的に患者は高カロリーの摂取が必要である。栄養状態が摂食補給によって改善しても成長遅滞は持続するため、積極的な摂食治療の効果はみられない。
2~4歳ごろになると患児は経口摂取ができるようになる。最初に受け付けるのは、しばしば強い味の食品(ケチャップなど)である。
神経系
大多数の患児は、筋緊張低下、易刺激性、発達遅滞、眼振を示す。
筋緊張低下はしばしば重症なことがあり、筋肉量低下と骨格筋ミオパチーを呈する(van der Burgt et al 2007, Tidyman et al 2011)
出生後の進行性の小脳過成長によって、キアリⅠ型奇形、水頭症、脊髄空洞症を引き起こすことがある(Gripp et al 2010)。小脳病変としては、小脳扁桃下垂、キアリ奇形、脊髄空洞症がある(Gripp et al 2000, 2002, Calandrelli et al 2015)。
脳波異常は約3分の1の患者で認められる。20~50%でけいれんがみられる(Delrue et al 2003, Kawame et al 2003)。
心臓
通常、心臓の異常は幼児期や小児期早期に存在しているが、どの年齢でも気づかれ得る。遺伝子診断で確定されたコステロ症候群患者146人のうち87%に何らかの心臓の異常が存在した。44%に先天性心奇形があり、最も多いのは非進行性の肺動脈弁狭窄であった。心房中隔欠損は稀であった。大動脈下中隔肥大などの肥大型心筋症は61%に、病的心筋異常は70%に認められた。
致死的な重症の肥大型心筋症を呈する新生児も少数存在する。その他の幼少患児では、進行性の重度の肥大型心筋症や多源性心房性頻脈で2歳までに死亡することもある。多源性心房性頻脈及びそのほかの心房性頻脈は大いに懸念されるが、積極的に治療することで通常は自然治癒する。
肺動脈弁狭窄は通常軽度から中等度で、手術やカテーテル治療の対象となる頻度は低い。
肥大型心筋症を有する患児の多くは軽症から中等症である。興味深いことに、中等度から重度の肥大型心筋症を持つ患者の中には、少数ながら年月を経て「リモデリング」が起こり、左心流出路閉塞の消失(あるいは著明な減少)するように見えるものも存在する。これらの患者の中で経過観察されているものは少数であり、その長期自然歴は完全にはわかっていない(Lin et al 2011)。稀な致死的重症型に加えて、肥大型心筋症が慢性的(圧較差の持続)であったり、進行性(圧較差の増大:14/37,37%)、不変型(増悪なし:10/37,27%)、あるいは減少型(治癒:5/37、14%)も認められる。8/37(22%)では予後不明であり(Lin et al 2011)、慎重な観察が必要である。
非リエントリー性心房性頻脈は一般に自然治癒するが、約4分の1で持続あるいは悪化する。非リエントリー性心房性頻脈の発症は肥大型心筋症とは無関係である(Levin et al 2018)。
中等度の肥大型心筋症または新規の不整脈を有する年長の患者(16~40歳)は最大の課題で、現時点では情報不足で予後の予測が困難である。高血圧は稀ではない。
大動脈二尖弁を伴わない軽度~中等度の大動脈拡張は、最近発見された心循環器病態で、約5%の患者にみられる。
一次的血管病変は稀にしか報告されていない。稀なGly12Glu変異をもつ早期致死的コステロ症候群患者1名では、肺血管異形成があり、小さな動脈と静脈にエラスチン分布異常が認められている。この患者では目立った肥大型心筋症はなかった(Weaver et al 2014)。
発達遅滞・知的障害
発達遅滞・知的障害はすべての患者で認められる(Axelrad et al 2004, 2007, 2009, 2011)。
言語記憶機能における認識記憶は、他の認知タスクに比して比較的保たれている(Schwartz et al 2013)。
発語の時期は、経口摂取を受け入れるようになった時と同時のことが多い。
分離不安障害はコステロ症候群患者の39%でみられるが、女児よりも男児に多い(Axelrod et al 2011)
行動/社会的課題
4歳以下の患者の多くは、自閉症スペクトラムのスクリーニングで診断基準を満たす。胃瘻チューブの必要性と独歩不能の間には正の相関がある。その一方で、4歳以上の患児は自閉症スペクトラムスクリーニングの診断基準を満たさないことから、自閉症スペクトラムの早期兆候は4歳までに消失することが示唆される(Schwartz et al 2017)。
年長のコステロ症候群患者におけるQOLに関する詳細な情報は限られている。16~34歳の患者でのQOLは4つの点において妥協したものとなっている:ごく近しい友人や家族以外の人間関係が限られる、自立していない、男性としての生殖機能不全、医療的課題の存在の4点である(Hopkins et al 2010)。可動性に関する整形外科的な問題から生じる機能的な制限や、社会的・認知的な制限が明らかにされている(Johnson et al 2015)。
皮膚
乳頭種は幼児期には見られず小児期に出現する。通常は鼻周囲に多いが、肛門周囲、体幹、四肢にもみられる。乳頭種は多くの場合美容的な懸念に留まるが、かなり目立って厄介になることもある。
手掌足蹠の角化症はよく見られ、重症例では機能にも影響を及ぼす(Murakian et al 2017)。そのほかには黒色表皮腫や厚い足爪がある。
筋骨格
コステロ症候群患者は関節の弛緩が著明(とくに指)である。手首や手指の尺側偏位もよくみられる。発育性股関節形成不全は激痛を起こし歩行の妨げになることがある。アキレス腱拘縮が起きることもある。
43名の患者コホートに対して整形外科医がX線写真の所見を調査したところ、半数以上に靱帯の弛緩 、側弯症、後彎症、特徴的な手と手首の変形、肩と肘の拘縮、アキレス腱拘縮、偏平足を認めた(Detweiler et al 2013)。股関節異形成が45%に認められたが、すべてが先天性ではなく後天性のものもあった。
骨粗鬆症がコステロ症候群の若年成人患者によくみられる(White et al 2005, Detweiler et al 2013)。16歳から40歳の成人では、骨密度を測定した8人すべてに異常があり、骨粗鬆症または骨減少が示唆された。そのうち3名では骨痛、脊椎骨折、身長低下があった(White et al 2005)。二重エネルギーX 線吸収測定法で検査された9名の患者では、正常対照群と比較してすべてに骨密度の著明な低下があった(Leoni et al 2014)。
呼吸器
睡眠ポリグラフ検査を検査室で受けた3歳から29歳の患者10人のうち7人で閉塞所見があった(Della Marca et al 2006)。文献検索では新生児の78%に呼吸器合併症が認められたが、その大半は治癒し、重症な臨床病型を伴う稀なHRASバリアントを持つ患者だけが重篤な合併症を有していた(Gomez-Ospina et al 2016)。
上気道閉塞は年長小児や若年成人に多い傾向があった(Gomez-Ospina et al 2016)。
内分泌
新生児高インスリン血症が報告されている(Alexander et al 2005, Sheffield et al 2015)。1例では膵臓の結節に限局した11p片親性ダイソミーと関係していた(Gripp et al 2016)。
年長患者では、低血糖は成長ホルモン分泌不全に関係しているかもしれない。成長ホルモン分泌不全はよく認められる(30~50%)(Estep et al 2006, Gripp et al 2010).
甲状腺機能低下症がありホルモン補充療法を要した患者数名が報告されている。
そのほかの内分泌異常としては、思春期遅発症や思春期早発症がある。
固形腫瘍
コステロ症候群患者では、一般集団に比べて非常に高い頻度で良性あるいは悪性の固形腫瘍が発生する。HRASの病的バリアントが同定された患者における悪性腫瘍の生涯発生率は約15%である(Gripp et al 2006a)。Kratzら(2011)が行った文献検索でもコステロ症候群患者における20歳までの累積がん発生率は約15%であることが確認された。横紋筋肉腫が最も効率に発生し、神経芽腫、膀胱移行上皮がん、その他の固形腫瘍と続く(Gripp 2005)。
横紋筋肉腫と神経芽腫はいずれも乳児期早期に認められる腫瘍であるが、コステロ症候群患者における発症年齢は一般集団と同じである。その一方、一般集団では高齢成人(70%が65歳以上)において発生する膀胱移行上皮がんが、コステロ症候群では青年期に発見されることがある。コステロ症候群患者3名での膀胱移行上皮がんの発症年齢は、10歳、11歳、16歳であった。
その他
- 幽門狭窄は一般集団よりも高頻度にみられる(Gripp et al 2008)。
- Whiteらの報告では成人期発症の胃食道逆流が4名の患者でみられた。追加症例も知られている(筆者の経験)。
- エナメル欠損を含む歯科異常の頻度は高い。上顎第一臼歯が下顎第一大臼歯よりも後方に位置する不正咬合はよくみられ、閉塞性睡眠時無呼吸の原因となることがある(Goodwin et al 2014)。しばしば分泌過多が認められる(Johnson et al 1998)。
- よく見られる視力異常や眼振に加えて、より頻度が低い眼科的異常として網膜変性(Pierpont et al 2017)と円錐角膜(Gripp & Demmer 2013)がある。
- 青年期の患者は、後側弯症、薄毛、早すぎる皮膚の老化があるため、実際の年齢よりも老けて見えることがある。
寿命
心血管系の解析が行われた患者の10%で(Lin et al 2011)、また文献に記述されている患者の20%で死亡原因が報告されており、その内訳はがんに合併した肥大型心筋症、冠動脈の線維筋性異形成、多源性頻脈、眼、肺疾患、多臓器不全である。
体細胞モザイク
HRASの病的バリアントの体細胞モザイクを持つ患者は、斑状の皮膚所見のみを示す(典型的なコステロ症候群患者の父親で報告されている:Sol-Church et al 2009)(Bertola et al 2017)こともあれば、生殖細胞系列の病的バリアントを有するコステロ症候群患者と区別できない臨床症状を持つ患者もいる(Girisha et al 2010)。
体細胞モザイクを持つある一人の患者(頬粘膜由来DNAの20~30%にHRASの病的バリアントp.Gly12Serがあるものの、血液由来のDNAには検出されない)は、コステロ症候群に起因する典型的な症状(知的障害、低身長、薄毛、粗な顔貌、鼻部の乳頭種、アキレス腱拘縮)をもつ一方で、モザイクに起因する非典型的な症状(小頭、色素沈着部分と脱色部分を線状にもつ皮膚、正常な初潮とそれに続く正常月経周期)がみられた(Gripp et al 2006b)。
神経画像
脳脊髄MRI検査に関する系統的レビューによると、28例中27例に小脳扁桃ヘルニアを伴う後頭蓋窩混雑(posterior fossa crowding)を認めることが明らかにされた(Gripp et al 2010)。これらの論文の大半で、この狭小化は進行性であった。小脳過成長が進行性(Paquinら(2009)が報告したように異常な細胞分化に由来すると思われる)であるため、後頭蓋窩混雑の後遺症としてシャント留置または脳室造瘻が必要な水頭症(7/28)、キアリⅠ型奇形(9/28)、脊髄空洞症(7/28)がみられる。
脊髄係留症が比較的よく認められる。
遺伝子型と臨床型の関連
HRASの病的バリアントを有する146人の系統的レビューでは、特定のバリアントと検討対象となった病態(肥大型心筋症、多源性頻脈、大動脈拡張)との間に明らかな相関はなかった(Lin et al 2011)(表5を参照)。数が少なく統計的処理ができないケースもあった。
p.Gly12Ser以外の変異を持つ患者はほとんど同定されていないため、遺伝子型と臨床型の関連は限定されている。
- Kerrら(2006)は、p.Gly12Ala変異を持つ患者 (4/7、57%)はp.Gly12Ser変異を持つ患者(4/65、7%)に比べて悪性腫瘍のリスクが高いことを示唆している。これまでのところp.Gly13Cysを有する患者で悪性腫瘍は発生していない(Gripp et al 2011a)。
- Loら(2008)は、より重症な新生児表現型は、p.Gly12Serやp.Gly12Cysを含む特定の稀な病的バリアントに関連していることを示唆したが、このことはMcCormickら(2013)によって追認されている。
- p.Thr58Ile、p.Ala146Valあるいはp.Gly60Val変異を持つ患者は、より軽症な表現型と関連する可能性がある(Gripp et al 2008, 2017)。
- 血縁関係がないp.Glu37dupをもつ2名の患者は、いずれも著しい薄毛と他の患者に比べてあまり粗野ではない顔貌を呈していた(Gremer et al 2010)。
- p.Gly13は2番目に最も多いアミノ酸置換がみられるコドンであるが、その中ではp.Gly13Cysが最も多い。Grippら(2011a)がこのアミノ酸置換を持つ患者12名について検討したところ、dolichocilia(しばしばトリミングが必要なほど極めて長い睫毛)と成長期性脱毛症候群(loose anagen hair syndrome)を含む特徴的な表現型がみられた。これらの症状は、それ以前にはコステロ症候群患者で認められていなかった。乳頭種や多源性頻脈はp.Gly13Cysを持つ患者ではみられておらず、低身長もほとんどない。最も頻度が高いp.Gly12Serをもつ患者と比較して、上記の差異は統計学的に優位である。
- 稀なp.Gly13Aspミスセンス変異を持つ5名の患者は、より軽症のようであり、悪性腫瘍発生例はなかった(Bertola et 2017)。
浸透率
浸透率は100%である(Aoki et al 2005、Estep et al 2006、Gripp et al 2006a、Kerr et al 2006)。
病名
コステロが1971年にこの病態の患者を初めて報告し、1977年と1996年に続報を報告している(Costello 1971,1977,1996)。Der Kaloustianら(1991)が、はじめて発見者の名を冠したコステロ症候群の名称を用いている。
コステロ症候群の名称が使用される以前には以下のように報告されている:
- AMICABLE症候群(amicable personality、mental retardation、impaired swallowing、cardiomyopathy、aortic defects、bulk、large lips and lobules、ectodermal defects)(Hall et al 1990)
- Faciocutaneous-skeletal syndrome(Borochowitz et al 1992)
頻度
コステロ症候群の出生頻度は英国では38万人に1人と推定されている。その一方、日本での頻度は全国疫学調査によって123万人に1人と示唆されている。後者については、確認手段の観点から過小評価されている可能性がある。
遺伝学的に関連した(アレリックな)疾患
生殖細胞系列の病的バリアント:
HRASの生殖細胞系列変異による他の臨床型は知られていない。
散発性の腫瘍:
コステロ症候群の症状は全くなく、単一の腫瘍として起こる孤発性の腫瘍(膀胱がんや肺がんのような成人期の悪性固形腫瘍を含む)はしばしばHRASの体細胞バリアントを有しているが、生殖細胞系列にはそのバリアントは存在しない。このような場合、腫瘍への易罹患性は遺伝しない。
鑑別診断
コステロ症候群の原因となる他の遺伝子座位は同定されていない(Grant et al 2018)。以前の報告でコステロ症候群が疑われたもののHRASの病的バリアントがない患者のうち10~15%は、その後cardiofaciocutateous (CFC)症候群(Rauen 2006, Gripp et al 2007)またはKRASの病的バリアントをもつヌーナン症候群であることが判明した(Lo et al 2009)。幼児期や小児期早期にコステロ症候群患者をCFC症候群やヌーナン症候群と鑑別することは難しいが、年長の患者ではコステロ症候群とヌーナン症候群は明確に区別できる。
注:コステロ症候群の表現型が他の染色体異常症候群と見誤れることはまずない。
表2コステロ症候群の鑑別診断にあたって考慮すべき疾患
| 鑑別疾患 | 遺伝子 | 遺伝形式 | 鑑別疾患の臨床像 | |
|---|---|---|---|---|
| コステロ症候群に重なる臨床像 | コステロ症候群とは異なる臨床像 | |||
| Cardiofaciocutateous (CFC)症候群 | BRAF KRASMAP2K1 MAP2K2 |
AD |
|
|
| ヌーナン(Noonan)症候群 | BRAF KRAS MAP2K1 NRAS PTPN11 RAF1 RIT1 SOS1 |
AD |
|
|
| Beckwith-Wiedemann症候群 | 脚注2参照 |
|
|
|
| Simpson-Golabi-Behmel症候群 | GPC3 | X連鎖 | 発達遅滞 |
|
| Wiliams症候群 | 脚注2参照 | AD > |
|
|
脚注
- 遺伝学的検査でCFC症候群と診断された患者の約40%に肥大型心筋症が認められるが、この頻度はコステロ症候群とほぼ同じである(Niihori et al 2006, Rodriguez-Viciana et al 2006, Gripp et al 2007)。CFC患者の少数に心房性頻脈が報告されているが、無秩序型心房性律動とはされていない(Niihori et al 2006)。
- Beckwith-Wiedemann症候群は、染色体11p15.5における2か所のインプリンティングドメインにおける遺伝子転写の調節異常を伴う。Beckwith-Wiedemann症候群患者の約85%には、本症候群の家族歴はないが、約15%では家族歴があり親由来の常染色体優性遺伝形式に合致する。
- Wiliams症候群の原因は、7q11.23の隣接遺伝子部位の反復性欠失であり、この部分にはエラスチンをコードするELNを含むWilliam-Beuren syndrome critical region (WBSCR)がある。
臨床的マネジメント
最初の診断時に引き続いて実施すべき評価
コステロ症候群と診断された患者における病状の程度を明らかにするために、表3にまとめた評価を行うこと(診断に至る経過で実施されていなければ)が推奨される。
表3 初めてコステロ症候群と診断された患者に対して推奨される評価項目
| 臓器・検討対象 | 評価 | コメント |
|---|---|---|
| 体格 | 身長、体重、頭囲の測定 | 発育障害はよく見られ、適切なカロリー摂取にもかかわらず持続する。 |
| 消化管/摂食 | 栄養状態、摂食、胃食道逆流の評価 | 発育障害は典型的:経鼻栄養チューブが必要 |
| 神経 | キアリⅠ型奇形・脊髄空洞症の臨床兆候に関する神経専門医の診察 |
|
| けいれんが懸念される場合、脳波検査 | ||
| 発達 | 発達評価 |
|
| 心臓 | 先天心奇形、肥大型心筋症、不整脈に関する循環器専門医の評価 | 標準的な評価 |
| 呼吸器 | 必要であれば、呼吸器専門医に紹介 | 上気道と下気道の問題が生じることがある:扁桃とアデノイド肥大が上気道閉塞を起こすことがある |
| 筋骨格 | 小児整形外科医の評価 | 股関節の異常と可動域に注意して、脊柱および四肢を評価 |
| 泌尿生殖 | 男性の場合、停留精巣 | |
| 眼 | 眼科学的評価 |
|
| 皮膚 | 乳頭種と角化亢進について皮膚科への紹介が必要 | 対症療法 |
| 歯 | 小児歯科への紹介を推奨 | エナメル質欠損と不正咬合はよく見られる |
| 内分泌 | 低血糖、成長ホルモン分泌不全について小児内分泌専門医の評価 | 思春期発来の異常についても評価が必要なことがある |
| 精神/行動 | 必要に応じて神経精神的評価 | 4歳以上の患者に対して、睡眠障害、ADHD(注意欠陥/多動性障害),不安、ASD(自閉症スペクトラム)を疑わせる兆候を含む行動異常のスクリーニング |
| そのほか | 臨床遺伝専門医、遺伝カウンセラーへの相談 | 遺伝カウンセリングを含む |
症状に対する治療
コステロ症候群患者に対する医学的管理ガイドラインが作成されている(Gripp et al 2019)。
表4 コステロ症候群患者における各種症状の治療
| 臓器・検討対象 | 治療 | 考慮すべき点/その他 |
|---|---|---|
| 摂食 | ほとんどの乳幼児において経鼻栄養チューブまたは胃瘻が必要 | 胃食道逆流と易刺激性に対してニッセン噴門形成術が必要になることがある |
| 幽門狭窄 | 標準的手術療法 | |
| けいれん |
|
水頭症、低血糖、副腎皮質ホルモン欠乏を考慮 |
| 発達遅滞/知能障害 | 「発達遅滞/知能障害の管理」の項を参照 | |
| 非リエントリー性頻脈(無秩序の心房性律動/多焦点性心房頻脈) | 抗不整脈薬投与やアブレーションなどの積極的な治療が必要になることもある |
|
| 先天心奇形 | 標準的治療に従う | 特定の先天心奇形(とくに肺動脈弁狭窄)は、亜急性細菌性心内膜炎防止のために抗生剤の予防投与が必要 |
| 大動脈拡張 | 大動脈拡張はまだ長期的に観察されておらず、稀で、軽症~中等度であること、さらにこれまで解離を起こしたという報告がないことから、現時点では治療を推奨するデータがない。診療方針は個別に判断すべき。 | |
| 上気道・下気道の閉塞 |
|
|
| 筋骨格 | 手首・指の尺側偏位 | 早期の装具着用:作業療法、理学療法 |
| 大関節の伸展制限に対する理学療法 | ||
| 脊柱後側弯症は手術矯正が必要なこともある | ||
| 停留精巣 | 手術 | |
| 眼/視機能 | 眼振 | 無治療 |
| 視力障害 | 教育的介入 | |
| 屈折異常 | 眼鏡矯正 | |
| 円錐角膜 | 専門医による評価と治療 | |
| 皮膚 | 洗いにくい身体の部位にある乳頭腫が炎症を起こしたり刺激性である場合、必要に応じて除去。角化亢進の治療 | 顔面の再発性乳頭腫:ドライアイスによる定期的な除去を考慮、あるいは切除 |
| 歯 | 小児歯科医・矯正歯科医による | エナメル質欠損。閉塞性睡眠時無呼吸をおこす不正咬合 |
| 低血糖 | ジアゾキサイド | 新生児高インスリン血症に対して |
| 成長ホルモン補充療法2(下記の項参照) | 成長ホルモン分泌不全に対して | |
| コルチゾール | コルチゾール分泌不全に対して | |
| 思春期発来の異常 | 患者の必要に応じて | |
| 悪性腫瘍 | 標準プロトコールに従う | 最もよく見られるのは、横紋筋肉腫、神経芽腫。膀胱移行上皮がん |
| 麻酔のリスク/鎮静 |
|
|
| 家族/地域社会 |
|
障害者スポーツやスペシャルオリンピック(知的障害者のためのオリンピック競技)への参加を考慮 |
- 両親/介護者に対し、よく見られるけいれん症状について教育しておくことが適切である。
- 成長ホルモン補充療法は、肥大型心筋症に関する心臓の評価を済ませてから行う。
成長ホルモン補充療法
成長ホルモンによる治療を考慮する場合には、その利点(まだ証明されていない)と潜在的なリスク、すなわちコステロ症候群患者でみられる肥大型心筋症と悪性腫瘍のリスクについて十分検討しておくべきである。成長ホルモン補充療法がこれらのリスクを高めることは示されていない。
- まだ証明されていない利点。コステロ症候群患者は、しばしば成長ホルモンのレベルが低い:
- 真の成長ホルモン分泌不全は成長ホルモン補充を必要とする。成長ホルモン分泌不全を持つ3名の患者で3~7年間成長ホルモン補充を行ったところ、成長が加速し副作用はなかった。しかしうち2名では低身長のままであった(Stein et al 2004)。
- 文献的には、部分的な成長ホルモン分泌不全を持つコステロ症候群患者で成長ホルモンが有効かどうかは不明である。負荷試験で異常な成長ホルモン分泌反応を示した患者で良好な初期の成長反応があった例が報告されている(Legault et al 2001)。
- 肥大型心筋症。成長ホルモンの同化作用が既に存在する肥大型心筋症を悪化させるかどうかは不明であるが、初期の症例報告ではその関連は示唆されない(Lin et al 2002, 2011)。稀なケースでは、成長ホルモン補充療法の開始後に肥大型心筋症が進行したが、因果関係があるのか偶然なのかは不明である(Kerr et al 2003)
- 悪性腫瘍。成長ホルモンが腫瘍発症に影響するかどうかは不確定である。関連性を示唆する2つの報告がある:
- 成長ホルモン療法を受けた16歳の患者が膀胱がんを発症した(Gripp et al 2000)。
- 生後12か月から成長ホルモン療法を受けた26か月の患者で横紋筋肉腫が診断された(Kerr et al 2003)。
発達遅滞・知的障害の管理
以下の情報は、発達遅滞/知的障害を持つ患者に対して推奨される米国での典型的な管理基準を示したものである。国によって勧告基準は異なるであろう。
0~3歳。初期介入プログラムへ紹介し作業療法、理学療法、言語療法、摂食療法を受けさせることが推奨される。米国では、初期介入は連邦政府によって資金提供されるプログラムであり、すべての州で適用される。
3~5歳。米国では地域の公立学校区を通じた就学前の発達教育が推奨される。配置前に、必要なサービスと治療を決めるための評価がなされ、個々人に応じた教育プラン(Individualized Education Plan : IEP)が作られる。
すべての年齢。適切なコミュニティ、州、教育機関の参画を確実にし、また、両親を支援してQOLを高めるため、発達専門の小児科医へコンサルテーションすることが推奨される。考慮すべき点は以下の通り:
- IEPサービス:
- IEPは、対象となる子供に対して、専用に作成された指導マニュアルおよび関連するサービスを提供するものである。
- IEPは毎年見直しがなされ、変更が必要かどうかが決められる。
- 特別教育法で求められていることに従い、学校で実行可能な範囲で最小限の制限環境下で、可能な限り普通の教育が受けられるようにすべきである。
- 視力及び聴力の専門家がこどものIEPチームに加わり、教材へのアクセス支援を行うべきである。
- IEPの一環として理学療法、作業療法、言語療法が提供され、子どもが教材にアクセスすることを支援する。患者の必要性に応じて個人的な支援治療も考慮すべきである。各種の治療に関する個別の勧告は、発達専門の小児科医によって作成される。
- 子供が10歳代になると、移行期の計画について検討しIEPに組み入れるべきである。IEPサービスを受けている者に対し、公立学校区は21歳までサービスを提供する必要がある。
- 504プラン(障害による差別禁止法)に従って、教室内席順配置、補助機器使用、ノート書取り、授業間の休憩時間延長、課題割り当て、テキストの拡大などを必要とする者に対して配慮する。
- Developmental Disabilities Administration (DDA)への登録が推奨される。DDAは米国の公的機関でサービスと支援を必要としている人に提供する。登録基準は州によって異なるが、一般的には診断名とそれに伴う認知/適応障害によって決定される。
- 収入や資産が乏しい家庭は、障害を持つこどもに対するSupplemental Security Income (SSI)に該当する。
運動機能障害
粗大運動機能障害
- 可動性を最大限にするため、理学療法が推奨される。
- 必要に応じて耐久性のある医療機器の使用を考慮(例:車椅子、歩行器、入浴椅子、装具、ベビーカー)。
微細運動機能障害 食事、身繕い、着衣、書字などの適応機能に影響する微細運動機能障害に対して作業療法が推奨される。
口腔運動機能障害 経口摂取が安全と考えられる患者で口腔運動機能障害のために摂食が困難な場合、摂食療法(一般的には作業療法士または言語療法士による)が推奨される。
口腔運動機能障害 は受診のたびに評価し、食事中の窒息/むせ、体重増加不良、頻回の呼吸器疾患、説明のつかない拒食がある場合には。臨床的な摂食評価やX線嚥下機能検査を実施すべきである。経口摂取が安全と考えられる患者では、協調運動の改善や感覚に関連する摂食障害の改善のために、摂食療法(一般的には作業療法士または言語療法士による)が推奨される。安全のため食物にとろみをつけたり冷やしたりすることもできる。重度の摂食障害に対しては、一般的に経鼻胃管や胃管が必要となる。
コミュニケーション障害 言語表現が困難な患者については代替のコミュニケ-ション方法(例:Augmentative and Alternative Communication: AAC~表情・身振り、道具、機器などの代替手段を活用する意思疎通)を評価検討する。AACの評価はそれを専門とするspeech-language pathologist(会話言語病理医)によってなされる。その評価では、認知能力と感覚障害を勘案し、最も適したコミュニケ-ション方法を決定する。AACに用いられる機器は、絵カード交換式コミュニケーションのようなローテクから、音声生成装置のようなハイテクまで幅広い。一般に信じられていることとは逆に、会話言語の発達を邪魔せず、多くの場合改善することができる。
社会的/行動的課題
患児に対して、自閉スペクトラム障害に用いられる応用行動分析(Applied behavior analysis: ABA)などの介入法が有用である。ABA治療は、個々の患児の行動的、社会的、適応性の強さ/弱さに的を絞って、学会認定行動分析士(board-certified behavior analyst)と一対一で行われるのが一般的である。
発達専門の小児科医に助言を求めることは有用で、適切な行動管理方法を両親に指導したり、必要に応じてADHDの治療薬を処方する。
重度の攻撃的・破壊的行動が問題となる場合は、小児精神科医に任せる。
追跡観察
表5 コステロ症候群患者に対して推奨される追跡観察項目
| 臓器/検討対象 | 評価 | 頻度 |
|---|---|---|
| 内分泌 | 新生児低血糖に対して | 低血糖のリスクをもつ新生児に対する一般的なプロトコール |
| 成長ホルモン分泌不全 | よく見られる。補充が必要 | |
| 心血管 | 心疾患のスペクトラムとその自然歴に精通した循環器専門医による。適当な年齢に達したときに、小児循環器専門医から成人循環器専門医への移行。 | 脚注1)参照 |
| 神経 | 幼小児期および症状を示す患者すべてに対し、繰り返し脳画像検査でキアリⅠ型奇形の有無を検索 | 1歳時。症状があるとき。 |
| 係留脊髄に対する画像検査 | 1歳までに。その後は症状があるとき。 | |
| けいれんのある患者に対して臨床的に必要と考えられる場合モニター | 治療を行う神経専門医の推奨に従う | |
| 腫瘍スクリーニング2 | 腹部・骨盤内超音波検査による横紋筋肉腫と神経芽腫3のスクリーニング | 8~10歳になるまで3~6か月毎 |
| 尿潜血検査による膀胱がんのスクリーニング | 10歳以降毎年 | |
| 筋骨格 | 骨折している患者に対してベースライン骨密度測定 | ベースライン検査の結果による |
| 発達遅滞/知的障害 | 発達の進捗と教育ニーズのモニター | 診断時。その後、学童では少なくとも年1回 |
| 精神/行動 | 不安、注意力、攻撃的・自傷的行動に関する行動評価 | 必要に応じて。学童では少なくとも年1回 |
- 一般的なガイドライン(Lin et al 2011)は、実際的には肥大型心筋症の有無で二分される。生後2年以内は、肥大の重症度、毎年の検査、適切なリスクの層別化に従って緊密に評価。
- 現時点では、どのスクリーング法もその有効性は示されておらず、研究進行中である。腫瘍早期発見において最も重要な点は、両親と主治医が腫瘍発生のリスクを認識していることである。
- 腫瘍が認められないコステロ症候群患者でカテコラミン代謝産物の上昇がみられることから、異常カテコラミン代謝産物のスクリーニングは有用ではないと結論されている(Gripp et al 2004)。
血縁者における発生リスクの評価
遺伝カウンセリングの項を参照
研究段階の治療法
様々な疾患と病態に対する臨床試験の情報は、米国のClinicalTrials.gov、欧州のEU Clinical Trials Registerを検索すると得られる。遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
コステロ症候群患は常染色体優性(顕性)遺伝形式によって遺伝する。通常は新生の優性病的バリアントによる。
家族構成員のリスク
患者の両親
- これまでのところ、ほとんどのコステロ症候群患者は新生の病的バリアントによる。高齢の親との関連が報告されている(Giannoulatou et al 2013)。父親の生殖細胞系列に由来する新生の病的バリアントがほとんどであるがすべてではない。Sol-Churchら(2006)の報告によると14例は新生病的バリアントは父由来で、2例は母由来であった。
- 垂直遺伝は2家系で報告されており、まれな軽症のコステロ症候群患者であった(臨床症状の項を参照)(Gripp et al 2012, 2015)
- 新生病的変異が明らかにされた患者の両親に対して分子遺伝学的検査が推奨される。
- 患者で同定されたHRASの病的バリアントが、いずれの両親の白血球DNAにも検出されない場合、患者はおそらく新生の病的バリアントを有している。もう一つの可能性は、親の体細胞系列/生殖細胞系列モザイクである。
ある症例報告では親の一人における体細胞系列/生殖細胞系列モザイクが示唆され(Bodkin et al 1999)、後に遺伝学的検査で確認された(Sol-Church et al 2009)。遺伝学的検査で確定されたコステロ症候群患者の同胞におけるハプロタイプ解析で、母由来の生殖細胞系列モザイクが病因として示唆された(Gripp et al 2011b)。
発端者の同胞
患者の同胞における罹患リスクは、患者両親の遺伝子の状態によって異なる。
- 患者で同定されたHRASの病的バリアントが、いずれの両親の白血球DNAにも検出されない場合、次子における再発リスクは、親の生殖細胞系列モザイクの可能性があるため、一般集団よりもやや高い。
- コステロ症候群の次子における再発が報告されており、親の生殖細胞系列モザイクの結果と推測されている(Zampino et al 1993, Johnson et al 1998)。患者の両親の項を参照。
発端者の子
- 軽症の表現型を持つ患者の子供が、HRASの病的バリアントを受け継ぐ確率は50%である。
- 典型的なコステロ症候群患者は、通常こどもを生まない。
その他の血縁者
コステロ症候群は、通常、新生の病的バリアントでおこるため、その他の血縁者における再発リスクは増加しないと推定される。
関連する遺伝カウンセリング課題
家族計画
- 遺伝的リスクを確定し、出生前/着床前遺伝学的検査について検討する最適なタイミングは、妊娠前である。
- コステロ症候群患者の両親に対して遺伝カウンセリング(次子罹患の潜在的リスクと可能なオプションに関する相談を含む)を提供することは適切である。
DNAバンキングは、将来使用する可能性のためにDNAを保管しておくことである。将来、検査手法、遺伝子・バリアント・疾患に関する私たちの理解が進む可能性が大きいため、患児のDNAを保管することを考慮すべきである。
出生前検査と着床前検査
遺伝学的検査
家族内の患者にHRASの病的バリアントが同定されていれば、リスクが高い妊娠における出生前検査や着床前検査が可能である。
コステロ症候群のリスクが高いと考えられていない妊娠における超音波検査
コステロ症候群胎児の表現型(項部肥厚、大頭、長管骨の軽度短縮、羊水過多、胎児頻脈)は疾患特有のものではない。そのため、稀な疾患であるコステロ症候群が考慮されないこともしばしばある。しかしながら、重度の羊水過多があり、胎児の染色体分析や染色体マイクロアレイが正常で、胎児心房性頻脈がある場合には、コステロ症候群の診断名を考慮すべきである。
資源
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- Costello Syndrome Family Network
1702 Tyndall Drive, Panama City FL 32401, USA
Phone: 848-228-CSFN (2736); 850-832-4055
Email: iinfo@CostelloSyndromeUSA.org; sandra@CostelloSyndromeUSA.org; Cherie@CostelloSyndromeUSA.org
www.CostelloSyndromeUSA.org
- CostelloKids UK
Manchester, United Kingdom
www.costellokids.com
- My46 Trait Profile
- National Library of Medicine Genetics Home Reference
- RASopathiesNet
244 Taos Road, Atlandena CA 91001, USA
Phone: 626-676-7694
Email: lisa@rasopathies.org
rasopathiesnet.org
- Children's Craniofacial Association (CCA)
13140 Coit Road, Suite 517, Dallas TX 75240, USA
Phone: 800-535-3643 (toll-free)
Email: contactCCA@ccakids.com
www.ccakids.org
- MAGIC Foundation
4200 Cantera Drive #106, Warrenville IL 60555, USA
Phone: 800-362-4423 (Toll-free Parent Help Line); 630-836-8200
Fax: 630-836-8181
Email: contactus@magicfoundation.org
www.magicfoundation.org
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A コステロ症候群:遺伝子とデータベース
| 遺伝子 | 染色体座位 | タンパク | HGMD | ClinVar |
|---|---|---|---|---|
| HRAS | 11p15.5 | GTPase HRas | HRAS | HRAS |
表B コステロ症候群に関するOMIM記載事項
| 190020 | HRAS PROTOONCOGENE, GTPase; HRAS |
| 218040 | COSTELLO SYNDROME; CSTLO |
遺伝子構造
HRASは、約3,300 bpの小さな遺伝子である。最長の転写産物バリアントNM_005343.3は6つのエクソンをもち、うち4つはアイソフォーム1(189個のアミノ酸よりなるタンパクで分子量21 kd(p21)(NP_005334.1))をコードする。選択的スプライシングによって生じる転写産物バリアントNM_176795.4はアイソフォーム2(170個のアミノ酸よりなるタンパク (NP_789765.1))をコードする。アイソフォーム1と比較して、アイソフォーム2は152-165残基を欠いている。
遺伝子とタンパクに関する情報の詳細な要約については、表A 遺伝子を参照。
病的バリアント
厳選された病的バリアントについては表6を参照。塩基置換の結果12番目または13番目のグリシン残基を置換する生殖細胞系列の病的バリアントが、コステロ症候群でよくみられる(Sol-Church & Gripp 2009)。
コステロ症候群の孤発例81名(Aoki et al 2005, Gripp et al 2006a, Kerr et al 2006)について検討すると、塩基置換c.34G>A(アミノ酸置換p.Gly12Serをおこす)が最も多かった(65/81、80%)。p.Gly12Alaを生じる塩基置換c.35G>Cは7名にみとめられた(9%)。
Estepら(2006)は、33名のコステロ症候群患者について上記の2つと同じバリアントを報告し、臨床症状をまとめた。注意:Estepらにより報告された患者のうち数名はGrippらによる報告(2006a)に含まれていた。両方の報告に含まれる患者を同定できなかったため、Estepらによる報告(2006)はこの数字には含まれていない。
他の病的バリアント(すなわち、p.Gly12Val、p.Gly12Cys、p.Gly12Glu、p.Gly13Cys、p.Gly13Asp、p.Glu37dup、p.Gly60Asp、p.Gly60Val)は、それぞれ数名の患者で認められた(Aoki et al 2005, Estep et al 2006, Gripp et al 2006a, Kerr et al 2006, Gremer et al 2010, Gripp et al 2015, Bertola et al 2017)。
2名の患者でエクソン3に病的ミスセンスバリアントが同定された:p.Thr58Ile(Gripp et al 2008)、p.Glu63Lys(van der Burgt 2007)。数名の患者でエクソン4にバリアントが同定された:ひとつはp.Lys117Arg(Kerr et al 2006)で、3つは146番目のアミノ酸に影響するバリアントでp.Ala146Thr(Zampino et al 2007)、p.Ala146Val(Gripp et al)、p.Ala146Pro(Chiu et al 2016)であった。
HRASはよく知られたがん遺伝子で、その異常な活性化は体細胞系列の孤発腫瘍でしばしば認められる。したがって、生殖細胞系列の病的を持つ患者において腫瘍の頻度が高いことは驚くに当たらない 。Kerrら(2003)の研究によれば、コステロ症候群の横紋筋肉腫でみられた11p15.5のヘテロ接合性の消失(loss of heterozygosity)は、正常型アレルの喪失が腫瘍発生のセカンドヒットであることを示唆している。この仮説を支持するものとして、Estepら(2006)によって示された横紋筋肉腫における正常アレルの消失や、Aokiら(2005)によって報告された腫瘍における単一アレル性発現(線維芽細胞では認められない)がある。
表6 厳選されたHRASの病的バリアント
| DNA塩基変化 | 予測されるタンパクの変化 | 検出頻度(症例数1) | 対照となる塩基配列 |
|---|---|---|---|
| c.34G>A | p.Gly12Ser | 81.3%(113) | NM_005343.2 NP_005334.1 |
| c.34G>T | p.Gly12Cys | 2%(3) | |
| c.34G>C | p.Gly12Ala | 7.2%(10) | |
| c.35_36delGCinsTT | p.Gly12Val | 1.4%(2) | |
| c.35_36delGCinsAA | p.Gly12Glu | <1%(1) | |
| c.37G>T | p.Gly13Cys | 1.4%(2) | |
| c.38G>A | p.Gly13Asp | 1.4%(2) | |
| c.64C>A | p.Gln22Lys | <1%(1) | |
| c.110_111+1dupAGG2 | p.Glu37dup | <1%(1)2 | |
| c.108_110dupAGA2 | p.Glu37dup | <1%(1)2 | |
| c.173C>T | p.Thr58Ile | <1%(1) | |
| c.179G>A | p.Gly60Asp | 4例 脚注3参照 | |
| c.179G>T | p.Gly60Val | 2例 脚注3参照 | |
| c.187G>A | p.Glu63Lys | <1%(1) | |
| c.350A>G | p.Lys117Arg | <1%(1) | |
| c.436G>A | p.Ala146Thr | <1%(1) | |
| c.436G>C | p.Ala146Pro | 1例 脚注3参照 | |
| c.437C>T | p.Ala146Val | <1%(1) |
表に列挙されたバリアントは著者から提供されたもので、GeneReviewのスタッフが独自にバリアントの分類を点検したものではない。GeneReviewは、Human Genome Variation Society (varnomen.hgvs.org)の標準的命名規則に従っている。
- 特記されているもの以外は、Sol-Church & Grippによって報告されたHRAS病的バリアントを有する患者数(総数=139)。
- Gremerらによる報告(2010)
- 2010年以降、このGeneReviewでの検討後に報告された
正常遺伝子産物
RASがん遺伝子であるHRAS,KRAS,NRASは21-kdのタンパクをコードし、p21RASと総称される。p21RASタンパクは細胞内膜に局在し、GDPおよびGTPに結合して弱い内因性GTPase活性を有する(Corbett & Alber 2001)。GTPに結合した形態は、RAS分子の非活性化状態である。細胞外からの刺激により(例えば成長因子受容体を通じて)、GDPを放出しGTPと結合する。GTPと結合した形は活性型で、シグナル伝達を行う。細胞分裂や成長を促進するこのシグナル伝達によって、種々の細胞で発現しているRASタンパクが、細胞増殖、分化、形質転換、アポトーシスを制御することができる。
結合したGTPがGDPに加水分解されることにより、活性化状態が元に戻る。RASタンパクの弱い内因性GTPase活性は、GTPase活性化タンパク質(GAPs)やニューロフィブロミンタンパク(神経線維腫症Ⅰ型の項を参照)などのその他の制御因子を通じて増強される。正常では、ほとんどの細胞内p21RASはGDP結合非活性型の状態で存在している。
異常遺伝子産物
異常遺伝子産物について知られていることの多くは、がん研究から得られたものである。その理由は、コステロ症候群を引き起こす生殖細胞系列のHRASの一塩基置換変異が、コステロ症候群とは無関係な孤発性悪性腫瘍でみられる体細胞系列の一塩基置換変異と同一のためである。12,13,61番目のアミノ酸置換をおこす活性型一塩基変異は、悪性腫瘍で最も多くみられる。頻度は低いが、59,63,116,117,119,146番目のアミノ酸置換もみられる。これらの病的ミスセンスバリアントは異常タンパク産物の恒常的な活性化を招き、その結果、Ras-MAPK経路(Sol-Church & Gripp 2009)とPI3K-AKT経路(Rosenberger et al 2009)のシグナル増強を起こす。より複雑なシグナル経路の制御異常が、稀なHRAS p.Gly60Aspバリアントで報告されている(Gripp et al 2015)。
アミノ酸の変化は、GTPase活性を減弱させ(アミノ酸残基12,13,59,61,63の場合)、そのため変異RASがん遺伝子タンパクが活性型のGTP結合状態のままとなったり、あるいは、塩基のアフィニティを低下させ、結合したGDPの細胞質GTPへの転換を促進する(アミノ酸残基116,117,119,146の場合)。一塩基置換変異は活性型RAS-GTP複合体の蓄積を起こし、恒常的に活性化されたGTP結合RASタンパクの蓄積を促進することによって、持続的なシグナル伝達を引き起こす。
がんと良性腫瘍
成人における悪性固形腫瘍(膀胱がんや肺がんを含む)は、しばしば体細胞系列の病的HRASバリアントを伴っているが、これらのバリアントは生殖細胞系列には存在しない(Giehl 2005)。このような場合、腫瘍への易罹患性は遺伝しない。体細胞変異のホットスポットは、アミノ酸残基12と13のグリシンおよび残基61のグルタミンである。これらのコドンにおける病的ミスセンスバリアントは遺伝子産物の活性増強を引き起こす。
更新履歴:
-
GeneReviews著者: Karen W Gripp, MD, FAAP, FACMG, Katheline A. Rauen, MD, FAAP, FACMG
日本語訳者:阿部裕,青木洋子(東北大学大学院医学系研究科 遺伝医療学分野)、松原洋一 (国立成育医療研究センター)GeneReviews最終更新日: 2019.8.29. 日本語訳最終更新日: 2021.6.23.[ in present]