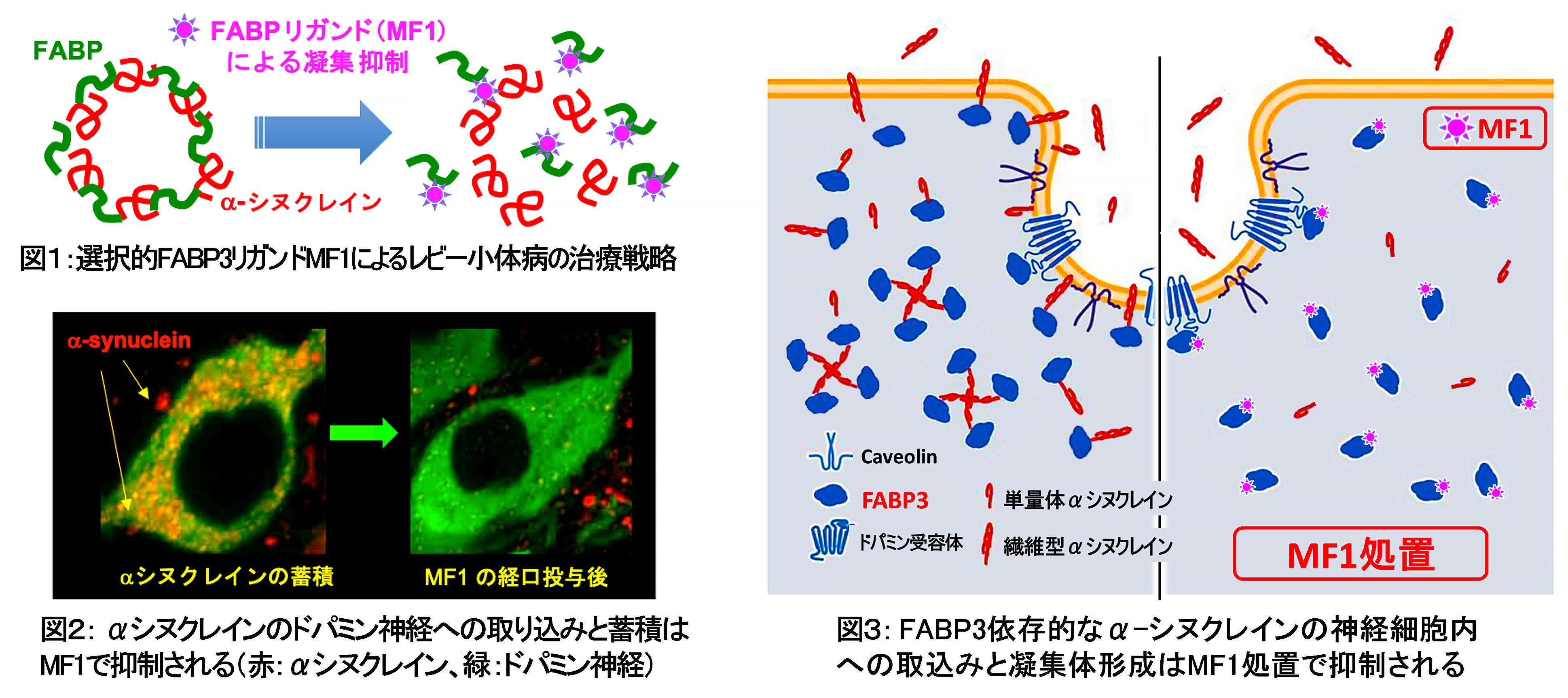
1.脂肪酸結合タンパク質を標的としたレビー小体病の治療薬開発
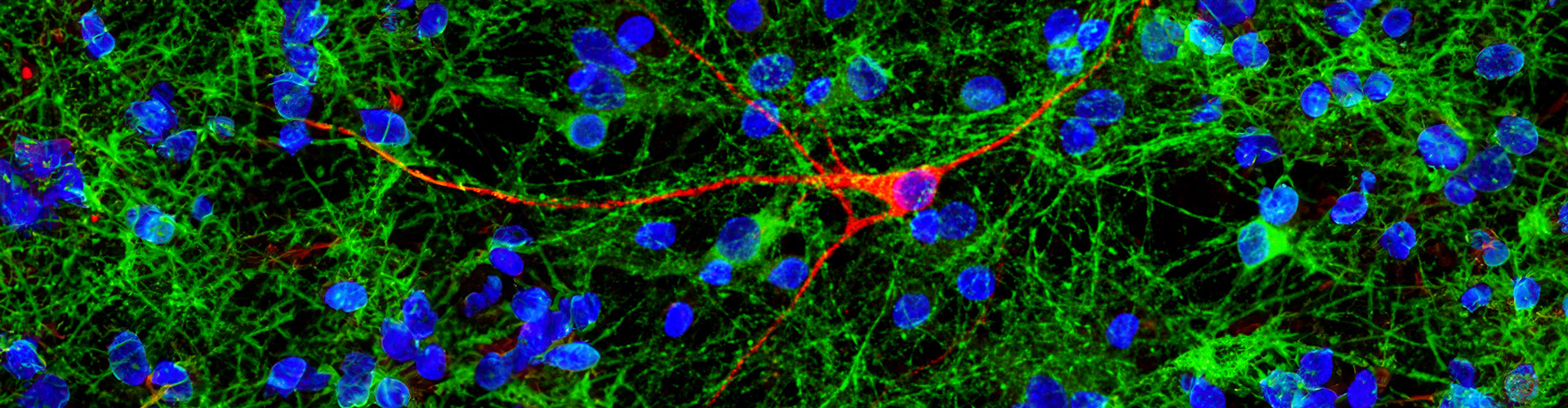
これまでに私たちは脂肪酸結合タンパク質(FABP)をターゲットとした数々のリード化合物の創出に成功し、レビー小体病の原因タンパク質でαシヌクレインの細胞内凝集を予防することに成功しました。FABPには多くの種類があり、神経細胞のほかグリア細胞、オリゴデンドロサイト等、様々な細胞に発現しています。これらの細胞特異的なリガンドを創製し、根本予防・治療薬の開発に取り組んでおります。対象疾患はパーキンソン病、レビー小体型認知症、パーキンソン病認知症、多系統萎縮症で、まずFABP3リガンド(WO2017171053 A1)が2025年3月に前臨床試験を完了し、2026年度より臨床試験を開始する計画です。
*令和4年度 「橋渡し研究プログラム(シーズB)」の採択課題(国立研究開発法人日本医療研究開発機構 - AMED)
*令和7年度 「橋渡し研究プログラム(シーズC)」の採択課題(国立研究開発法人日本医療研究開発機構 - AMED)
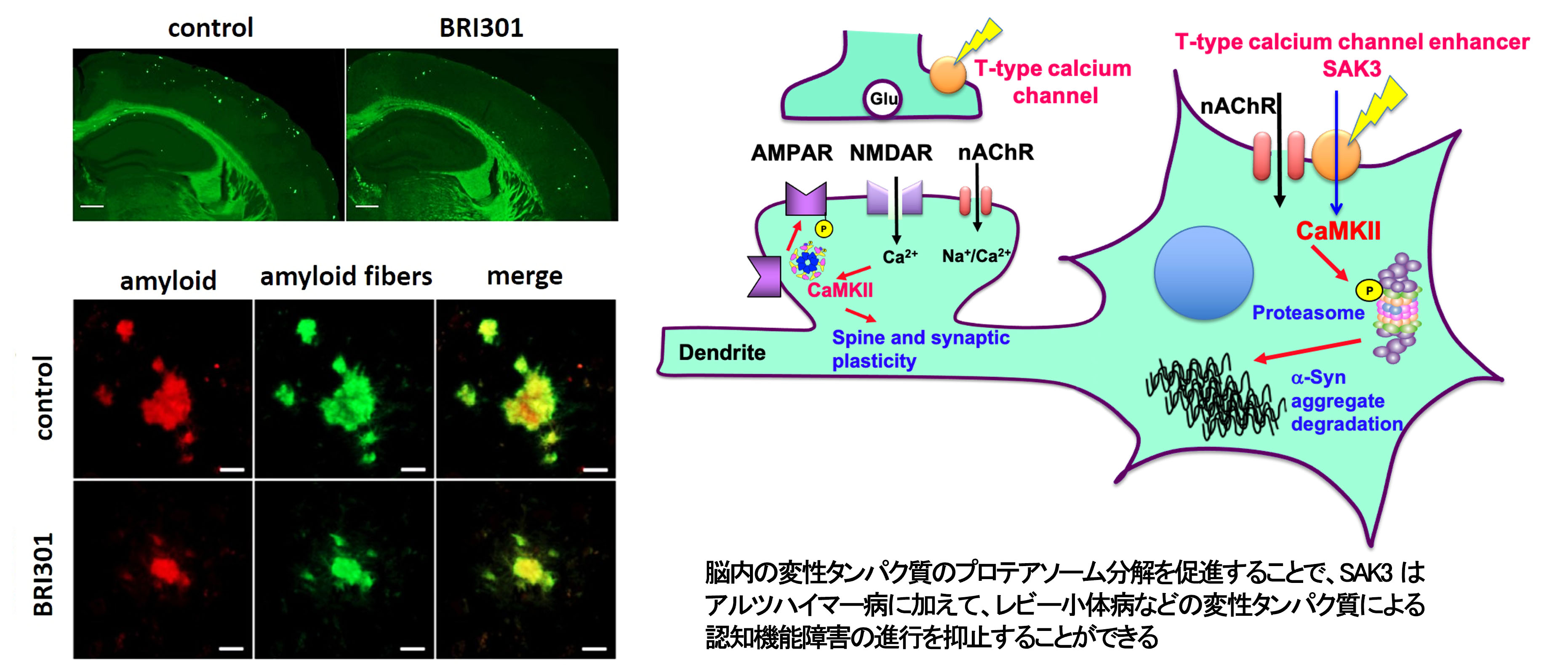
2.プロテアソームを標的としたアルツハイマー病の治療薬開発
変性タンパク質を分解する装置プロテアソームを活性化して、神経細胞内の変性タンパク質を除去することを新たに発見しました。さらに、SAK3 が神経細胞のプロテアソームを活性化して変性タンパク質の分解を促進する機構を明らかにしました。本研究成果は、アルツハイマー型認知症の原因となるアミロイドベータタンパク質やタウタンパク質、パーキンソン病やレビー小体型認知症の原因タンパク質であるαシヌクレイン、ハンチントン病で蓄積するハンチンチンなどの変性タンパク質の分解を促進して、神経細胞死を防ぐことにつながり、これらの疾患の治療応用が期待されます。
*東北大学プレスリリース - http://www.pharm.tohoku.ac.jp/file/information/20210629.pdf
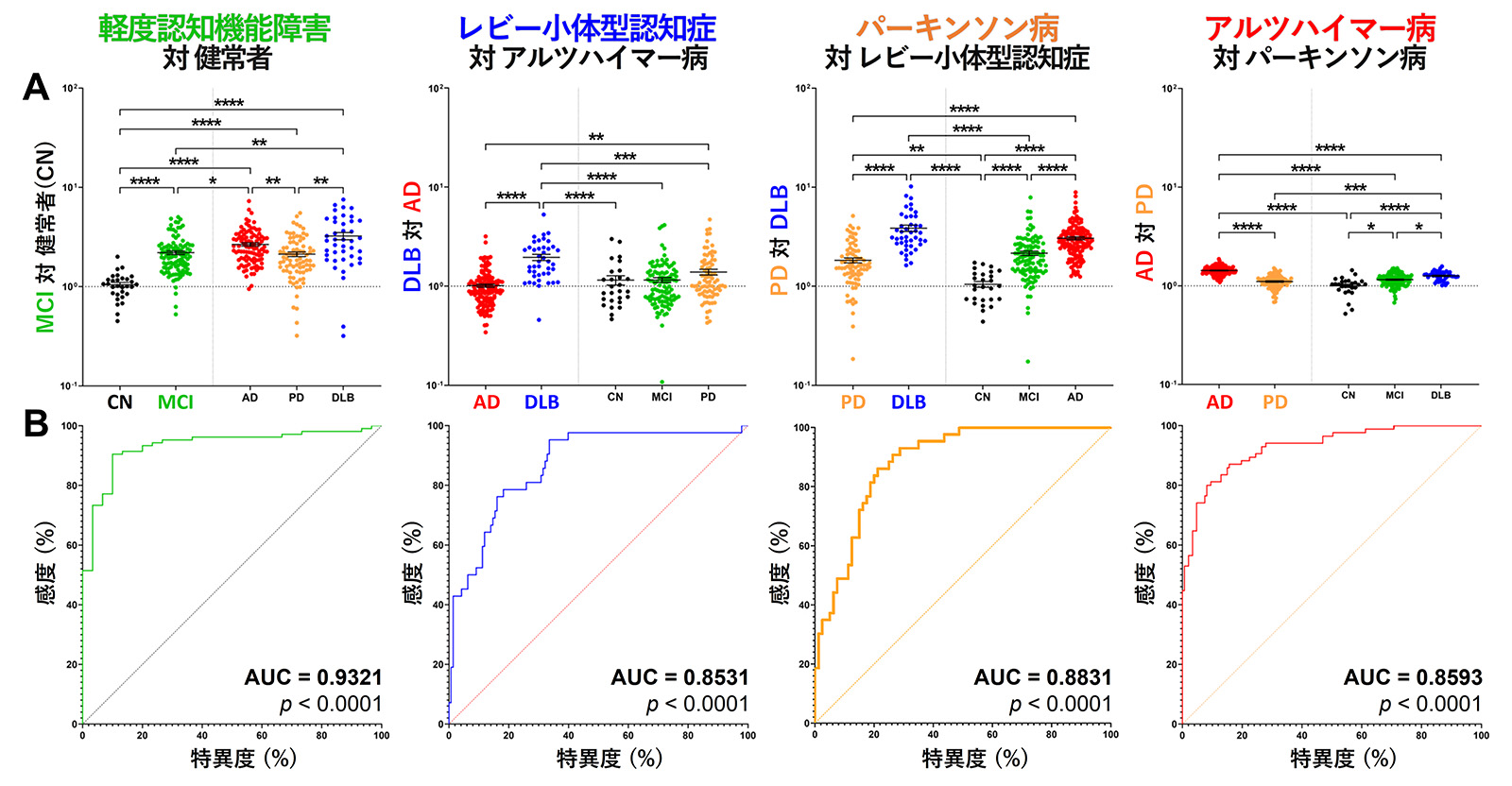
3.レビー小体型認知症・パーキンソン病の超早期診断技術の開発
最近わたしたちはレビー小体病の独自バイオマーカーと定量化技術の開発に成功しました(特許出願2021-012620、WO2022163818 A1)。この技術により、レビー小体型認知症、パーキンソン病をはじめ、アルツハイマー病を精度よく鑑別することが可能であり、発症前における認知・運動疾患の診断応用が期待されます。また上記の治療薬対象となる患者様を精度よくスクリーニングできるため、臨床試験と治療効果の精度を高めることが可能です。
プレスリリース:脳疾患の新規予測・鑑別技術 ~ 認知症の超早期診断に期待
→https://www.tohoku.ac.jp/japanese/2023/09/press20230925-03-ad.html
→http://www.pharm.tohoku.ac.jp/file/information/20230925.pdf
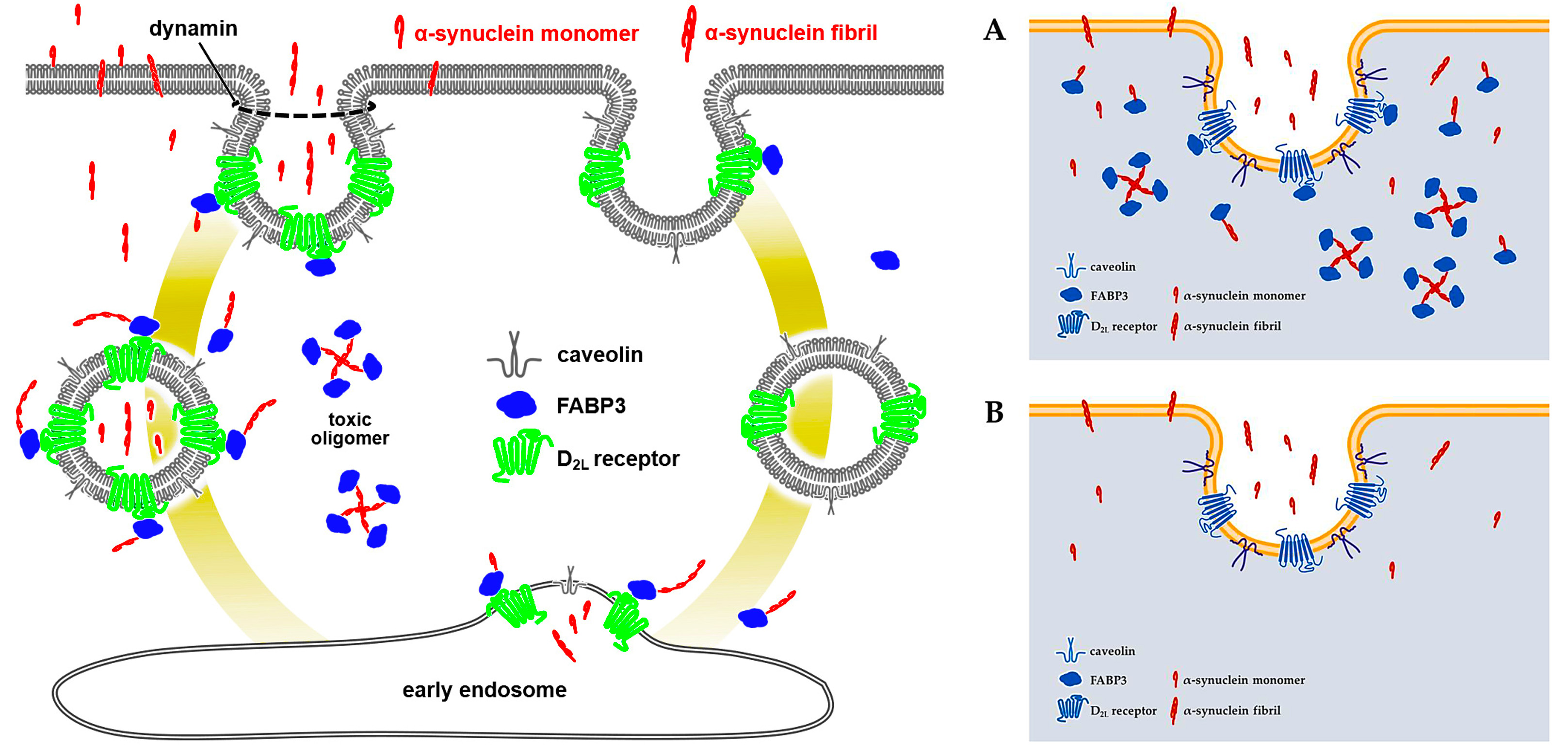
4.レビー小体病の発症メカニズムとαシヌクレインの伝播機構の解明
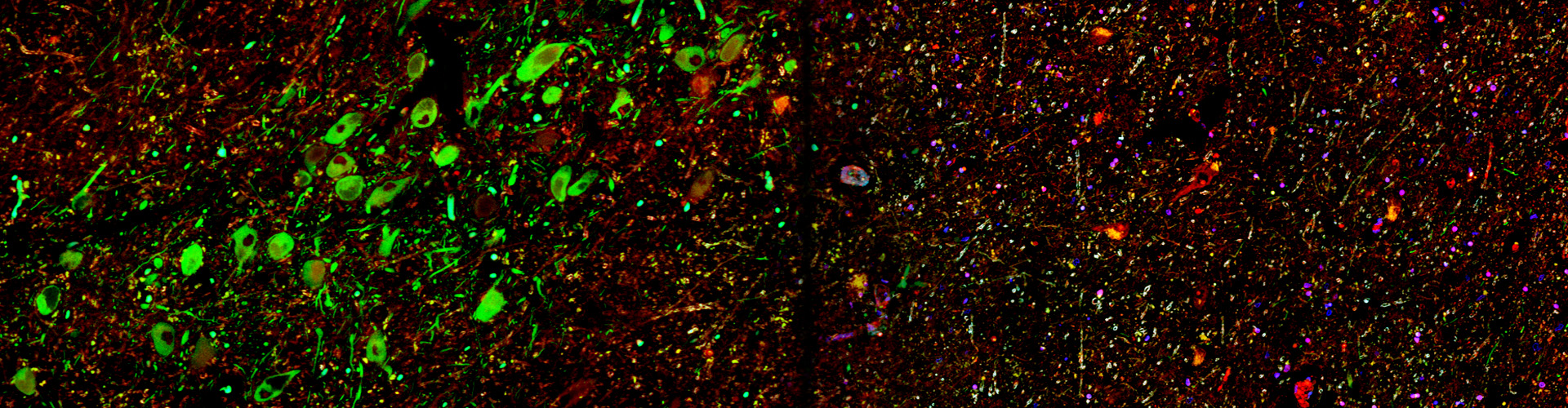
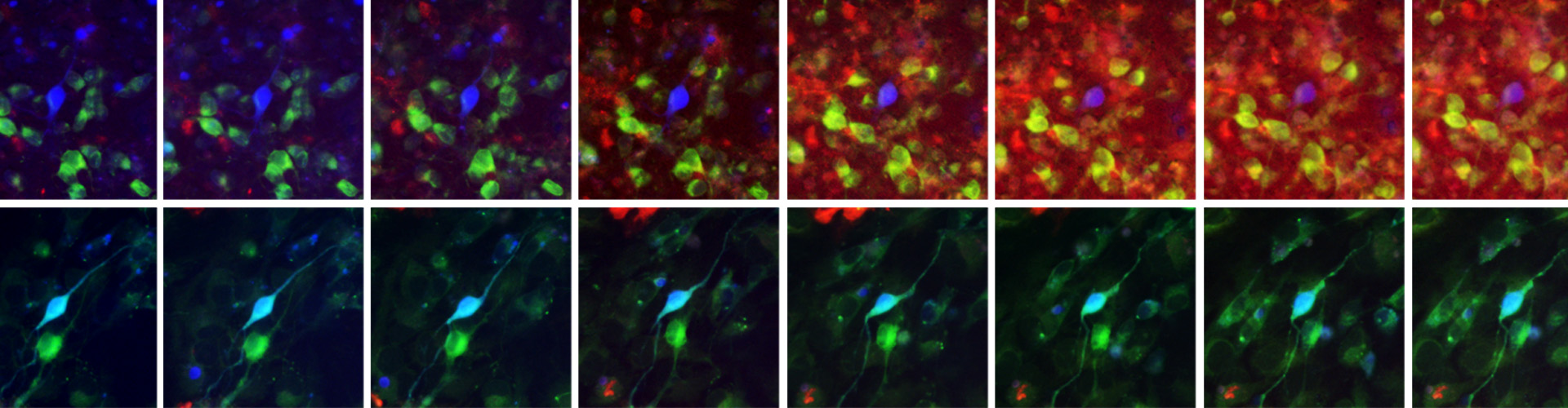
レビー小体病の原因タンパク質であるαシヌクレインは体を伝播し脳内に蓄積することが病気の原因と考えられています。私たちはこのαシヌクレインが脂肪酸結合タンパク質FABP3と様々な細胞膜表面の受容体と相互作用し、細胞内に取り込まれる新たなメカニズムを明らかにしました。またこの現象はドーパミンの生合成に重要なチロシン水酸化酵素の消失につながることを明らかにしました。αシヌクレインの伝播そのものを根本的に抑制し、レビー小体病を予防可能な治療薬の開発も行っています(特許出願2020-127958, WO/2022/024693 A1)。
*Kawahata I, Fukunaga K. Impact of fatty acid-binding proteins and dopamine receptors on α-synucleinopathy. J Pharmacol Sci. 2022 Feb;148(2):248-254. doi: 10.1016/j.jphs.2021.12.003. Epub 2021 Dec 14.
5.レビー小体病理と腸脳相関の分子メカニズムの解明
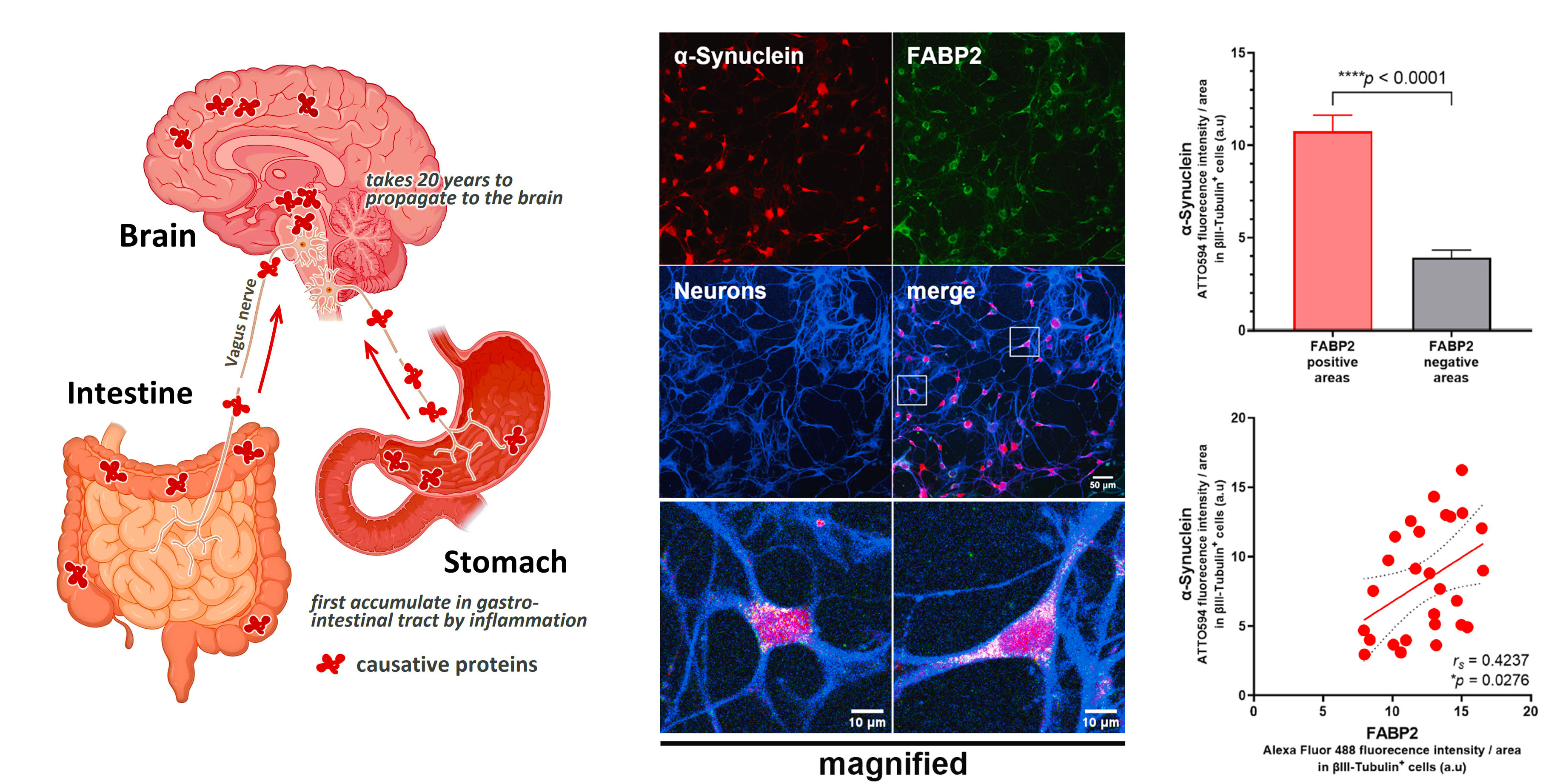
私たちの研究では、腸内に存在する脂肪酸結合タンパク質FABP2が、パーキンソン病などの「シヌクレイノパチー」の進行に関与する可能性を検討しています。特に、腸内神経系での異常なαシヌクレインの蓄積メカニズムに注目し、動物実験や患者血液中のタンパク質濃度解析を通じて、FABP2の役割を明らかにしました。これにより、疾患の早期発見や進行予測に寄与する新しいバイオマーカーとしての可能性が示唆されています。
Sekimori T, Fukunaga K, Oizumi H, Baba T, Totsune T, Takeda A, Sasaki T, Kawahata I*, FABP2 is Involved in Intestinal α-Synuclein Pathologies. J Integr Neurosci 2024 Feb 22;23(2):44. doi: 10.31083/j.jin2302044.
6.遺伝性神経疾患・小児疾患の原因遺伝子解析と発症機構の解明
私たちは遺伝性変性疾患、とくに小児性遺伝性疾患であるドーパ応答性ジストニア(瀬川病)や遺伝性パーキンソン病を中心に、神経学の理解を深めるための遺伝子解析を行っています。