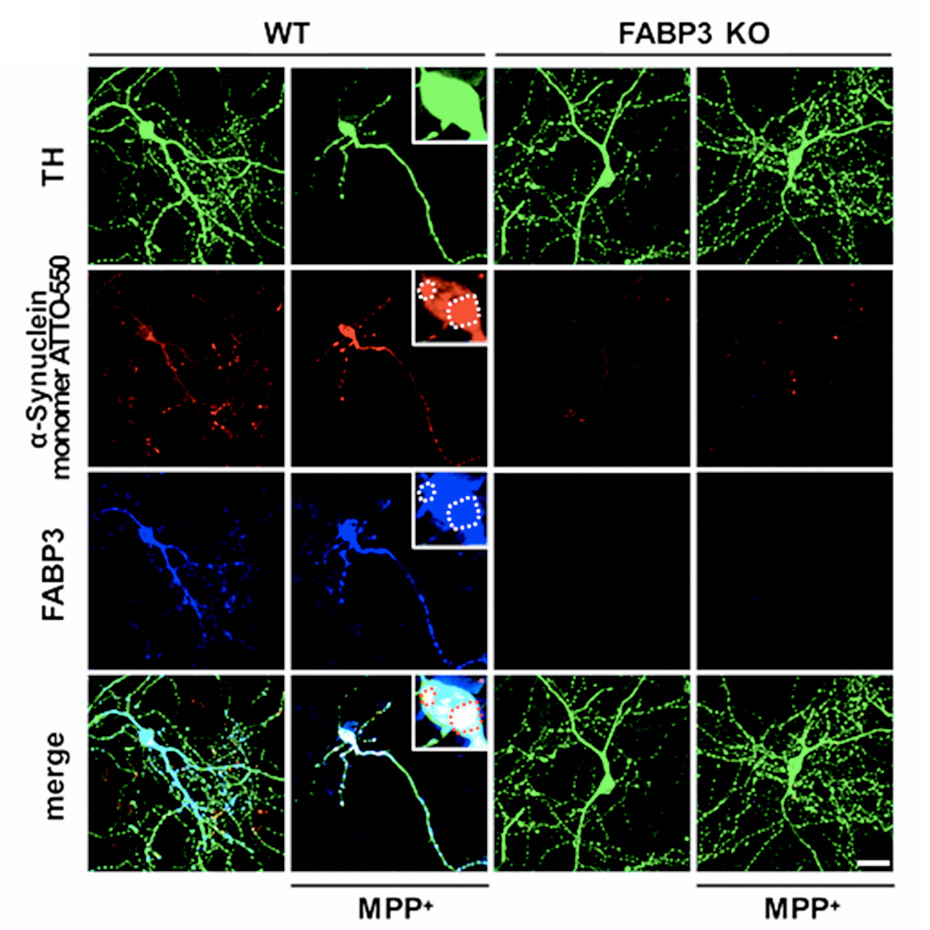
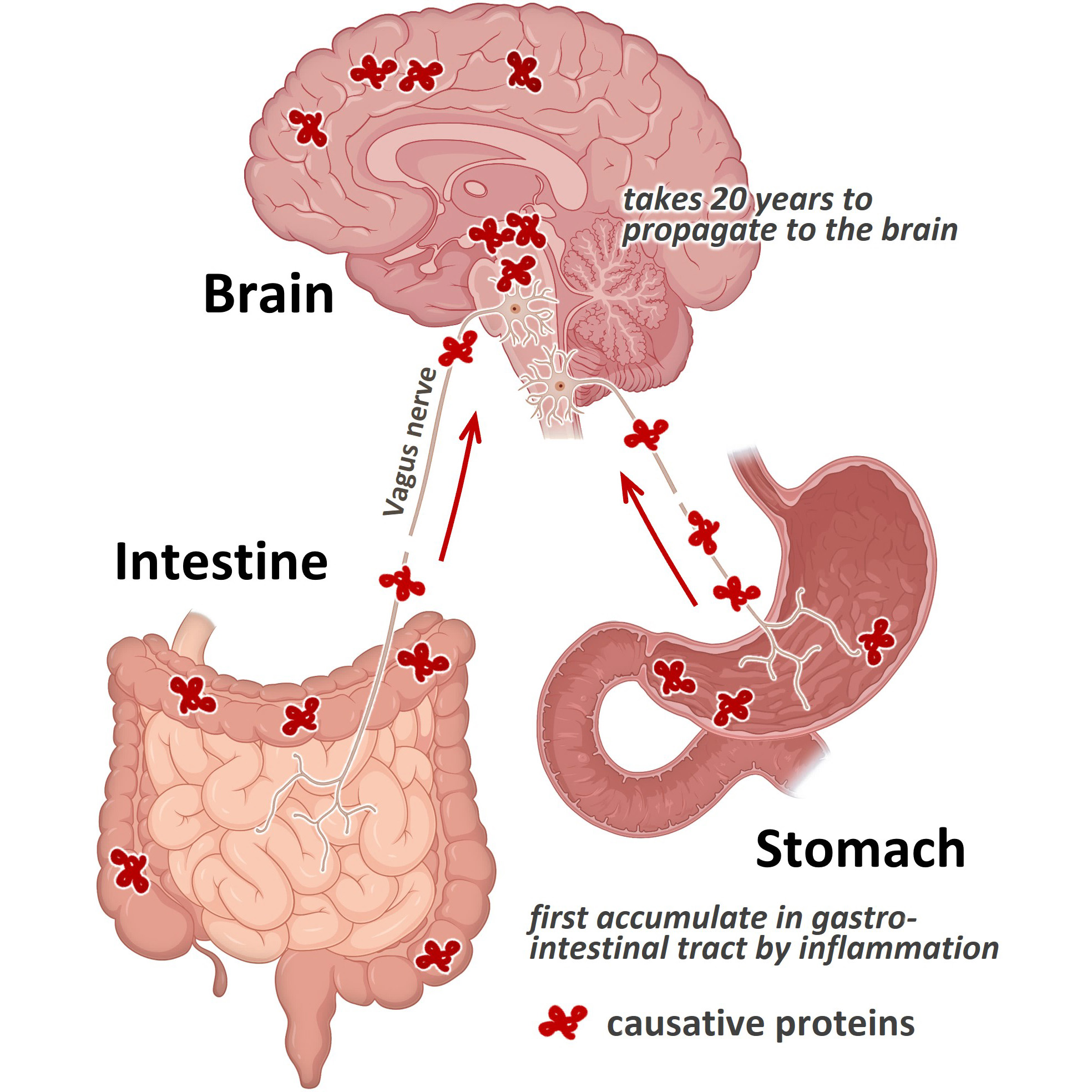
病態解明

早期予測
根本治療
神経変性疾患を克服する先進脳創薬
この度は、私どもの研究開発に多大なるご関心をお寄せいただき、誠にありがとうございます。連日、数多くのお問い合わせをいただいており、皆様の切実な思いを一通一通、大切に拝見しております。
現在の状況について、ご説明させていただきます。私どもは2026年度から治験を開始することを目指しております。しかしながら、治験には定められた手順があります。まず健常者の方々での安全性を十分に確認する必要があります(第I相試験)。ヒトで一定の安全性が確認された場合には、次の治験(第II相試験)として患者様に治験薬(試験的に用いる未承認の候補化合物)を投与して有効性の有無や程度を確認します。そのため、実際に患者様にご参加いただけるのは、早くても2027年度以降となる見込みです。
治験は全国の研究分担機関で実施する計画を進めており、より多くの地域の患者様にご参加いただける機会をご提供できるよう準備を進めております。治験審査委員会で承認され、医薬品医療機器総合機構において治験計画届が受理されましたら、jRCT(https://jrct.mhlw.go.jp)にて治験の概要を公表いたします。治験実施機関につきましても、当該ホームページにて公表いたします。参加方法や募集要項などの詳細につきましては、各実施医療機関における規定に従って告知させていただきますので、今しばらくお待ちいただけますと幸いです。
皆様からいただいた貴重なお声は、私どもの研究開発を進める大きな力となっております。しかしながら現時点では、個別のお問い合わせすべてに研究代表者がお返事することが難しく、お一人お一人のお気持ちに応えられず大変心苦しく存じます。私どもは、一日も早く研究開発を進め、関連分野の企業や研究機関との連携の可能性を検討しつつ、チーム一同、全力で取り組んでまいります。皆様の期待に応えられる日が一日も早く訪れますよう、誠心誠意努力してまいります。引き続き、温かく見守っていただけますと幸いでございます。
※2026年4月より、研究代表機関が公立大学法人静岡県立大学に変更となります(研究代表者の所属変更に由る)。本研究プロジェクト自体に変更はございません。ご心配をおかけし大変申し訳ございません、ご理解のほど何卒よろしくお願い申し上げます。
本研究プロジェクトは、国立研究開発法人日本医療研究開発機構(AMED)および国立研究開発法人科学技術振興機構(JST)のご支援をいただき実施しております。