線維性骨異形成症/McCune-Albright症候群
(FibrousDysplasia/McCune-AlbrightSyndrome)
[Synonyms:FD/MAS]
Gene Reviews著者: AlisonMBoyce,MD,PabloFlorenzano,MD,LuisFdeCastro,PhD,andMichaelTCollins,MD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2019.6.27. 日本語訳最終更新日: 2023.4.23.
原文: FibrousDysplasia/McCune-AlbrightSyndrome
要約
疾患の特徴
線維性骨異形成症/McCune-Albright症候群(FD/MAS)は、胚初期においてGNAS(cAMP経路関連Gタンパク質、Gsαをコードする)に体細胞性の接合後機能亢進型病的バリアントが生じることで発生する疾患で、皮膚・骨格・一部の内分泌器官に病変が現れることを特徴とする。ただし、Gsαシグナル伝達は遍在性であるため、それ以外の組織にも影響が現れることがある。
出生時あるいは出生後ほどなく現れる皮膚のカフェオレ斑が多くの例でみられ、これが本疾患で最初に出現する症候である場合が多い。線維性骨異形成(FD)は、頭蓋顔面・軸骨格・付属肢骨格のいずれでも、また、これらのどういった組合せでも生じる可能性があり、その範囲も、単発性で無症状の単骨性病変が何かの機会にたまたま見つかるといったものから、実質的にすべての骨格に発生し、進行性の脊柱側彎、顔面変形、歩行機能・視力・聴力の喪失といった重度の障害をもたらす多骨性病変に至るまで、大きな幅がみられる。
内分泌障害としては、次のようなものがある。
- 女児では反復性卵巣嚢腫、男児では自律性テストステロン産生に起因して生じるゴナドトロピン非依存性思春期早発症
- ゴナドトロピン非依存性思春期早発症を伴うことのある精巣病変
- 非自己免疫性甲状腺機能亢進症を伴うことのある甲状腺病変
- 成長ホルモン分泌亢進
- 線維性骨異形成に関連する低リン酸血症を伴うことのあるFGF23媒介性リン酸塩喪失
- 新生児高コルチゾール症
FD/MAS罹患者の予後は、疾患の部位と重症度によって決まってくる。
診断・検査
大多数の例については、特徴的臨床症候が2つ以上みられることを根拠として、FD/MASの診断が下される。臨床所見が単骨性線維性骨異形成症のみにとどまる場合は、分子遺伝学的検査にてGNASに体細胞性の機能亢進型病的バリアントが同定されることが診断確立の要件となる。バリアントの検出のされやすさは、組織中のモザイクのレベル、ならびに使用する手法の感度により変わってくる。
臨床的マネジメント
症状に対する治療:
専門家で構成された多職種チームによる管理が最も効果的である。
- 線維性骨異形成:骨折や変形(脊柱側彎など)といった病的状態を最小限に抑え、機能を最大限に引き出すことが管理の中心となる。
- 思春期早発症:骨年齢の亢進と成人期の低身長を防止する治療を行う。女児については、アロマターゼ阻害薬であるレトロゾールが用いられる。男児については、治療法の確立には至っていない。
- 甲状腺疾患:甲状腺機能亢進に対してはメチマゾールが効果的ではあるものの、甲状腺機能亢進は持続性であるため、甲状腺切除術が多く用いられる。
- 成長ホルモン分泌亢進:内科的治療が第一選択となる。具体的には、オクトレオチドと、成長ホルモン受容体拮抗薬であるペグビソマントを単独使用あるいは併用することになる。
- 高コルチゾール症:治療は、新生児Cushing症候群の症状の現れ方により変わってくる。
定期的追跡評価:
線維性骨異形成症/McCune-Albright症候群(FD/MAS)
以下に関するモニタリングを行う。
- 新生児:高コルチゾール症の臨床的徴候
- 全小児:成長の加速をはじめとする思春期早発症や成長ホルモン分泌亢進を窺わせる臨床的徴候
- 小児
- 5歳未満:甲状腺機能異常
- 超音波検査で甲状腺に異常がみられるものの、甲状腺機能には異常がみられない例:甲状腺機能に関する定期的モニタリング
- 男性:精巣の病変(身体の直接診査と精巣超音波検査)
- 以下を使用している例
- ペグビソマント:肝毒性
- ソマトスタチンアナログ製剤:胆嚢疾患の徴候ならびに症候
- 女性:乳癌(一般集団でモニタリングが推奨される年齢より若年で行う)
線維性骨異形成(FD)
- 定期的にX線写真を撮影して、既存のFDのモニタリングに加えて、新規にFDが発生していないかチェックを行う。
- 定期的に血清リン濃度(低リン酸血症の発生に備えて)、ならびに25ヒドロキシビタミンD値を測定する。
- 頭蓋顔面のFDについて:視覚と聴覚の評価を毎年、頭蓋骨のCTを定期的に、通常の血清IGF-1値の測定を成人初期まで継続的に行う。
- 脊椎のFD:進行性脊柱側彎に関するモニタリングを綿密に行う。
避けるべき薬剤/環境:
- コンタクトスポーツその他の高リスクの活動(骨格病変が顕著にみられる例)
- 予防的な視神経減圧術(頭蓋顔面のFDを有する例)
- 卵巣嚢腫の外科的切除
- FDに対する治療としての放射線療法
- 悪性腫瘍に関しリスク要因となるもの(例えば、放射線被曝)
遺伝カウンセリング
FD/MASは遺伝性疾患ではない。FD/MAS罹患児の親が、この疾患に特徴的な症候をはっきりした形で有していた例は、これまでに報告されていない。同胞の有するリスクも、一般集団と同レベルと考えられる。FD/MASの垂直伝播が確かめられた例はない。
診断
線維性骨異形成症/McCune-Albright症候群(FD/MAS)は、通常、臨床的根拠に基づいて診断が行われる。ただ、今のところ正式な診断基準は公表されていない。
本疾患を示唆する所見
以下のような皮膚・骨格・内分泌症候をいずれかでも有する例は、FD/MASを疑う必要がある。
皮膚
罹患者には、特徴的カフェオレ斑がみられることがある。
- 辺縁はギザギザで不規則、しばしば「メイン州の海岸線状」と形容される(ちなみに、神経線維腫症1型でみられる病変は辺縁が平滑で、「カリフォルニア州の海岸線状」と評される)。
- 斑の分布には身体の正中線が(「尊重される形で」)関連しており、胚細胞の移動パターンを反映するBlaschko線に沿う形で現れる(図1参照)。
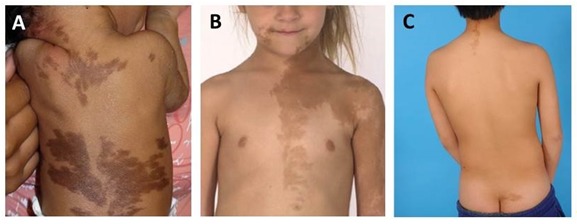
図1:カフェオレ状の皮膚の色素沈着
A.新生児にみられた皮膚病変。
身体の正中線との特徴的な関連を示し、分布は胚期の細胞移動(発生期のBlaschko線)のパターンを反映したものとなっている。
B.胸、顔、腕にみられた典型的病変。
辺縁は「メイン州の海岸線」状を呈し、身体の正中線との関連がみられる。発生期のBlaschko線に従った分布を示す。
C.後頸部や臀部の割れ目の部分に多くみられる典型的病変。
骨格
線維性骨異形成(FD)とは、正常な骨や骨髄が線維骨性組織に置き換わる状態をいい、その結果、骨折・変形・機能障害・疼痛などのリスク上昇を招く。
- FDは、単骨性(病変が1つの骨にのみみられるもの)と多骨性(病変が複数の骨に及ぶもの)に分類される。
- FDの病変は、頭蓋顔面・軸骨格・付属肢骨格のいずれの部位にも生じ、またこれらがどのように組み合わさった形でも生じうる(図2参照)。
- FDの最初の時点の放射線評価は、99Tc-MDP骨シンチグラフィーを含むものとすべきである。
- シンチグラフィーで明らかになった骨格病変部位については、その位置と範囲に応じ、X線写真や頭部CTで、さらに詳しい評価を行う。
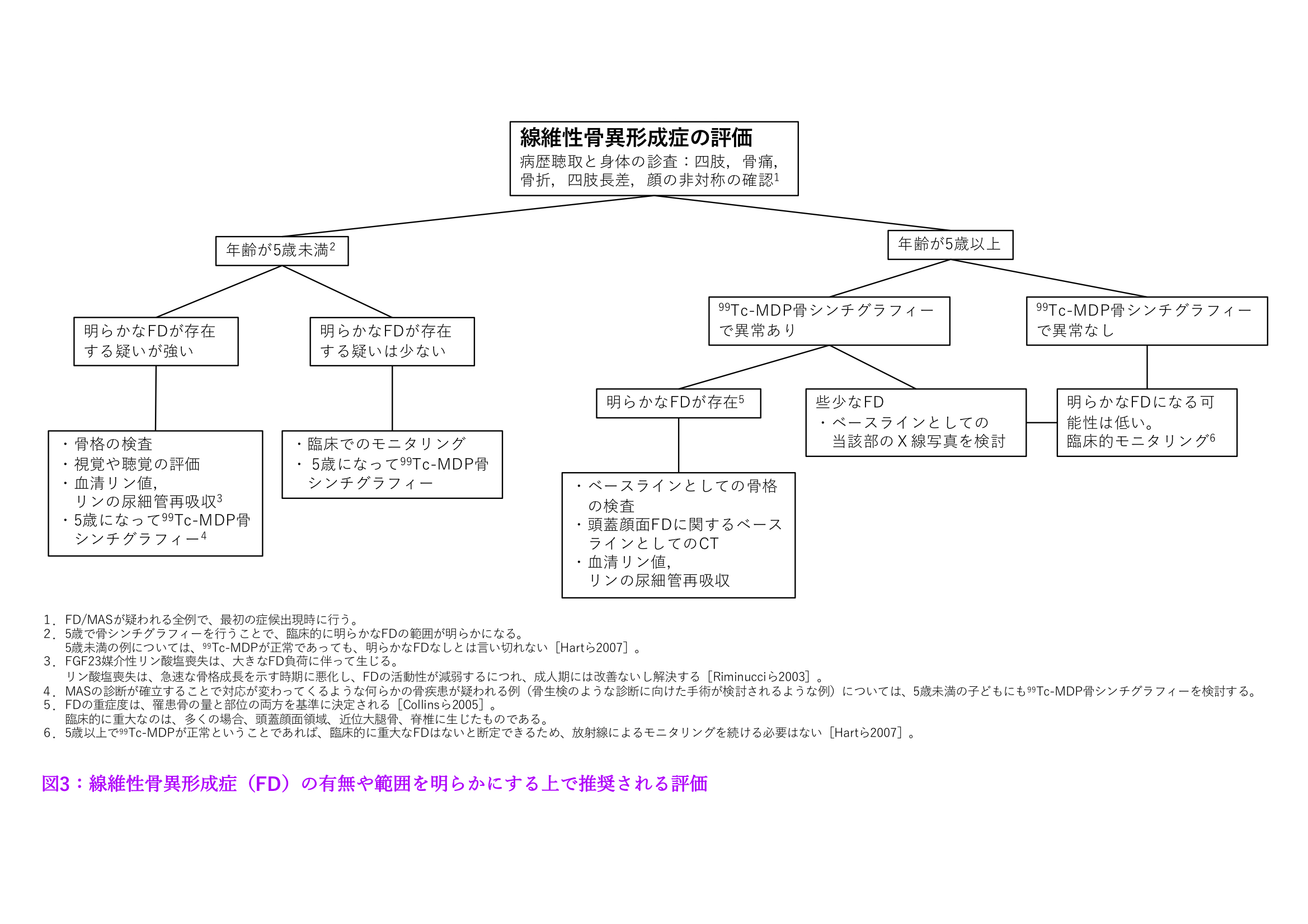
- FDの診断に用いられる評価法については、図3を参照されたい。
図2:線維性骨異形成症(FD)
A.近位大腿骨にみられたFD。
典型的な擦りガラス様外観を呈し、内反股変形(羊飼いの杖変形)を伴っている。
B.頭蓋顔面のFDを有する26歳男性のCTの3D再構成画像。
成長ホルモン分泌亢進に対するコントロールがなされておらず、大頭症と重度の顔面変形に至っている。
C.10歳女児のCT画像。
頭蓋顔面のFDが、若年者に特徴的な擦りガラス状の外観を呈する。
視神経管はFD内に包み込まれた状態(白矢印)ではあるが、視覚障害は伴わなかった。
D.40歳女性のCT画像。
頭蓋顔面のFDが、年長の罹患者に特徴的な、より硬化の進行した固形部分と嚢胞様部分が混在した外観を呈している。この例でも、視神経管がFD内に包み込まれた像(白矢印)がみられるものの、やはり視覚障害は伴わなかった。
E.左右に並べて示したのは、それぞれ、99Tc骨シンチグラフィーの後-前位像と前-後位像である。モザイク様の発現パターンに一致した形で、矢印で示した頭蓋骨・肋骨・大腿骨・脛骨等の骨格罹患部位にトレーサーが斑状に取り込まれていることが確認される。
図3:線維性骨異形成症(FD)の有無や範囲を明らかにする上で推奨される評価
内分泌
内分泌所見として、以下のようなものがみられる場合がある。
- ゴナドトロピン非依存性思春期早発症。
- 特徴的な超音波所見を伴うLeydig細胞やSertoli細胞の過形成をはじめとする精巣病変(図4B参照)。時として、これに関連するゴナドトロピン非依存性思春期早発症を伴うことがある。
- 特徴的な超音波所見を伴う甲状腺病変(図4Cならびに4Dを参照)。これは、時として非自己免疫性甲状腺機能亢進症を伴うことがある。
- 成長ホルモン分泌亢進
- 時として低リン酸血症を伴う線維芽細胞増殖因子23(FGF-23)関連リン低下。
- 新生児高コルチゾール症
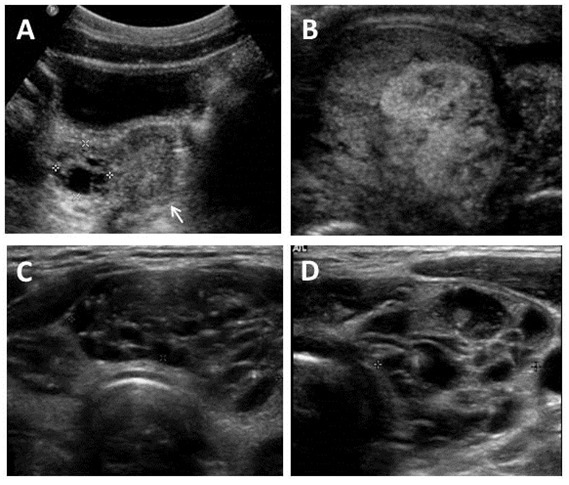
図4:超音波検査
A.7歳女児の骨盤超音波像。
片側性の複雑卵巣嚢腫(クロスハッチ印で範囲を示した)がみられる。子宮は思春期前の大きさである(矢印)。
B.成人の精巣超音波像。
固体成分と嚢胞成分が入り混じった異質性の様相を示す。
CならびにD.甲状腺にみられる特徴的超音波所見。
異質性を示し、嚢胞状(スイスチーズ様)外観を呈する。
診断の確定
FD/MASの診断は、FD/MASの特徴的臨床症候を2つ以上有することをもって確定する。単骨性線維性骨異形成症が唯一の臨床所見である例については、GNASに体細胞性の機能亢進型病的バリアントが同定されることが診断確立の要件となる(表1参照)。分子遺伝学的検査のアプローチとしては、p.Arg201とp.Gln227のコドンに関する標的型解析がある。PCRシーケンシングベースの診断手法を用いる場合には、可能なら病変組織のサンプルを用いるのが最も臨床的感度の高い解析法である。
- 病変組織では80%近く。
- 末梢血リンパ球では20%-30%近く。
注:(1)バリアントが検出されるかどうかは、組織中のモザイクのレベル、ならびに解析手法の感度により変わってくる。標準的なPCRを用いたときのp.Arg201のバリアントの検出割合は、内分泌器官が最も高く、罹患皮膚標本で最も低い値を示す[Lumbrosoら2004]。モザイクに関する検出能力が、アッセイの検出率に影響を及ぼすことになる(表1ならびに表4を参照)。
(2)標的型の解析としては、GNASのエクソン8と9のシーケンシングのみ行うことが考えられる。FD/MASにおいて、過去に報告されたもの以外のGNASのバリアントが検出されたとしても、それは意義不明バリアントと解釈されることになるはずである。
(3)Gsαは、ほぼすべての組織において、GNASの母性・父性の両アレル性発現である。ただ、GNASは座位的に複雑で、GNASのインプリンティングにより選択的転写産物や別の表現型が生じる可能性を有している(「遺伝子の上で関連のある疾患」と「分子遺伝学」の項を参照)。
表1:線維性骨異形成症/McCune-Albright症候群で用いられる分子遺伝学的検査
| 遺伝子1 | 方法 | 検出されるバリアント | その手法で病的バリアント2が検出される発端者の割合 |
|---|---|---|---|
| GNAS | 病変部生検によるエクソン8と9の標的型解析3,4 | p.Arg201His, p.Arg201Cys5,6 |
8%-90%7 75%-100%8 |
| p.Gln227Leu6 | 5%5 |
- 染色体上の座位ならびにタンパク質に関しては、表A「遺伝子とデータベース」を参照。
- この遺伝子で検出されているアレルバリアントの情報については、「分子遺伝学」の項を参照のこと。
- 標的型解析には配列解析が用いられる。配列解析を行うことで、benign、likelybenign、意義不明、likelypathogenic、pathogenicといったバリアントが検出される。バリアントの種類としては、遺伝子内の小欠失/挿入、ミスセンス・ナンセンス・スプライス部位バリアントなどがあるが、通常、エクソン単位あるいは遺伝子全体の欠失/重複については検出されない。配列解析の結果の解釈に際して留意すべき事項についてはこちらをクリック。
- 病変部の生検で得た検査標本は、血液標本より高い陽性率が得られる。血液サンプルでの検出率は20%-30%近くである[Lumbrosoら2004,Kalfaら2006]。
- FD/MAS罹患者におけるGNASの体細胞性ミスセンスバリアントは、p.Arg201(病的バリアントの95%超)[Lumbrosoら2004]、p.Gln227(5%未満)[Idowuら2007]の2つのうちの1つに限定した形で現れることがわかっている。
- 稀に、p.Arg201とp.Gln227にこれ以外のアミノ酸が置換することがある(「分子遺伝学」の項を参照)。
- バリアントの検出率は、その組織のモザイクのレベルと、用いる手法の感度により変わってくる。標準的なPCRを用いたときにp.Arg201にバリアントが検出される率は、内分泌器官で最も高く、罹患皮膚標本で最も低い[Lumbrosoら2004]。
- プライマーの変更(ペプチド核酸)[Biancoら2000]と次世代シーケンサー[Narumiら2013]の手法を組み合わせる[Narumiら2013]ことで、罹患組織では実質的に全例、白血球では75%の罹患者で、p.Arg201のバリアントが検出される可能性がある。
臨床的特徴
臨床像
線維性骨異形成症/McCune-Albright症候群(FD/MAS)は、cAMP経路関連Gタンパク質であるGsαをコードするGNASに体細胞性の機能亢進型病的バリアントが生じることで発生する疾患である。罹患組織は、外胚葉由来、中胚葉由来、内胚葉由来のいずれの組織にも生じうるが、多くの場合、皮膚、骨格、ある種の内分泌器官に生じる。ただ、Gsαシグナル伝達は実質的にすべての組織に存在するため、上記以外の組織に生じる可能性もある。
FD/MASの表現型のスペクトラムは、無症状で何かの機会にたまたま発見されるようなものから、新生児致死性のものまで、ばらつきがある。罹患組織の数、罹患の程度とも、罹患者間で非常に大きな幅がみられる。疾患の現れ方は、体細胞性の病的バリアントが出現した胚発生の時期、発生した組織、罹患組織におけるGsαの役割によって変わってくる。病的バリアントが発生初期に生じた場合は、疾患の範囲が広範囲に及び、発生後期に生じた場合は、その範囲が限られることになる。
色素斑
皮膚のカフェオレ斑が多くみられ、通常、これが本疾患で最初に現れる症候である。皮膚病変の大きさと疾患が及ぶ範囲との間、皮膚疾患の分布と線維性骨異形成が生じる部位との間には、特段の相関はみられない。
骨の線維性異形成
皮膚と同様、線維性骨異形成もモザイクのパターンを示し、頭蓋顔面、軸骨格、付属肢骨格のいずれの部位にも、またどういった組合せでも生じうる。病変が最も現れやすいのは、頭蓋底と大腿骨近位部である[Kellyら2008]。一般的に、中枢部に多く末梢部に少ないという勾配はみられるものの、病変が現れる骨の組合せには、あらゆる可能性がある。
線維性骨異形成は、単発性で無症状の単骨性病変がたまたま発見されるというものから、骨格全体に多骨性に病変が現れて、視覚、聴覚、移動能力が失われて障害を及ぼすような重度のものまで、広いスペクトラムをもった現れ方をする。
個々の骨病変は、通常、生後数年のうちに生じ、小児期を通じ拡大していく。臨床ではっきり認められる骨病変の大部分は、10歳までには検知可能な状態になる。15歳以降に新規に発生することは稀で、臨床ではっきり認められる骨病変が15歳以降に現れることはほとんどない[Hartら2007]。成人期になると、通常、線維性骨異形成の病変の活動性は低下するが、その背景として、病的バリアントを有する細胞のアポトーシスが関係しているように思われる[Kuznetsovら2008]。
線維性骨異形成(FD)の臨床症候や臨床経過は、病変の現れる骨格の部位や範囲により変わってくる。
- 付属肢骨格
- 付属肢骨格に線維性骨異形成を有する子どもは、通常、跛行、疼痛、病的骨折といった形で影響が現れる。
- 反復性の骨折と進行性の変形により、歩行困難となって移動能力が失われるようなこともある。
- 頭蓋顔面領域
- FDは、疼痛を伴わない「膨らみ」あるいは顔面非対称の形で現れる場合がある。
- 頭蓋顔面の病変が拡大することで、進行性の顔面変形に至る場合があり(図2B参照)、稀には(通常は成長ホルモン分泌亢進が絡む形で)、視神経や外耳道に影響が及ぶことで視覚や聴覚の喪失に至るような場合もある[Cutlerら2006,Boyceら2018]。
- 椎骨
- 椎骨にFDが現れることは多くあり、脊柱側彎に至る場合がある。そして稀には、重度で進行性となり、死亡に至るような場合もある[Leetら2004b]。
- 早期に病的状態をもたらすようなFDの症候はそれほど多くはないが、進行性の脊柱側彎は、未治療の場合、そうしたものの1つになる。
骨痛
骨痛は、線維性骨異形成の主たる合併症の1つである。骨痛はあらゆる年齢でみられるものの、多いのは、小児期には骨痛がなく、思春期に発現して成人期にかけて拡大するというパターンである[Kellyら2008]。
動脈瘤様骨嚢胞
動脈瘤様骨嚢胞とは、もともとFDが存在した部位の内部に液で満たされた病変が急速に拡大していく状態をいう。こうした病変を最も検出しやすいのはMRIである。これがみられる場合は、激しい疼痛が急に出現し、局所の変形が急激に拡大する。そして、稀には嚢胞が視神経を圧迫して急速に視力が失われるような例もみられる。こうしたことから、動脈瘤様骨嚢胞は罹病リスクが高い(「臨床的マネジメント」の項を参照)。
悪性転化
合併症としてFDの悪性転化が生じることは稀である。悪性転化をみた例の多くは、過去に受けた放射線治療との関連で報告されたものである[Ruggieriら1994]。ただ、成長ホルモン分泌亢進は、悪性転化の素因となりうる1要素である[Salenaveら2014]。
X線写真所見
線維性骨異形成のX線写真上での現れ方は、その部位により変わってくる。
- 付属肢骨格は、X線写真で膨張性の病変がみられ、骨内縁のホタテ貝様陥凹、皮質の菲薄化、「擦りガラス様」外観を呈する(図2A)。
- 頭蓋顔面骨格に現れる線維性骨異形成は、通常は膨張性で、X線写真では硬化像として現れるが、CTでは典型的な「擦りガラス様」外観を呈する(図2C)。
- 加齢とともに、付属肢骨格の線維性骨異形成病変はX線写真上での硬化度を増す傾向にあり、一方、頭蓋顔面の線維性骨異形成は「嚢胞様の」外観を呈するようになる(図2D)。
内分泌障害
内分泌障害は、以下のどの形でも現れる可能性がある。
- 思春期早発症
FD/MASの女児には、思春期早発症が多くみられ(85%)、表に現れる症候はこれであることが多い。反復性卵巣嚢腫(図4A)により間歇性にエストロゲンが産生され、これにより乳房の発達、成長促進、膣出血などが生じる。嚢腫形成の間期には乳房組織は退行し、エストロゲン値は思春期前の時期のレベルにまで低下する。卵巣嚢腫は、通常、成人期まで存続し、月経不順をもたらす。これにより排卵周期が中断される可能性があり、成人女性では受胎までの期間の延長につながる場合がある。大きな嚢腫が持続する女児や女性で、稀に卵巣捻転がみられる[Clarkら2000]。
思春期早発症は、FD/MASの男児ではそれほど多くはみられないが(10%-15%近く)、その原因となるのは、自律的なテストステロン産生である[Boyceら2012a]。そして、成長加速、陰毛・腋毛、痤瘡、攻撃的で不適切な性的行動といった進行性の思春期発達を生じる。
女児にも男児にも言えることであるが、性ステロイドの自律的産生が遷延すると、通常、視床下部-下垂体軸の活性化と、中枢性思春期早発症の発生を招くことになる。
- 妊孕性
自律性の性ステロイド産生が成人における下垂体-性腺機能や妊孕性に及ぼす影響については、まだ十分には解明されていない。FD/MASの女性の中には、反復性嚢腫を有し、成人期における月経不順をきたす例がみられる[Lalaら2007]。NIHのコホートで、多くの女性が妊娠に成功しているとはいえ、排卵周期が中断されることで妊孕性の低下や受胎までの期間の延長を招いているということは、可能性として考えられる[著者らの個人的見解]。
- 精巣の異常
MASの少年や男性の大多数(85%近く)に精巣の異常がみられ、通常、それは片側性あるいは両側性の巨大精巣の形で現れる[Boyceら2012a]。超音波検査では、Leydig細胞やSertoli細胞の過形成領域に一致した形で、別々の高エコー・低エコー病変ならびに微小石灰化が確認される(図4B)。
精巣病変の悪性転化の可能性については、よくわかってはいないものの、低いように見受けられる[Boyceら2012a]。
- 甲状腺疾患
FD/MASでは、甲状腺に影響が及ぶ例が多くみられる。FD/MAS罹患者の約半数において、甲状腺は、正常に見える組織の間に嚢胞状、固体状の病変が散りばめられたような形の超音波所見を示す(図4Cならびに4D)[Celiら2008,Tessarisら2012]。
FD/MAS罹患者の10%から30%に甲状腺機能亢進症がみられるが、これは、ホルモン産生の増加と、サイロキシン(T4)からトリヨードサイロニン(T3)への変換亢進の両方によって生じる[Celiら2008]。
甲状腺機能亢進症は、通常、軽度から中等度であるが、中には重度の例もみられ、これが把握できていないような場合は、手術の際の麻酔の導入時に甲状腺クリーゼに陥る危険がある[Lawlessら1992]。
甲状腺機能亢進症に対するコントロールがなされていないと、骨年齢亢進、骨代謝亢進、骨折といったものをきたす場合がある。
稀ながら、罹患甲状腺組織の悪性転化の報告がみられる[Collinsら2003]。
- 成長ホルモン分泌亢進
FD/MAS罹患者の約15%-20%は、下垂体前葉にGNASの病的バリアントを有し、これにより自律的な成長ホルモン産生をきたす可能性がある。自律性の成長ホルモン産生を示す罹患者の約80%は、同時に高プロラクチン血症も有する[Salenaveら2014]。
罹患者には、通常、線的成長の加速がみられ、先端巨大症の症候を示すようになる場合がある。成長ホルモン分泌亢進は、臨床的には、同じく成長加速を示す思春期早発症や甲状腺機能亢進症とはっきり区別する必要がある。
成長ホルモン分泌亢進を未治療のままにしておくと、頭蓋顔面の線維性骨異形成の拡大により、大頭症、ならびに視力喪失のリスク上昇につながる[Boyceら2013](図2B参照)。
- FGF23媒介性リン酸塩喪失
FD罹患者の大多数は、リン酸尿ホルモンであるFGF23のFD組織中における産生増加により、一定量のリン酸塩喪失を伴う腎尿細管疾患に至る[Collinsら2001]。ただ、FD罹患者で通常の低リン酸血症がみられることはそれほど多くない。その理由は、1つには、不活化断片への切断が進むようなFGF23のプロセッシングの変化がFD組織内で生じることにある[Bhattacharyyaら2012]。FD内におけるFGF23の過剰産生の程度は、疾患の重症度や骨格的負荷と相関関係がある。すなわち、通常の低リン酸血症がみられるのは、相当量のFD負荷を有する罹患者に限られるということである[Riminucciら2003]。
FD/MASでみられる他のほとんどの症候と違い、低リン酸血症は、罹患者の生涯を通じて悪化・軽快を繰り返すことがあり、急激な骨格成長を示す時期に、より重度となることがある。また一方、罹患者の年齢が上がるにつれて、低リン酸血症の問題は解決するといったこともある。こうしたことは、おそらく、年齢とともに生じるFD内部の変化を反映したものと思われる[Kuznetsovら2008]。
通常の低リン酸血症を有する罹患者については、くる病/骨軟化症、骨折の頻発、骨痛を発症する場合がある[Leetら2004a]。
- 高コルチゾール症
FD/MASの乳児については、胎児副腎からのコルチゾール産生過剰に起因するCushing症候群を呈する例が稀にみられる[Brownら2010,Carneyら2011]。臨床症候は、通常、新生児期に発症し、時に重度のことがあり、深刻な状況に至って死亡するようなこともある。生存者の約半数で自然消退が生じると報告されているが、これはおそらく胎児副腎の退縮によるものと思われる。
肝臓
- 乳児期には、顕著な肝炎や新生児胆汁鬱滞がみられる場合がある。これはふつう、年齢とともに、より軽度な持続性のものへと落ち着いていく[Silvaら2000,Ikawaら2016]。
- 肝細胞腺腫で、GNASの機能亢進型病的バリアントが同定された例の報告がみられる[Gaujouxら2014]。
- FD/MASの成人罹患者で肝不全に陥った例は、報告されていない。
消化器
- 小児については、胃食道逆流症がみられることがあり、時に重度の場合もある。
- FD/MAS罹患者に多くみられる所見として、最近になって上部消化管ポリープが報告されている[Woodら2017]。
膵臓
FD/MAS罹患者の約15%が、膵臓の合併症を有する。
- 膵炎
- 膵管内乳頭粘液性新生物(IPMN)
その場合の異形成のグレードには、ばらつきがみられる[Gaujouxら2014,Woodら2017]。
IPMN腸型サブタイプに由来する膵癌罹患者の報告がみられる[Parvanescuら2014]。
粘液腫
筋肉内粘液腫は、良性で、ふつうは無症状、偶然発見されるという例が多い。
血液
- 骨と骨髄は、程度の差こそあれ、ふつう、造血性の骨髄を欠く線維性組織に置換される。
- FD/MAS罹患者において、摘脾を要するような汎血球減少と髄外造血を伴う骨髄不全の報告がみられる[Mahdiら2017,Robinsonら2018]。
乳癌
FD/MAS女性は乳癌に関し高リスクである可能性があり、かつ、一般集団と比較して低年齢で生じる可能性を有する。ただし、FD/MAS女性の乳癌中にGNASの病的バリアントが同定されたのは、調査したものの半数に過ぎない[Majoorら2018a]。
健康関連のQOL
FD/MAS罹患者に身体機能に障害がみられ、疾患の重症度と強い相関を示すとの報告がいくつかみられる。それでも、本疾患を有する罹患者は社会性や感情といった機能は維持されている。こうしたものは、予後や親の安心といった点では重要な要素である[Kellyら2005,Majoorら2018b]。
遺伝型-表現型相関
遺伝型-表現型相関として、わかっているものはない。
現在までにFD/MAS罹患者で同定されているのは、p.Arg201、p.Gln227という2つの残基に生じたGNASの体細胞性の機能亢進型病的バリアントのみである。
疾患の重症度は、モザイクのレベル、ならびに罹患組織がどこかといったことによって左右される要素が強いように思われる。
疾患名について
FD/MASと筋肉内粘液腫との連合は、「Mazabraud症候群」と呼ばれている[Coxら2017]。
発生頻度
FD/MASは稀な疾患である。発生頻度に関する信頼に足るデータは存在しないものの、推定値は、100,000人に1人から1,000,000人に1人の間にある。
これとは対照的に、線維性骨異形成(特に単骨性のもの)はそれほど珍しいものではなく、良性骨腫瘍の7%を占めると推定されている。
FD/MASの罹患者は両性に及び、特定の集団に偏る傾向もみられない。
遺伝学的に関連のある疾患(同一アレル疾患)
GNASの特定の残基に生じる体細胞性の活性化型(機能獲得型)バリアントがFD/MASを引き起こすのに対して、GNASに生じる生殖細胞系列の不活性化型(機能喪失型)バリアントは、複数の表現型を引き起こす。さらに、GNASはインプリンティングを受ける遺伝子であるため、生殖細胞系列の不活性化型バリアントに起因して生じる表現型は、変異アレルが母性起源か父性起源か、ならびに、組織中で生じているインプリンティングの程度により変わってくる。GNASの生殖細胞系列の不活性化型病的バリアントに伴って生じる各種表現型を、表2に示した(「GNAS不活化疾患」のGeneReviewを参照)。
表2:GNASの生殖細胞系列不活性化型(機能喪失型)バリアントで生じる同一アレル疾患
| 表現型 | GNASのバリアント | OMIM/参照 |
|---|---|---|
| 偽性偽性副甲状腺機能低下症 | 父性GNASアレルのヘテロ接合性不活性化型病的バリアント | 612463 |
| 偽性副甲状腺機能低下症Ⅰa | エクソン1-12の母性GNASアレルのヘテロ接合性不活性化型病的バリアント | 103580 |
| 偽性副甲状腺機能低下症Ⅰb | インプリンティング異常:母性GNAS複合体座位調節因子のヘテロ接合性欠失1 | 603233 |
| 偽性副甲状腺機能低下症Ⅰc | 母性GNASアレルのエクソン13のヘテロ接合性の不活性化型病的バリアント | 612462 |
| 進行性骨性異形成症 | 父性GNASアレルのヘテロ接合性の不活性化型病的バリアント | 166350 |
- 偽性副甲状腺機能低下症Ⅰbは、STX16のヘテロ接合性欠失によっても引き起こされる。
FD/MASの症候を有さず、単一腫瘍として発生する散発性の腫瘍(下垂体・膵・乳腺・結腸直腸等の腫瘍)内に、GNASの体細胞性の機能亢進型病的バリアントがしばしば同定される(生殖細胞系列にみられるわけではない)。こうした例では、腫瘍に関する素因が継承されるわけではない。
詳しい情報については、「分子遺伝学」の「癌ならびに良性腫瘍」の項を参照されたい。
鑑別診断
神経線維腫症1型(NF1)
神経線維腫症1型とFD/MASは、カフェオレ斑、骨格異常をはじめ、いくつかの症候が重なる。NF1では、皮膚所見として、6つ以上のカフェオレ斑がみられる。FD/MASの場合の皮膚病変が「メイン州の海岸線」状の不規則なラインになるのに対し、NF1のほうは境界が平滑な「カリフォルニア州の海岸線」状を呈する。NF1の骨格症候としては、脊柱後側彎、蝶形骨異形成、長管骨皮質の菲薄化、脛骨を中心とした骨の彎曲や異形成(これにより偽関節に至る場合がある)などがある。また、NF1の特徴的症候として、神経線維腫、視神経膠腫、色素性虹彩過誤腫、腋窩部雀卵様色素斑をはじめとする神経系の腫瘍がある。NF1は、NF1のヘテロ接合性病的バリアントに起因して生じ、常染色体顕性の遺伝形式をとる。
皮膚骨格低リン酸血症候群
皮膚骨格低リン酸血症候群は、HRASとNRASの体細胞性機能亢進型病的バリアントに起因して生じるモザイク障害である[Limら2014]。罹患者には、モザイク状の分布を示す皮膚病変(表皮性で大きな色素細胞母斑)、モザイクの骨格異形成、くる病/骨軟化症をもたらすFGF23の産生過剰、その他、眼・脳・血管にさまざまな幅の関連奇形が現れる[Ovejeroら2016]。
線維骨性病変
線維骨性病変においては、線維性骨異形成症と同様のX線写真症候ないし組織学的所見が現れることがある。線維骨性病変は基本的に孤立性であり、骨以外の症候を伴わない。また、GNASに病的バリアントもみられない。
- 骨巨細胞腫(giantcelltumorofbone)
骨巨細胞腫は、骨髄間質細胞の増殖や複数の多核巨細胞の存在といった、線維性骨異形成症に似た病理組織像を呈する後天性病変である。巨細胞腫は、通常、良性であるが、局所の骨破壊をきたしたり、稀ながら転移を起こしたりする場合もある。
- 骨形成線維腫(ossifyingfibroma)
骨形成線維腫は、通常、下顎骨と上顎骨に現れる良性病変で、固く無痛性の塊の局所性拡大がみられる。一般に、骨形成線維腫は、頭蓋顔面の線維性異形成病変より侵襲性が強いため、外科的切除での対応が行われる。
- 骨線維性異形成(osteofibrousdysplasia)
骨線維性異形成は、通常、10歳未満の小児に生じ、脛骨前部に最も多く現れる。患児には、無痛性、限局性の腫脹が現れ、稀には骨折や進行性変形を示す場合もある。X線写真では、骨皮質内面に沿った位置に、特徴的な硬化縁をもつ境界明瞭なX線透過性病変として現れる。
- ケルビム症
ケルビム症は、主として下顎骨と上顎骨に現れる進行性の線維骨性病変を特徴とする。通常、幼児期に、下顔面の両側性、対称性拡大として現れ、後には、上顎骨の病変により両眼が上を見つめているような、特徴的な「ケルビム様」外観を呈するようになる。顔面の変形は小児期から思春期初期にかけて進行するが、その後、自然退行に転じるような例も一部みられる。ケルビム症の大多数は、SP3BP2のヘテロ接合性病的バリアントに起因して生じる。遺伝形式は常染色体顕性遺伝である。
臨床的マネジメント
最初の診断に続いて行う評価
線維性骨異形成症/McCune-Albright症候群(FD/MAS)罹患者については、最初の診断の後、疾患の範囲を確定するための評価をすべての例で行う必要がある。FD/MASの何らかの症候がみられる場合には、それ以外の症候がないか、詳細にわたって臨床評価を急ぐ必要がある。著者らは、まだ行っていないようであれば、以下の検査を行うことを推奨する。
骨格
- FDの範囲を確定させることを目的とした全身の骨シンチグラフィー[Collinsら2005]。臨床的に重要な骨格病変の大部分は、5歳までには骨スキャンで認められるようになる。
- FDと確認された部位については、病変の範囲とその解剖学的状態を明確にするためのX線写真(軸骨格と付属肢骨格のFD)ないしCT(頭蓋顔面のFD)による画像化。
- 頭蓋顔面のFDを有する例については、ベースラインの記録としての眼科的、耳鼻咽喉科的、聴覚的評価。
- 骨格の評価(図3参照)
内分泌
内分泌障害の臨床的徴候に関する評価を行うことを目的として、徹底した病歴聴取と身体の診査、ならびに、可能なら成長曲線をチェックすることが推奨される。
- 甲状腺機能亢進症、成長ホルモン分泌亢進(IGF-1値)、FGF23関連低リン酸血症に関する生化学的スクリーニング(図3,図6,図7参照)。
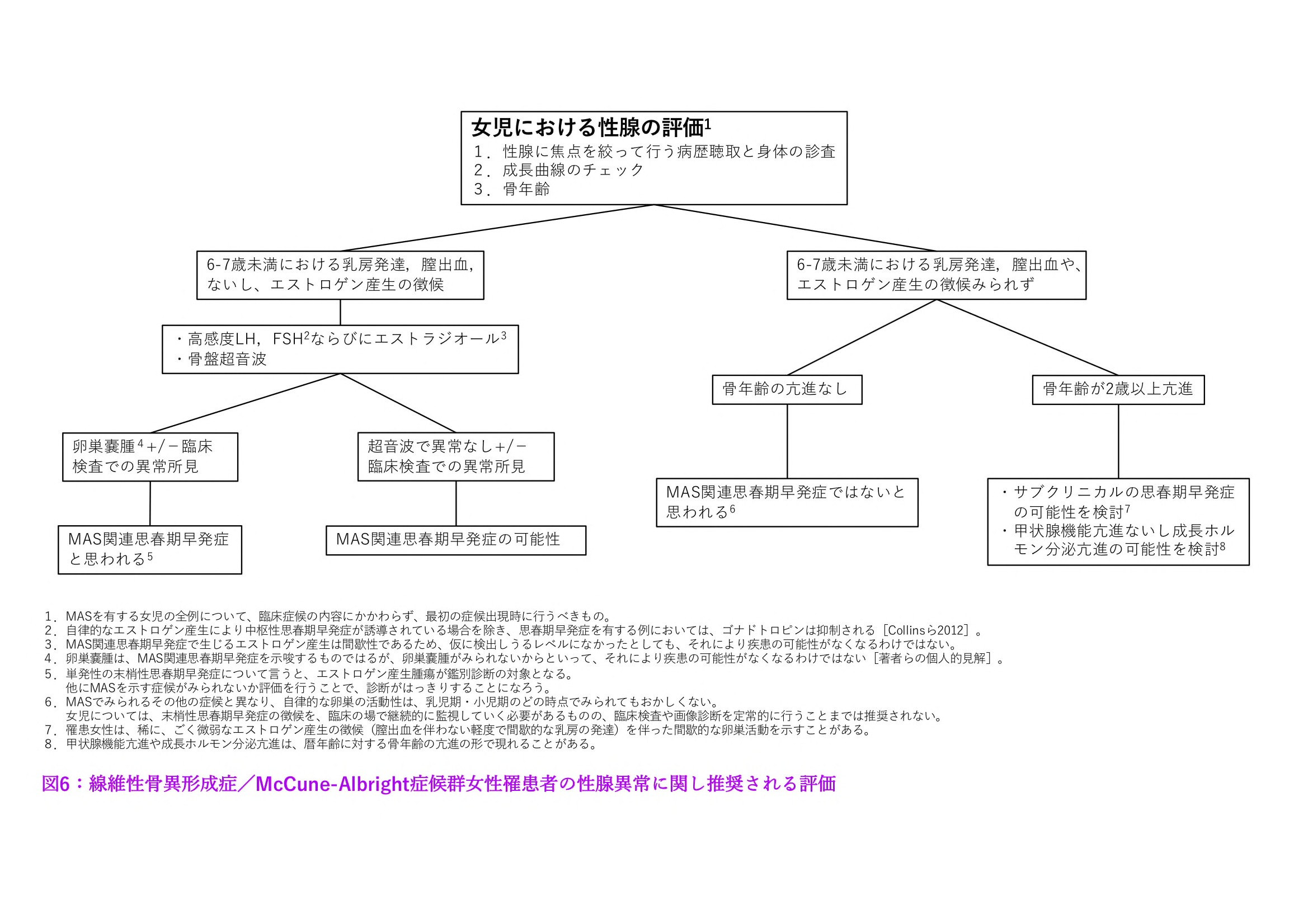
- 臨床的徴候あるいは過去に思春期早発症の既往がある例について:生化学的スクリーニング,骨盤の超音波検査(女性),骨年齢評価(図5ならびに図6参照)。
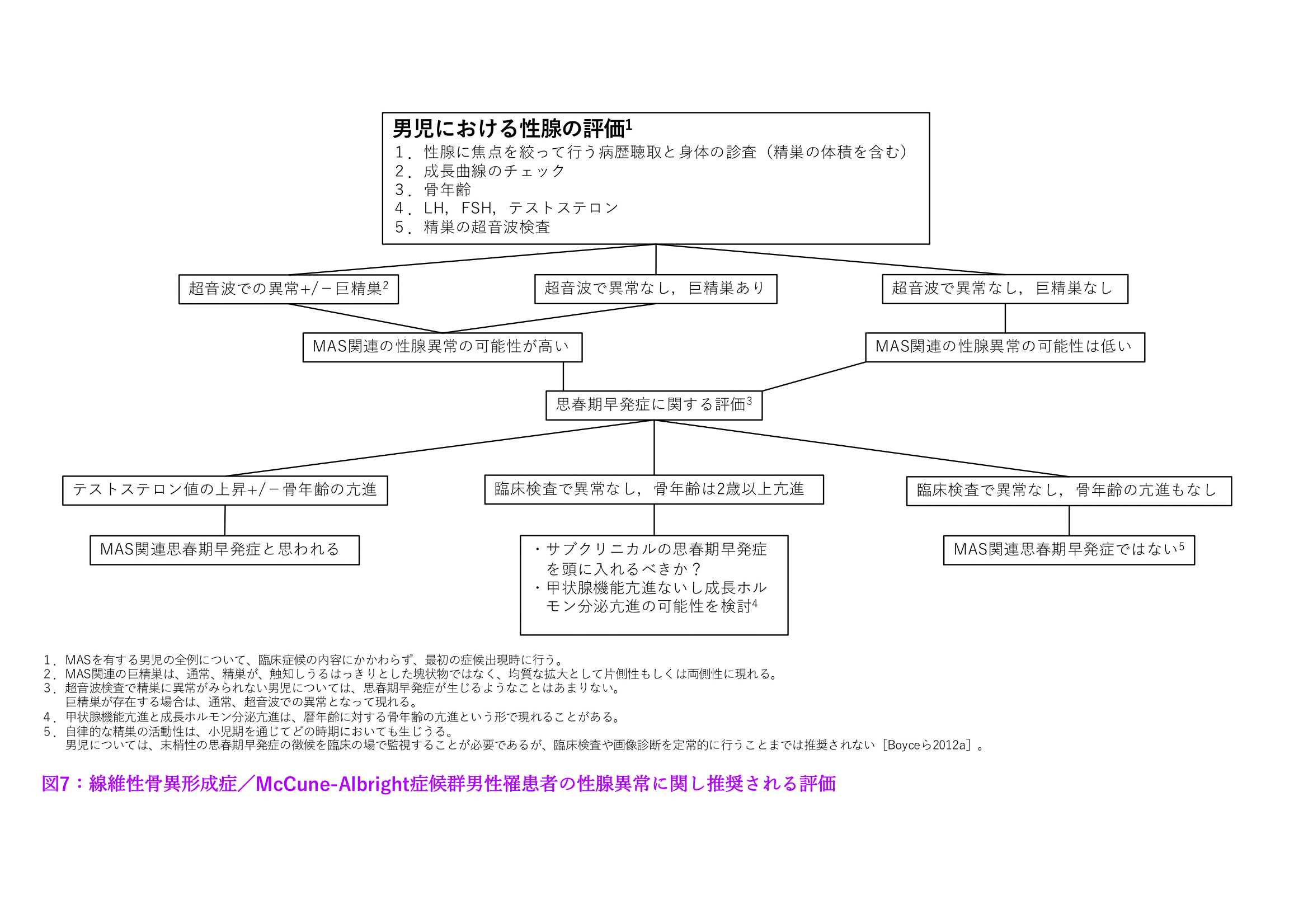
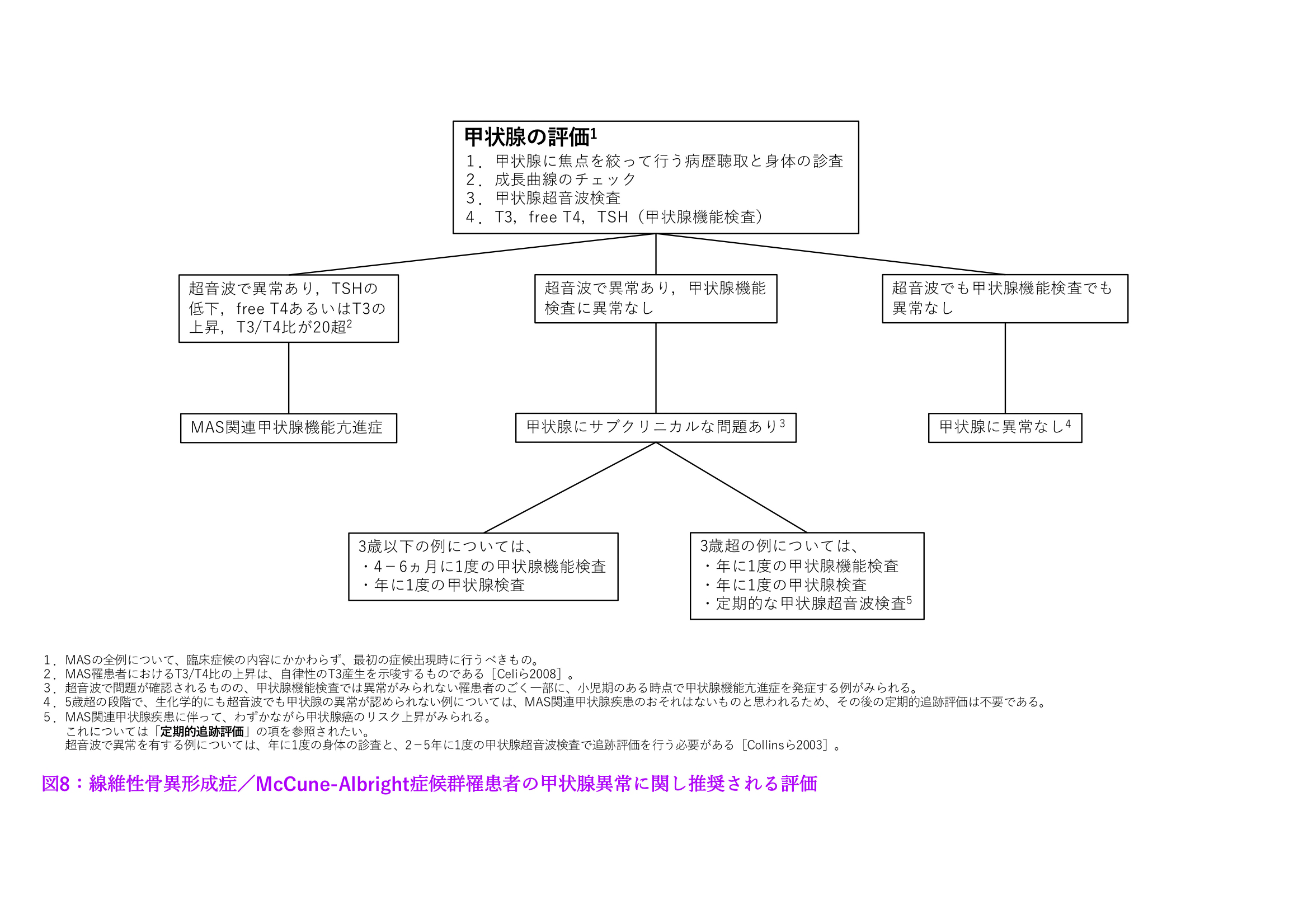
- 顕在化していない病変の評価を目的とした甲状腺ならびに精巣(男性の全例)の超音波検査(図7ならびに図8参照)。
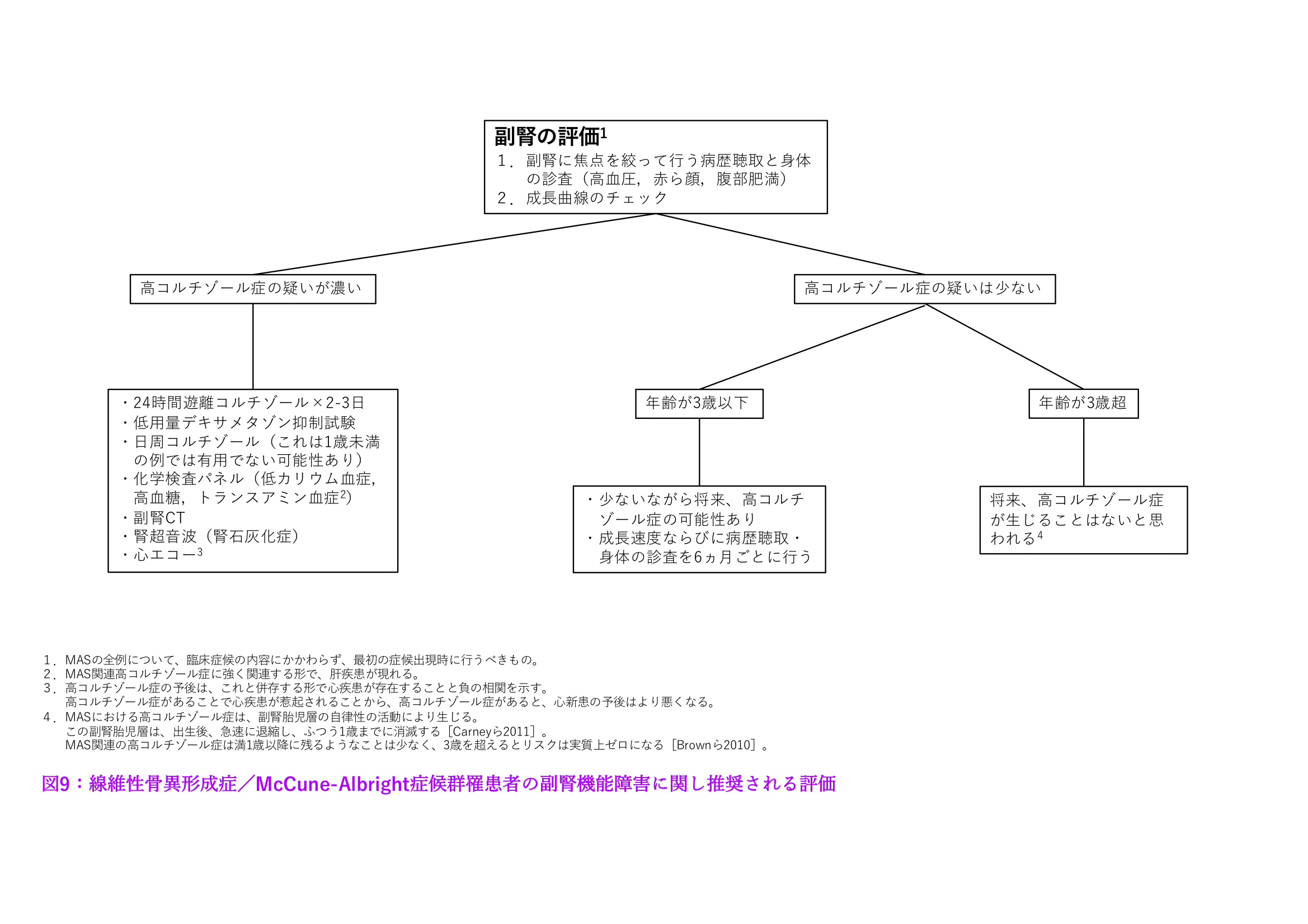
- Cushing症候群を示す臨床的データ(高血圧,顔面肥大,腹部肥満,発達遅滞,成長障害,在胎不当過小)を有する乳児に対する高コルチゾール症の検査(図9参照)。
それほど多くみられない症候
「臨床像」の項で取り上げたそれほど多くみられない症候に対しては、適切な臨床評価を行うとともに、必要に応じ画像診断や生化学検査を施行することを検討すべきである(消化器系の評価については図10参照)。
図5:線維性骨異形成症/McCune-Albright症候群罹患者の成長ホルモン分泌亢進に関して推奨される評価
図6:線維性骨異形成症/McCune-Albright症候群女性罹患者の性腺異常に関して推奨される評価
図7:線維性骨異形成症/McCune-Albright症候群男性罹患者の性腺異常に関して推奨される評価
図8:線維性骨異形成症/McCune-Albright症候群罹患者の甲状腺異常に関して推奨される評価
図9:線維性骨異形成症/McCune-Albright症候群罹患者の副腎機能障害に関して推奨される評価
図10:線維性骨異形成症/McCune-Albright症候群罹患者の消化器系の問題に関して推奨される評価
症候に対する治療
内分泌内科医、整形外科医、リハビリテーション医、眼科医、聴覚医、内分泌外科医、頭蓋顔面外科医、臨床遺伝医などから成る多職種チームの手で治療を進めることが最も効果的である。今のところ、コンセンサスを得た治療のガイドラインは公表されていない。
線維性骨異形成症
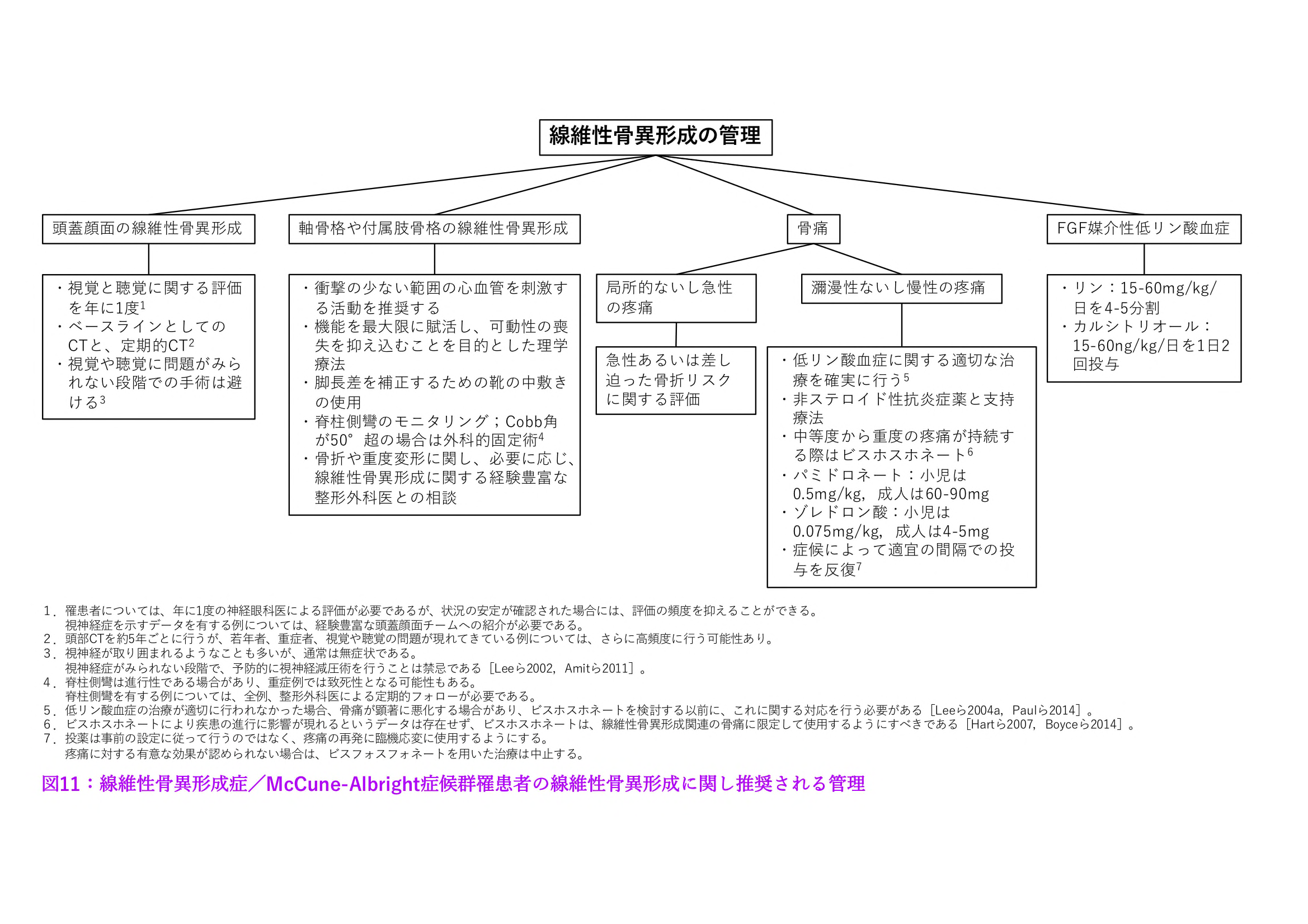
線維性骨異形成で生じる疾患の経過に変化を加えることができるような治療法は存在しない。現在行われている管理は、機能を最大限に引き出すとともに、骨折や変形といった病的状態を最小限に抑えることに焦点を当てたものとなっている。管理の要点は以下の通りである(図11を併せて参照)。
- 骨折を修復したり、変形を予防ないし矯正したりといった整形外科手術。従来、標準と考えられてきた治療法(例えば、搔爬、移植、外固定)は、多くの場合、有効ではない[Stantonら2012,Leetら2016]。そのため、紹介は、FDに関して経験豊富な外科医に向けて行うべきである。
- 脊柱側彎に対する診断や治療はきわめて重要である。というのは、これは急激に進行することがあり、稀ながら、致命的な呼吸障害をきたす場合があるからである。こうした理由から、脊椎のFDを有する例は、全例、進行がみられないかどうか、整形外科医もしくはリハビリテーション医が詳しくチェックする必要がある。脊椎の安定化に向けては、固定術が有効であることがわかっている[Leetら2004b,Manciniら2009]。
- 動脈瘤様骨嚢胞はもともとFDの存在した部位に生じる、液を内包して急速に拡大していく病変である。この検出には、MRIが最も適している。これが現れると重度の疼痛が急激に現れ、局所の変形が急速に拡大する。そして、稀ながら、嚢胞により視神経が圧迫されると、視力障害が急速に進む。こうしたことから、動脈瘤様骨嚢胞は病的状態を引き起こすリスクが高く、外科医による迅速な評価が求められる[Leeら2012,Manjilaら2013]。
- 視力障害のリスクを減少させることを目的として予防的に視神経減圧術を行うことは、むしろ視力障害のリスクを増大させることにつながりかねないため、禁忌とされている[Leeら2002,Cutlerら2006,Amitら2011]。
- 機能を最適な状態に誘導し、可動性の喪失を抑制する上では、理学療法が有用である。特に、下肢にFDを有する例については、腰帯の筋力低下、可動域、脚長差といった問題に対応するための治療が有益と思われる[Paulら2014]。
- 疼痛の緩和には、通常、ゾレドロン酸やパミドロン酸などのビスホスホネートの静脈内投与が有効である。投与は、一定間隔、あるいは骨代謝マーカーに従って行うのではなく、症状に従って行う必要がある。ビスホスホネートの経口薬であるアレンドロン酸は、骨痛の治療には無効であることがわかっている[Boyceら2014]。
- FDの数例で、RANKLに対するヒトモノクローナル抗体であるデノスマブが使用されており、疼痛、骨代謝マーカー、腫瘍増殖速度などの抑制がみられている。ただ同時に、これにより、治療中・投与中止後とも、骨塩代謝障害が臨床的に明らかな形で現れることもわかっている[Boyceら2012b,Benhamouら2014,Ganda&Seibel2014]。こうしたことから、われわれは、デノスマブについては、FD罹患者の治療経験が豊富な医療機関で、できるだけ臨床試験の形で使用するという場合にのみ推奨したい。
- FDの病変が急性ないし急速な形で拡大していく例、あるいは、骨皮質が直上にある軟組織とともに侵されていくような非定型的X線写真所見を呈する例については、悪性化ということも頭に入れておく必要がある。
図11:線維性骨異形成症/McCune-Albright症候群罹患者でみられる線維性骨異形成に関して推奨される管理
分泌障害
思春期早発症
思春期早発症の治療は、骨年齢の亢進を抑制し、成人期の身長の問題を回避する上で重要である。
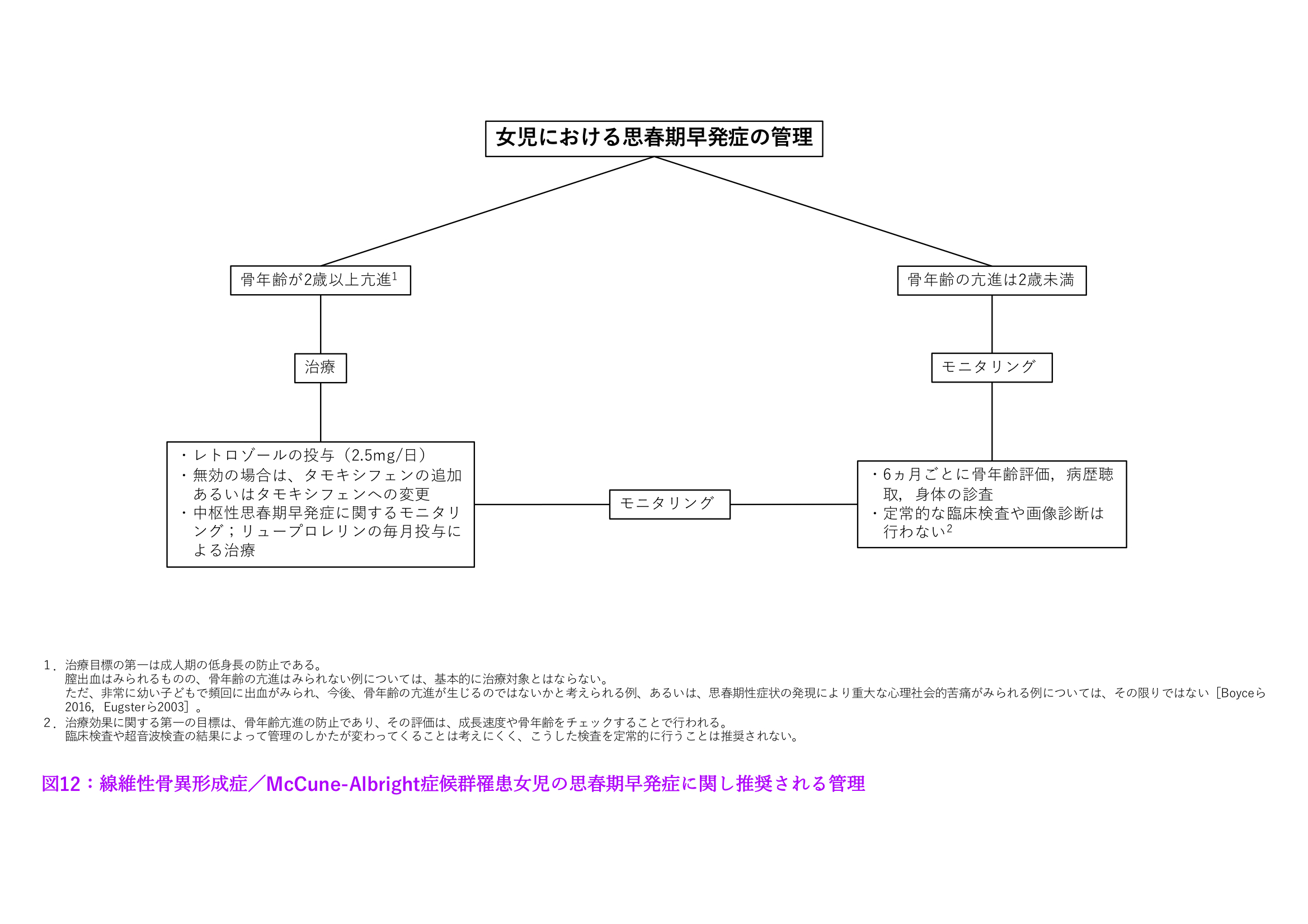
- 女性(図12参照)
女性に対しては、アロマターゼ阻害薬であるレトロゾールが1つの有効な治療法である[Feuillanら2007]。これまでで最も長い追跡期間をとった研究が、最近、公表されている。それによると、レトロゾールを用いた治療により、骨格成熟、成長速度、予測される成人期の身長といった点で、有益な効果がはっきりした形でみられたという[Estradaら2016]。同時に、大多数の女性については、月経時の出血回数の減少がみられている。大きく、また遺残性の卵巣嚢腫に対して、予防的視点から外科的介入を行うことについては、嚢腫の再発リスク、ならびに罹患女性の卵巣予備能低下の可能性が判明していることから、十分な上にも十分な注意が必要である。
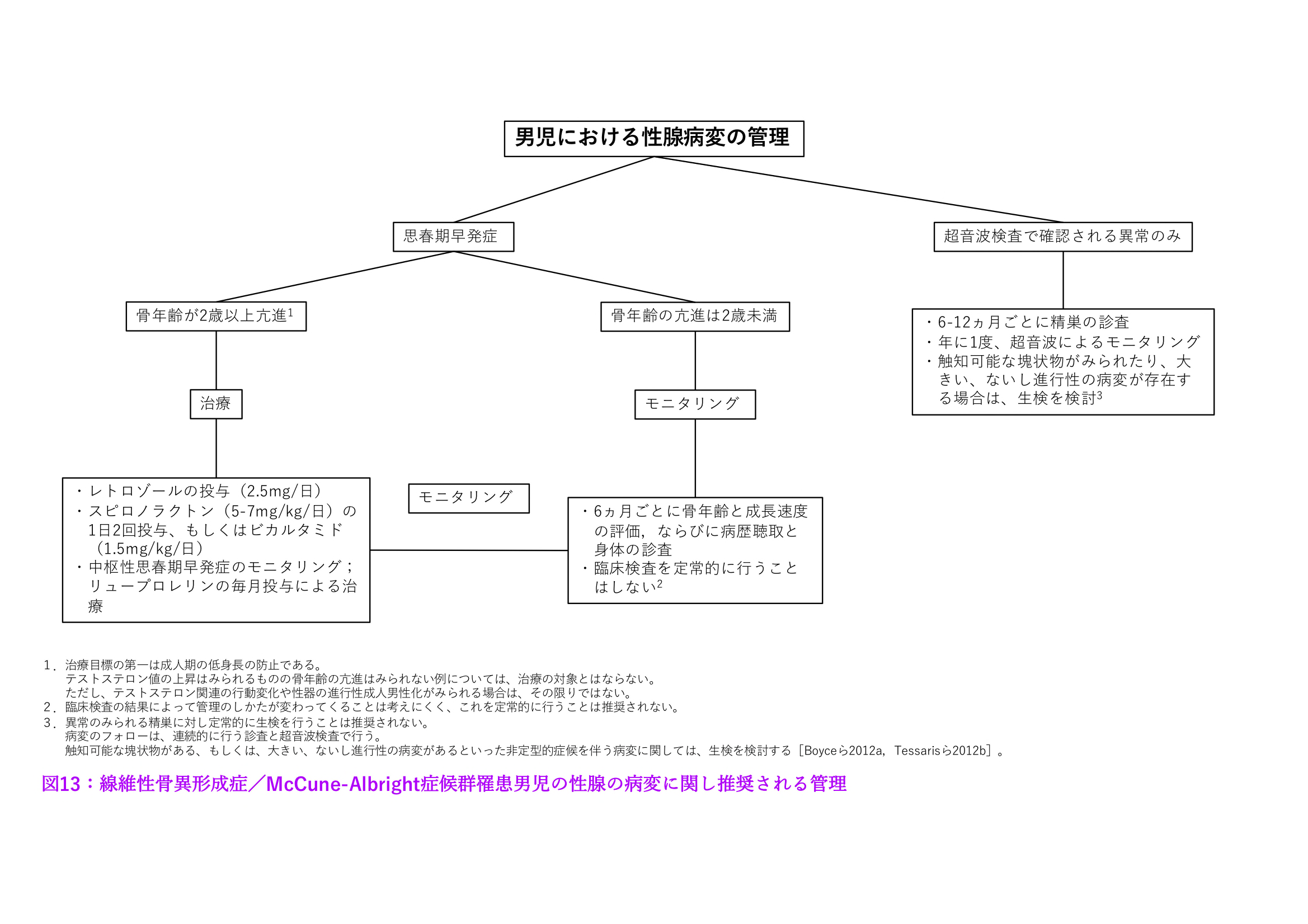
- 男性(図13参照)
男性の思春期早発症は稀であるため、治療法は十分に確立されていない。1つのやり方として、アンドロゲン受容体遮断薬(例えば、スピロノラクトンやビカルタミド)と性ステロイド合成阻害薬(例えば、レトロゾール)の併用が考えられる[Boyceら2012a]。
男児・女児両方に言えることであるが、通常より早期に性ステロイドに曝露することで、しばしば中枢性思春期早発症に移行することになる(「臨床像」の項を参照)。この中枢性思春期早発症は、それまで良好にコントロールされていた末梢性思春期早発症の子どもに再度、思春期の徴候が出現するという形で現れる場合が多い。ほとんどの例については、リュープロレリンを先に述べた薬剤と組み合わせて処方することが、治療戦略上、有効である。
図12:線維性骨異形成症/McCune-Albright症候群女児の思春期早発症に関して推奨される管理
図13:線維性骨異形成症/McCune-Albright症候群男児の性腺の問題に関して推奨される管理
甲状腺疾患
甲状腺機能亢進症治療にはメチマゾールが有効で[Tessarisら2012]、これが治療の第1選択となる。プロピオチルウラシルは、小児に対し許容範囲を超えるレベルの肝毒性のリスクがあるため、もはや推奨されない[Rossら2016]。FD/MAS関連の甲状腺機能亢進症は持続性であるため、最終的には、大多数の罹患者で根治治療が必要となる。そして、根治治療としては、ほとんどの場合、甲状腺摘出術が選択される。甲状腺組織は、再度増殖することが考えられるため、通常は全摘出が推奨される。合併症を最小限に抑え、最良の治療成績を得る上では、経験豊富で、症例数を多くこなした内分泌外科医を選択することが決定的に重要である。組織の再増殖の状況を評価するため、術後、罹患者は年に1度の割合で超音波検査によるモニタリングを受けることになる。
図14を参照されたい。
ラジオ波焼灼療法は、GNASの体細胞性機能亢進型病的バリアントを有する組織にラジオ波が優先的に取り込まれ、術後に残った非罹患腺組織中に悪性新生物が生じるリスクが高まる可能性があることから、通常、これは適用されない。さらに言うと、GNASの病的バリアントについては、甲状腺組織、非甲状腺組織とも、わずかながら悪性転化のリスク上昇があり、これが放射線被曝によって加速されるリスクが考えられる。
図14:線維性骨異形成症/McCune-Albright症候群罹患者の甲状腺機能亢進症に関して推奨される管理
成長ホルモン分泌亢進
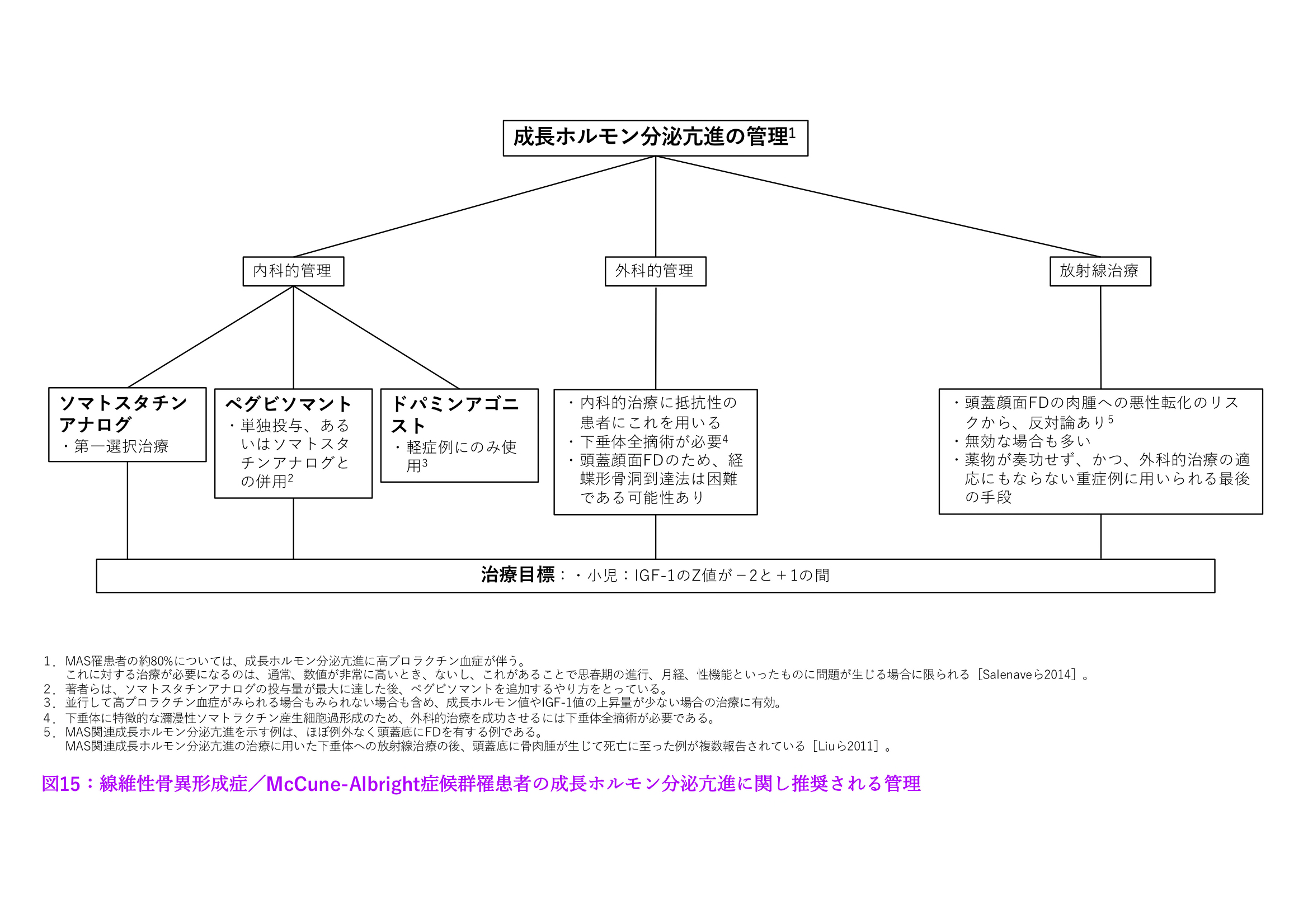
薬物療法が治療の第1選択となる。具体的には、ソマトスタチンアナログや、成長ホルモン受容体拮抗薬であるペグビソマントを、単独使用あるいは併用することが選択肢となる[Boyceら2013,Salenaveら2014](図15参照)。
- 成長期の子どもについては、IGF-1値を、正常範囲の中央付近で、なおかつZ値0未満に維持することが治療目標となる。
- 骨格成熟を終えた例については、IGF-1値を可能な限り下げることが目標となる。
薬物療法は、通常、無期限に継続されることになる。というのは、根治治療には重大な医学的問題がつきまとうからである。手術という選択肢は、手技的に困難でもあろうし、頭蓋顔面のFDのために非適応となるようなこともあろう。さらに言うと、GH産生細胞が下垂体にびまん性に浸潤しているとすれば、罹患者には下垂体全摘術が必要ということになり、汎下垂体機能低下をきたす結果になる[Vortmeyerら2012]。難治性の例については、放射線治療が有効な場合もあろうが、同時に、頭蓋顔面FDの致命的悪性転化につながる可能性もあるとされている[Hansen&Moffat2003,Liuら2011]。
成長ホルモン分泌亢進に伴ってしばしばみられる高プロラクチン血症については、通常、カベルゴリンやブロモクリプチンなどのドパミンアゴニストを用いた治療が奏功する。このクラスの薬剤は、高プロラクチン血症の有無を問わず、GH、IGF-1値の軽度上昇を伴う成長ホルモン分泌亢進の治療にも一定の効果を発揮することがある[Katznelsonら2014]。
図15:線維性骨異形成症/McCune-Albright症候群罹患者の成長ホルモン分泌亢進に関して推奨される管理
FGF23媒介性リン酸塩喪失
通常の低リン酸血症の治療は、リン、カルシトリオールの経口摂取といった、他のFGF23過多の疾患と同じやり方で行われる。治療終了の指標として重要なものに、成長速度と、X線写真で確認される骨端線の閉鎖がある。他のFGF23過多の疾患と異なり、FD/MASの場合、骨代謝マーカー(例えば、アルカリホスファターゼ)は恒常的に上昇することがあるため、治療に対する骨格の反応を計る指標としては有用ではない。
高コルチゾール血症
新生児Cushing症候群は稀であることから、高コルチゾール症の治療のガイドラインを確立することは難しい。さらに、発症の段階ですでに重篤な状況にあるような場合もあり、そうした状況次第で治療の選択肢は大きく影響されることになる。
- 根治治療は、病的状態にある副腎の外科的切除になる。
- 薬物治療に関して言うと、メチラポンが有効なことが多く、肝臓の異常を伴う子どもについては、ケトコナゾールよりもこちらのほうが多く用いられる。
数人の罹患者でみられた自然寛解を正確に述べた報告がみられる[Brownら2010]。ただ、どういった罹患者であれば寛解が得られるのかという点を事前に把握できるところ
にまでは至っていない。副腎摘出術を施行するか先送りにするかの決定は、病状の重症度、コルチゾール値を薬剤でコントロールできる余地があるか否か、高コルチゾール症が続くことで神経発達にどういった影響が考えられるかといった点を勘案しながら、症例ごとに下す必要がある。図16を参照されたい。
図16:線維性骨異形成症/McCune-Albright症候群罹患者の高コルチゾール症に関して推奨される管理
膵臓疾患
FD/MAS関連の膵管内乳頭粘液性腫瘍(IPMN)の自然経過、ならびにIPMN特異的悪性化リスクについては、まだよくわかっていない。著者らは、これが明らかになるまで、暫定的に、一般集団でのIPMNの評価に関するガイドライン[Tanakaら2012]に準拠することを推奨したい(図17参照)。
図17:線維性骨異形成症/McCune-Albright症候群罹患者の膵臓疾患に関して推奨される管理
定期的追跡評価
本疾患はモザイク的性格を有しているため、罹患者の臨床所見には非常に大きなばらつきの幅があり、ある例では1つの器官のみに病変がみられるということもあれば、またある例では非常に広い範囲に影響が及ぶといったこともある。さらに、年齢によって変わってくる症候もあり、ある年齢を超えれば現れることはないという症候もあれば、逆に、子どもに比べ、年齢を経た罹患者に現れやすいといった症候もみられる。以下に述べる追跡評価に関する情報は、本疾患の徴候や症候に関する評価をすでに終えた罹患者、ならびに、疾患の範囲に関する評価がすでになされた罹患者を対象としたものである。追跡評価の内容は、あくまで、罹患者個人の年齢や罹患組織の範囲に応じて、個別的に検討されるべきものである(表3参照)。
線維性骨異形成
図3を参照されたい。
- 頭蓋顔面のFDを有する罹患者については、視覚や聴覚に関する評価を年に1度、そして頭蓋骨のCT撮影を定期的に行う必要がある。
- 脊椎のFDを有する罹患者については、進行性の脊柱側彎を念頭に、注意深くモニタリングを行う必要がある。
- 症候の新規発現あるいは悪化状況を把握するとともに、FDの解剖学的状況や骨の質的状況を随時把握していくため、定期的にX線写真を撮影する必要がある。
- FGF23媒介性低リン酸血症の発症に関するモニタリングを目的として、リン値のチェックを定期的に行う必要がある。
- 通常の骨の状況把握の一環として、25ヒドロキシビタミンD値のモニタリングを定期的に行う必要がある。
内分泌障害
思春期早発症
小児の罹患者については、全例、成長の加速や、その他の思春期早発症の臨床的徴候に関するモニタリングを行う必要がある(図5参照)。
精巣の病変
男性罹患者については、全例、身体の直接診査と精巣超音波検査を定期的に行うことでモニタリングを行うのが賢明である(図7参照)。
甲状腺
5歳未満の子どもについては、全例、甲状腺機能の検査(TSH,freeT4,freeT3)を行う必要がある。
- 甲状腺超音波検査で異常がみられるものの、甲状腺機能検査では異常がみられないといった例については、小児期を通じて継続的、定期的に臨床検査を行う必要がある。それは、その後、通常の甲状腺機能亢進症が出現する可能性があるからである(図8参照)。
- 甲状腺の手術後も異常甲状腺組織が残存している例については、甲状腺組織が再増殖する可能性があるため、通常の身体の診査、ならびに定期的な甲状腺超音波検査によるモニタリングが必要である。
成長ホルモン分泌亢進
子どもについては、全例、成長の加速に関するモニタリングが必要である。
- 大きな頭蓋顔面のFDを有する例については、成人初期に至るまでの間、通常のIGF-1値のモニタリングを行う必要がある。
- ソマトスタチンアナログで内科的治療を受けた例については、胆嚢疾患に関するモニタリングが必要である。
- また、ペグビソマントで治療を受けた例については、肝毒性に関するモニタリングが必要である(図15参照)。
FGF23媒介性リン酸塩喪失
血清リン値については、全例において定常的モニタリングが必要である(図3参照)。
高コルチゾール血症
これについては、定常的な生化学的追跡は不要である。ただ、乳児については、全例、高コルチゾール症の臨床的徴候に関するモニタリングが必要である。
Cushing症候群が自然寛解をみた既往を有する例については、遅発性の副腎不全に関するモニタリングが必要である(図9参照)。
悪性腫瘍
FD/MASの病的バリアント(すなわち、GNASのp.Arg201とp.Gln227の2つの残基の機能亢進型病的バリアント)と悪性腫瘍との間に特段の相関を示すデータが存在するわけではないものの、リスク因子となりうるもの(例えば、放射線被曝)がこれに加わることを最小限に抑え、警戒・監視を怠らないようにするのが賢明である。
FD/MASの女性は乳癌に関し高リスクであることから、一般集団で推奨されている年齢より早い段階でスクリーニングを行うことを検討する必要がある[Majoorら2018a]。
表3:線維性骨異形成症/McCune-Albright症候群罹患者に検討すべき定期的追跡評価
| 系/懸念事項 | 評価 | 実施頻度 | |
|---|---|---|---|
| 筋骨格1 | 整形外科医もしくはリハビリテーション医による脊柱側弯の進行状況、ならびにその他の骨格所見に関するモニタリング | 通常の間隔で。 | |
| 頭蓋骨のCT | 5年ごと。 ただし、若年者や重症者、あるいは視覚・聴覚に問題が現れた場合は、もう少し間隔を狭めて行う可能性あり。 |
||
| 症候の新規発現あるいは悪化状況を把握するとともに、FDの解剖学的状況や骨の質的状況を随時把握していくためのX線写真 | 定期的に。 | ||
| 内分泌 | 思春期 (女性) |
成長の加速をはじめとする思春期早発症の臨床的徴候に関する評価2,3 | 来院ごと。 |
| 骨年齢評価 | 骨年齢が2歳以上進んでいる例について、6ヵ月ごと。 | ||
| 思春期 (男性) |
成長の加速をはじめとする思春期早発症の臨床的徴候に関する評価2,3 | 来院ごと。 | |
| 骨年齢評価 | 骨年齢が2歳以上進んでいる例について、6ヵ月ごと。 | ||
| 精巣の直接診査 | 来院ごと。 | ||
| 精巣超音波検査 | 定期的に。 | ||
| 甲状腺 | 甲状腺機能検査(TSH,freeT4,T3) | 5歳未満の子どもは全例、通常の間隔で行う。 超音波検査で異常がみられた場合、小児期を通じ、3歳未満で4-6ヵ月ごと、3歳超で年に1度の間隔で行う4。 |
|
| 甲状腺の直接診査 | 甲状腺摘出術後に異常甲状腺組織が遺残した例について、定期的に行う5。 | ||
| 甲状腺超音波検査 | 甲状腺超音波検査で異常がみられた例、あるいは、甲状腺摘出術を行った例について、定期的に行う6。 | ||
| 副腎7 | 高コルチゾール症の臨床的徴候8 | 乳児について、来院ごと。 | |
| Cushing症候群が自然寛解をみた既往をもつ例について、遅発性の副腎不全の徴候・症候に関する評価 | 来院ごと。 | ||
| 血清IGF-1値 | 頭蓋顔面のFDを有する例について、成人初期まで通常の間隔で。 | ||
| ソマトスタチンアナログの投与を受けた例について、胆嚢疾患の徴候・症候に関する評価 | 定期的に。 | ||
| 腎 | 血清リン値ならびに25ヒドロキシビタミンD値の評価1,9 | 定期的に。 | |
| 眼 | 眼科医(あるいは神経眼科医)による評価 | 頭蓋顔面のFDを有する例について、年に1度。 | |
| 耳鼻咽喉 | 聴覚士による評価 | 頭蓋顔面のFDを有する例について、年に1度。 | |
| 消化器 | ペグビソマントの投与を受けた例について、肝毒性を示すデータの評価 | 定期的に。 | |
| 腫瘍 | 一般集団で推奨される年齢より早い段階で乳癌のスクリーニングを開始することを検討10 | 定期的に。 | |
- 図3参照。
- 図6参照。
- 成長の加速は、成長ホルモン分泌亢進の徴候である場合もある。
- 甲状腺超音波検査で異常がみられるものの、甲状腺機能検査では異常がみられないといった例については、通常の甲状腺機能亢進症が出現するリスクがある。
- 図14参照。
- 甲状腺組織は、甲状腺摘出術後に再増殖する可能性がある。
- 図9参照。
- 高コルチゾール症については、通常の生化学的追跡評価の適応とはならない。
- FGF23媒介性低リン酸血症の発生に関する監視、ならびに通常の骨の生理的評価の一環として行う。
- Majoorら[2018a]。
避けるべき薬剤/環境
大きな骨格病変を有する例については、コンタクトスポーツや高リスクの活動を控える必要がある。
予防的視神経減圧術は施行しない。(「症候に対する治療」の項を参照)
卵巣嚢腫摘出術は、細心の注意を払って、限られた状況においてのみ行うようにする必要がある。
FDの治療に、放射線治療は適応とはならない。FDの病変部位の放射線被曝は、悪性転化のリスクが考えられることから、制限する必要がある[Ruggieriら1994]。
甲状腺機能亢進症に対するラジオ波焼灼療法は、GNASの体細胞性機能亢進型病的バリアントを有する組織にラジオ波が優先的に取り込まれ、術後に残った非罹患腺組織中に悪性新生物が生じるリスクが高まる可能性があることから、通常は回避される。
リスクを有する血縁者の評価
FD/MASは遺伝性疾患ではないため、血族にリスクの高まりがみられることはなく、したがって、特段の評価は要しない。リスクを有する血縁者に対して行う遺伝カウンセリングを目的とした検査関連の事項については、「遺伝カウンセリング」の項を参照されたい。
妊娠に関する管理
FD/MASを有する女性の骨や内分泌の問題に対する妊娠の影響については、あまり研究が行われていないものの、著者らの知る限り、大多数の例については、妊娠中に疾患の悪化をきたすようなことはない。
研究段階の治療
さまざまな疾患・状況に対して進行中の臨床試験に関する情報については、アメリカの「ClinicalTrials.gov」、ならびにヨーロッパの「EUClinicalTrialsRegister」を参照されたい。
注:現時点で本疾患に関する臨床試験が行われているとは限らない。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
線維性骨異形成症/McCune-Albright症候群は遺伝性疾患ではない。
- これまでに垂直伝播の確認された例はみられない。
- 分子データの示すところによると、すべての罹患者は、胚発生初期に散発性に生じるGNASの機能亢進型病的バリアントをモザイクで有している。
家族構成員のリスク
発端者の両親
FD/MASを有する罹患児の親が本疾患の明瞭・明確な症候を有していた例はみられず、また、本疾患のもつ体細胞性の性格を考えると、そうしたことが実際に生じるとも考えにくい。
発端者の同胞
FD/MASの発症メカニズムは体細胞性変異であることから、同胞の罹患リスクは、一般集団と同等と考えられる。
発端者の子
FD/MASの垂直伝播の例は存在しない。胚性致死がその背景にある可能性も考えられる。
他の家族構成員
他の血族の有するリスクは、一般集団と同等である。
関連する遺伝カウンセリング上の諸事項
見かけ上denovoの病的バリアントのモザイクと思われる血縁者における考慮事項
FD/MASの再発リスクに関するカウンセリングにあたっては、妊娠に際しての本疾患の再発リスクはゼロではないものの、一般集団の数字を上回るものではないという点を強調する必要がある。
家族計画
罹患者である若い成人に対しては、遺伝カウンセリング(子に生じる可能性のあるリスクや、子を儲ける上での選択肢についての説明を含む)を提供することが望ましい。
DNAバンキング
検査の手法であるとか、遺伝子・病原メカニズム・疾患等に対するわれわれの理解が、将来はより進歩していくことが予想される。そのため、分子診断の確定していない(すなわち、原因となった病原メカニズムが未解明の)発端者のDNAについては、保存しておくことを検討すべきである。詳細については、Huangら[2022]を参照されたい。
出生前検査
FD/MASは、GNASに生じた接合後体細胞変異に起因するもので、遺伝性ではないため、FD/MASに関しては、出生前検査の対象とはならない。
関連情報
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- uropeanAssociationforMcCune-AlbrightSyndromeandOtherRareDiseases
- FD/MASAlliance
- FibrousDysplasiaSupportSociety
UnitedKingdom
Email:enquiries@FDSSUK.org.uk
www.fdssuk.org.uk - MAGICFoundation
- MedlinePlus
- PatiëntenverenigingFibreuzeDysplasie
Italy
Email:info@eamas.net
www.eamas.net
6645WestNorthAvenue
OakParkIL60302
Email:ContactUs@magicfoundation.org
McCune-Albright Syndrome / Fibrous Dysplasia
Netherlands
Email:info@fibreuzedysplasie.eu
www.fibreuzedysplasie.eu
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A:線維性骨異形成症/McCune-Albright症候群:遺伝子とデータベース
| 遺伝子 | 染色体上の座位 | タンパク質 | Locus-Specificデータベース | HGMD | ClinVar |
|---|---|---|---|---|---|
| GNAS | 20q13.32 | グアニン結合タンパク質Gsαサブユニットアイソフォーム短小型 | GNAS complex locus (GNAS) @ LOVD | GNAS | GNAS |
データは、以下の標準資料から作成したものである。
遺伝子についてはHGNCから、染色体上の座位についてはOMIMから、タンパク質についてはUniProtから。
リンクが張られているデータベース(Locus-Specific,HGMD,ClinVar)の説明についてはこちらをクリック。
表B:線維性骨異形成症/McCune-Albright症候群関連のOMIMエントリー(内容の閲覧はOMIMへ)
| 139320 | GNASCOMPLEXLOCUS;GNAS |
| 174800 | MCCUNE-ALBRIGHTSYNDROME;MAS |
遺伝子構造
GNASの座位は、インプリンティングの発現パターンを伴う複雑な座位である。4つのプロモーターと、下流の共通エクソン群にスプライシングを加える5’側エクソンが用いられることで、母性発現、父性発現、両アレル性発現の転写産物といった複数の遺伝子産物ができる[Weinsteinら2004](OMIM139320に要約されている)。GNASの主要な産物は、ユビキタスに発現するGsαで、これは最も下流にあるプロモーター(エクソン1)により産生される。遺伝子ならびにタンパク質に関する情報の詳細は、表Aの「遺伝子」の欄を参照のこと。
病的バリアント
これまでに報告されている全FD/MASの95%超で、p.Arg201の病的バリアントの体細胞モザイクが同定されている。そして、最も高頻度にみられる病的ミスセンスバリアントは、p.Arg201Hisとp.Arg201Cysである[Lumbrosoら2004]。ごく稀ではあるが、アルギニンがセリン、グリシン、ロイシンに置換されている例も報告されている。また、p.Gln227に生じたミスセンスバリアントも稀に報告される[Idowuら2007]。
現在、感度を高めた検出法の開発に向けた研究が進行中で[Biancoら2000,Narumiら2013,deSanctisら2017]、将来は、病的バリアントの検出に末梢血リンパ球(PBL)が使用できるようになる可能性があり、また、サンプル内における野生型に対する変異型の比率に関する定量(PCR-RFLP法での「あり-なし」の判定に代わって)もできるようになる可能性がある。
表4:GNASの体細胞性バリアントの検出法
| 方法 | 検出率 | |
|---|---|---|
| 血液 | 罹患組織 | |
| ポリメラーゼ連鎖反応(PCR)によるバリアント特異的増幅、ないし、 制限酵素消化(RFLP)法に続いて、バリアントの座位のダイレクトシーケンシングを施行1。 |
20%-30%近く | 80%近く |
| ペプチド核酸プローブを用いたPCR2と、次世代シーケンサー(PNA-NGS)との組合せ3。 | 75%近く | 100%近く |
| 低変性温度での共増幅とアレル特異的PCRベースのTaqManジェノタイピングの組合せ(リアルタイムCOLD-MAMA-PCR法)4 | 75%近く | 100%近く |
- Lumbrosoら[2004],Kalfaら[2006]
- Biancoら[2000]
- Narumiら[2013]
- deSanctisら[2017]
最近の研究で、FD/MASの病原として、GNASの選択的転写産物の関与が示唆されている。父性の病的バリアントを有する罹患者で、Gαsの大きな転写産物XLαsのp.Arg543Hisのバリアント(これは、Gαsにおけるp.Arg201Hisの位置に相当)が同定されている。一方、罹患組織中に母性の病的バリアントを有する罹患者で、変異した神経内分泌タンパク質55(NESP55)のバリアント転写産物が同定されている。野生型XLαsのinvitro機能アッセイでは、トランスフェクションが行われた細胞内においてアデニル酸シクラーゼ活性の強い誘導が明らかになっており、GNASのこのバリアントがFDの病原として一定の役割を果たしている可能性が示唆されている[Mariotら2011]。
表5:このGeneReviewで取り上げたGNASの体細胞性バリアント
| DNAヌクレオチドの変化 | 予測されるタンパク質の変化 | 参照配列 |
|---|---|---|
| c.601C>T | p.Arg201Cys | NM_000516.4 NP_000507.1 |
| c.601C>G | p.Arg201Gly | |
| c.601C>A | p.Arg201Ser | |
| c.602G>A | p.Arg201His | |
| c.602G>T | p.Arg201Leu | |
| c.679C>A | p.Arg227Lys | |
| c.680A>T | p.Arg227Leu | |
| c.680A>G | p.Arg227Arg | |
| c.681G>T | p.Arg227His |
バリアントの分類に関する注意事項:表中のバリアントは報告者の記載をそのまま載せたもので、GeneReviewsのスタッフが独自にバリアントの分類を検証したものではない。命名法に関する注意事項:GeneReviewsは、HumanGenomeVariationSociety(varnomen.hgvs.org)の標準命名規則に準拠している。
命名規則の説明については、QuickReferenceを参照のこと。
正常遺伝子産物
GNASは、cAMP経路関連Gタンパク質、Gsαをコードしている。Gsαは数多くのホルモン関連経路やシグナル伝達経路の重要な構成要素である。その主たる役割は、Gタンパク質共役型受容体をアデニル酸シクラーゼとカップリングさせ、受容体誘導型の細胞内cAMP産生を促進することである。Gsαは、不活性状態にある時はGsβ、Gsγサブユニットとヘテロ三量体を形成し、その結合部位にGDPが結合している。Gタンパク質共役型受容体にリガンドが結合すると、αサブユニットからのGDPの遊離やGTPの結合が促進される。GTPが結合したGsαは、β-γとのヘテロ三量体から離れて移動し、アデニル酸シクラーゼと相互作用してcAMPの産生を促進する。GTPは、内在するGTPaseによりGDPへと加水分解され、cAMPの産生が停止するとともに、α-β-γヘテロ三量体が再度形成される。cAMPは、数多くある組織依存性ホスホジエステラーゼの中の1つにより、下流でAMPへと代謝される。
異常遺伝子産物
GNASのp.Arg201とp.Gln227という2つの残基に生じるFD/MAS関連バリアントにより、内在性のGTPaseの活性が損なわれ、恒常的活動状態になってcAMPシグナル伝達が不適切な形で亢進することとなる[Landisら1989]。
FD/MASのスペクトラムは、何かのきっかけで偶然発見される無症状のものから、新生児致死性のものまで、幅がみられる。FD/MASの表現型は、その組織内でGsαの果たす役割の大小、ならびに、GNASの病的バリアントを有するのがどの組織なのかという条件によって決まってくる。また、どの組織が罹患部位となるかは、発生の過程において散発性の病的バリアントが発生する時期、ならびに、病的バリアントを有するクローンの運命によって決まる。組織によっては、変異したGsαに幹細胞が耐えることができず、発生過程で排除されることになるように思われる。したがって、Gsαシグナル伝達が重要な役割を果たす組織にあっては、その影響が及ばないということになる。例えば、成長板の発生において、Gsαシグナル伝達は重要ではあるものの、成長板が罹患部位となることは、事実上ない。
FD/MAS罹患者におけるGNASの活性化型すなわち機能獲得型病的バリアントはモザイク状態で存在する。これは、発生の初期過程で生じた接合後体細胞性病的バリアントが原因となって、罹患組織内に変異細胞のモノクローナルな集団ができ上がったことに起因するものである。機能亢進型病的バリアントの大多数は、非モザイク状態の場合、胚性致死となるものと推定される(OMIM174800より改変)。
癌ならびに良性腫瘍
非症候群性の良性腫瘍[Landisら1989]ならびに悪性腫瘍[Woodら2007]中に、GNASのp.Arg201、p.Gln227残基にFD/MAS関連の機能亢進型病的バリアント(これらを総称してgspがん遺伝子と呼ぶ)がみられたとの報告が存在する。ただ、GNASの病的バリアントが存在するということだけでは、罹患組織の悪性転化には十分ではなく、これとは別のゲノムあるいはエピゲノムのイベントが素因を形成している可能性が高い。
ence.2007;318:1108–13.[PubMed]
更新履歴:
-
Gene Reviews著者: AlisonMBoyce,MD,PabloFlorenzano,MD,LuisFdeCastro,PhD,andMichaelTCollins,MD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2019.6.27. 日本語訳最終更新日: 2023.4.23.[in present]