- 〒142-8555
- 東京都品川区旗の台1-5-8
- 昭和大学医学部顕微解剖学
- 本田一穂
- Tel: 03-3784-8103
- Fax: 03-3784-6815
- E-mail: kzhonda@med.showa-u.ac.jp
クイズ
Q5
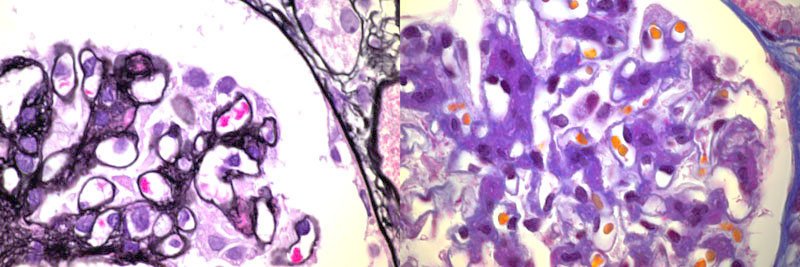
症例:関節リウマチ患者。考えられる疾患は。
Q5解説
慶應義塾大学 橋口明典
膜性糸球体腎炎(膜性腎症)およびIgA腎症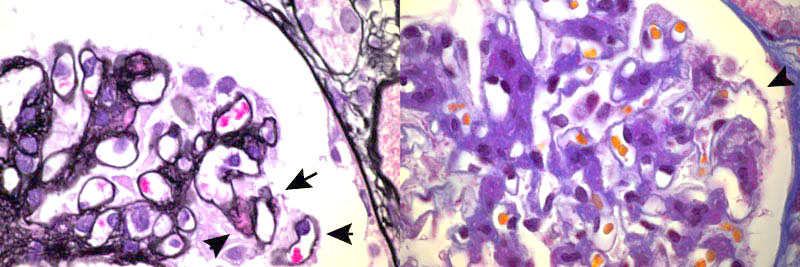 |
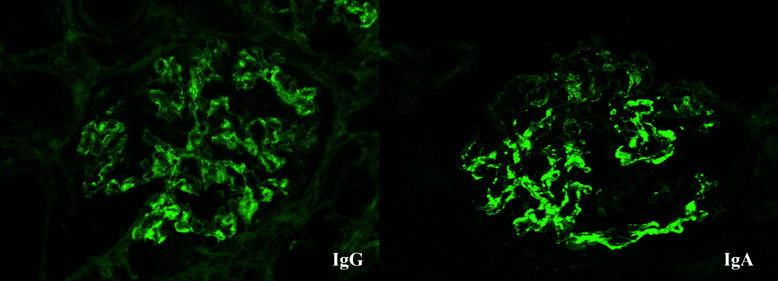 |
やや美しくない病変で恐縮であるが、メサンギウムへの粗大な沈着物と基底膜の変化に着目されたい。
関節リウマチ患者に生ずる腎病変について整理するのが、このクイズの目的である。
膜性腎症、IgA腎症、基底膜菲薄化症候群、他の膠原病の合併に伴う腎病変など。
Q4
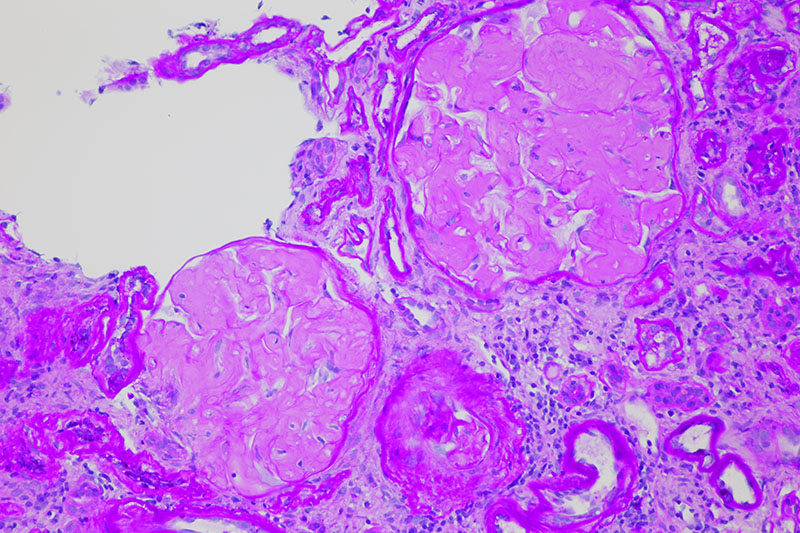
症例:70歳代、男性。30年来の糖尿病。最近になって、ネフローゼ症候群を発症した。
どのように鑑別を進めるか。
Q4解説
慶應義塾大学 橋口明典
Amyloidosisを疑い、Cong red 染色を行う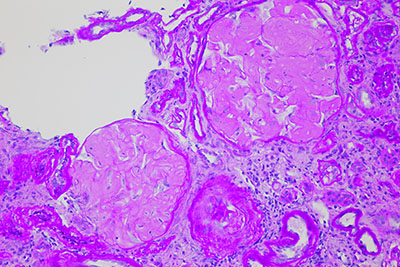 |
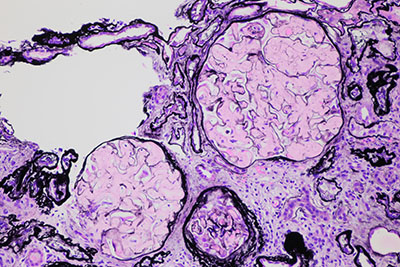 |
糸球体は結節状を呈しているが、PAS淡染性である。PAM染色で銀をとらない(Spiculaを除く)。
クイズそのものは簡単であるが、生検診断に必要ないくつかの要素がある。
糖尿病性腎症の患者さんは、糖尿病性腎症で説明できない臨床症候がある場合、生検されることが多い。
高齢者のネフローゼ症候群における鑑別診断。
いわゆる"Nodular glomerulosclerosis"の鑑別診断。
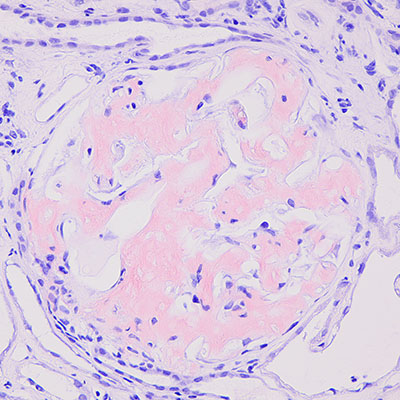 |
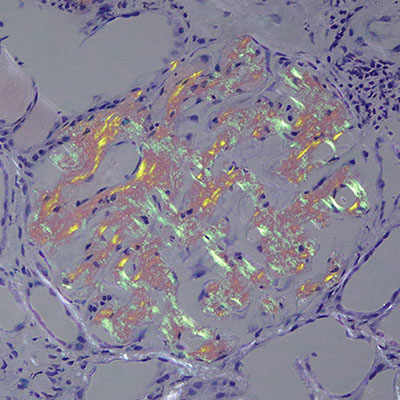 |
アミロイドの確定は必ず偏光板を用いた観察を行う。
偏光板を回していくと角度によって、赤や緑を呈する部が変化する。光量は普段よりも強い方がよい。切片は厚めに作製することが重要である。
本症例は容易な鑑別であるが、糖尿病患者の生検は、特に「糖尿病性腎症らしくない」症例が多いことから、複雑な「応用問題」になることが多い。
臨床症候と組織形態学を対応させ、複雑に絡み合った病変を紐解いていくことが重要である。
Q3
症例:透析患者の剖検腎
この結晶構造は?
(画像提供:立野 正敏先生 釧路赤十字病院病理診断科)
Q3解説
慶應義塾大学 橋口明典
透析患者、後天性多発性嚢胞腎でみられたシュウ酸塩結晶である。
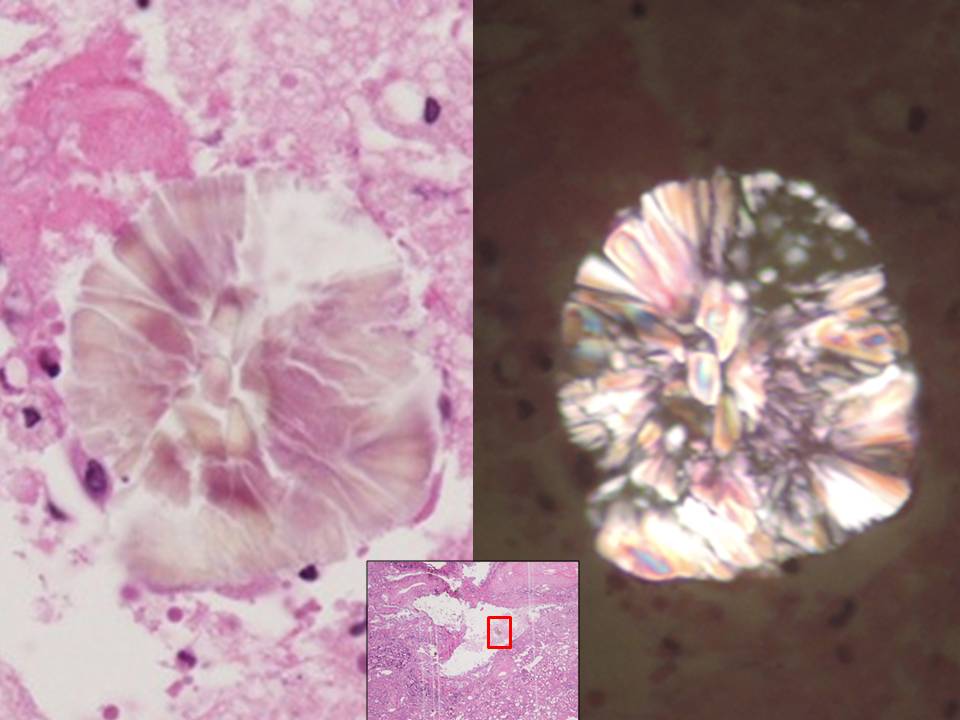 |
|
| HE | 偏光 |
腎、尿細管・間質には様々な結晶構造みられる。直接の診断に関与することはない場合が多いが、整理して置くことが重要であろう。偏光板は、アミロイドの確定に重要であるが、確認を怠っている病理医も少なからずみかける。常に使えるよう準備してあると便利である。
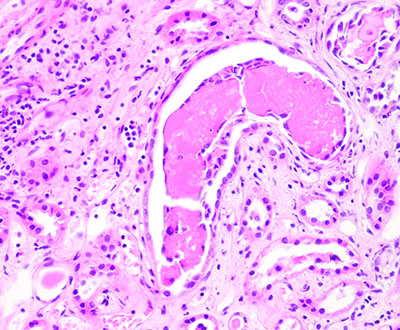 |
||
| 尿酸 | Tamm-Horsfall蛋白 | 骨髄腫腎 |
Q2
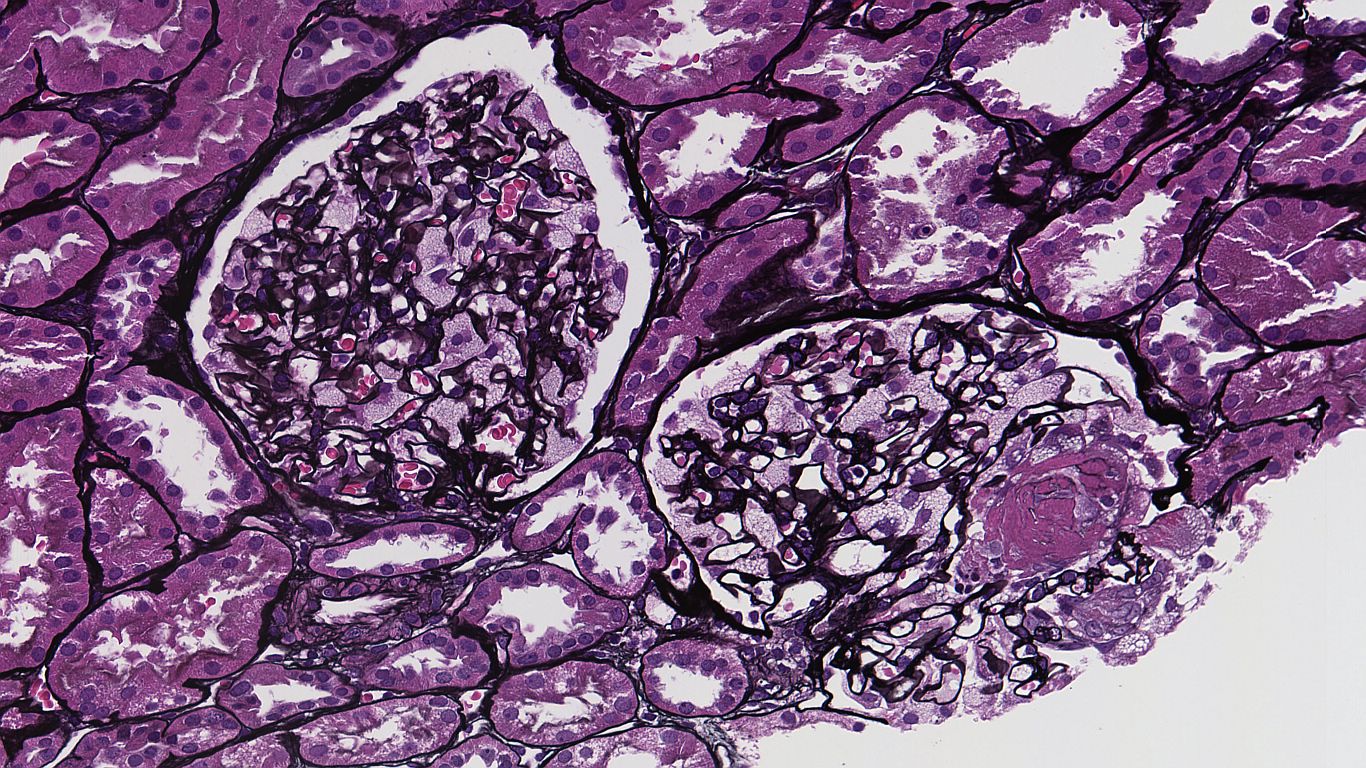
症例:29歳男性、Granulomatosis with polyangiitisを疑われ、生検となる。
壊死性糸球体腎炎を認め、同疾患と確定したが、背景にあった疾患は?
Q2解説
慶應義塾大学 橋口明典
答:Fabry病
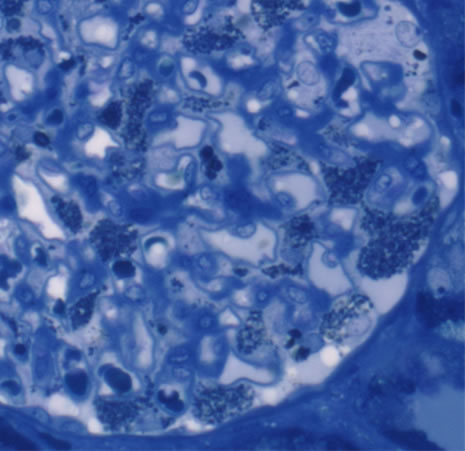
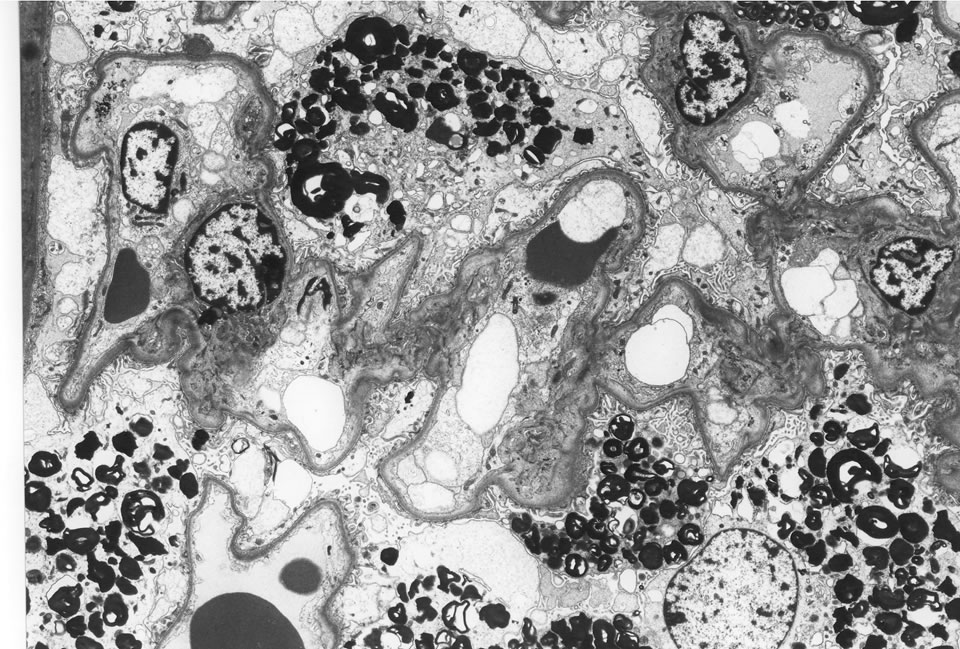
先入観を持たず、虚心坦懐に所見をとる、第三者的な姿勢が必要である。
上皮細胞の泡沫化が顕著であり、 電顕所見等から、最終的にFabry病の合併が確定した。
ANCA関連血管炎を疑い、半月体形成性・壊死性糸球体腎炎を認めるとそれで安心してしまいがちである。
患者の当面の予後には関係しないが、長期的に重要な情報を見落とすことになる。
確かにこのような合併は偶然ともいえ、つい、電子顕微鏡用の試料を採取するのも怠りがちであるが、故 田口 尚 先生のコラムにある通り、その必要性を改めて提起したい。
Q1
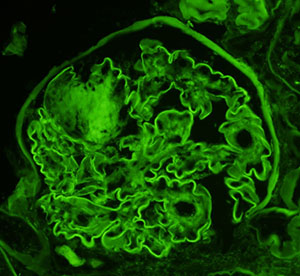
以下のいずれが最も適当か?
1.抗基底膜腎炎
2.膜性腎症
3.糖尿病性腎症
4.重鎖沈着症
5.膜性増殖性糸球体腎炎II型 (dense deposit disease)
Q1解説
筑波大学 長田道夫
こういった問題では、疾患を除外していくと整理しやすいと思います。 糸球体基底膜に沿って、IgGが陽性です。まず、DDDは、現在では補体制御の異常によって、補体の活性が亢進し、糸球体基底膜にC3が線状あるいはリボン状に沈着することが知られ、IgGをはじめとした免疫グロブリンは基本的には陰性ですので、除外可能です。基底膜は厚く正常のループパターンを描いてはいないことがまず目に入ります。これは、管内に病変があることを反映しています。染色パターンは線状かつ連続性で、顆粒状ではありません。顆粒状の場合は、膜性腎症の他、感染関連腎炎やMPGN3型などがまず考えられます。本例では同時に拡大した、あるいは結節を形成するメサンギウム基質にもやや薄く、しかし明らかな染色性が見られます。さらにボウマン嚢基底膜や尿細管基底膜にも陽性像を認めます。このIgGがcirculating immune complexであれば、このようなびまん性で、均一感のある沈着は呈しにくく、in situ immune complexなら、これだけの部分に同様(量)に抗体が結合する共通の物質が存在するはずであり、糸球体構造からすると考えにくいと思います。このような基本をまず踏まえて、この写真を見ます。抗基底膜抗体腎炎は、糸球体基底膜に存在するIV型collagenのa3鎖NC1domainに対する自己抗体がin situ immune complexを形成する機序で沈着します。したがって、沈着は線状になりますが、ボウマン嚢基底膜にはほとんど染まりません( 写真1 )。メサンギウム基質にも陰性であり、本問題の沈着パターンとは異なることがわかります。 また、背景の糸球体病変からは、糖尿病、重鎖沈着症(MPGNも)が鑑別に上がります。5時方向にはドーナッツ病変、11時方向にはKW結節が見られます。 さて、こからが、本問題のねらいです。今回はIgGだけを提示していますが、光顕では鑑別が難しい重鎖沈着症(HCDD)、糖尿病性腎症をIFで鑑別するために、何を調べればいいのか?これがポイントです。 HCDDは、稀な疾患ですが、IFで単クローン重鎖を証明することが必要になります。単クローン重鎖はIgGであればサブクラス(IgG1-4)がクロナリティーを持ち、軽鎖が欠損していることを、サブクラス染色、kappa, lambda染色に加えて、重鎖と軽鎖が結合する重鎖のCH1部、あるいはヒンジ部が欠損していることを、特異的抗体を用いて証明する必要があります。詳しくはOe et al, Clin Exp Nephrol. 2013 Dec;17(6):771-8.参照のこと。HCDDは、重鎖の種類によっては(IgG1、IgG3にそれが強い)補体結合部位を持つため( 表1 )、糸球体にC3が沈着し、低補体を呈することが知られています(サブクラスを特定する意義がここにあります)。また、電顕所見は特徴的なpowder-like沈着がみられることも鑑別点としては重要です ( 写真2 )。 本例は、糖尿病性腎症の患者のIF IgG所見であり、ネフローゼ症候群、補体正常、基底膜肥厚IgG線状沈着、メサンギウムや尿細管にも沈着していることなどから、いわゆる免疫複合体ではなく“染み込み様変化”として、透過性の高まった基底膜を中心にIgGが沈着しているものと考えられます。ただし、IgM, IgA,C3の沈着パターンも参考にすべきであり、できればkappa, lambdaが両方同様に陽性であることなどを確認できれば、診断はほぼ確定できると考えられます。この場合の軽鎖はIgGや他の免疫グロブリンの多クローンの軽鎖を一括して検出していると判断されます。糖尿病の際の電顕所見では、基底膜に沿って、高電子密度沈着物は認められず、傍メサンギウム領域に、密度のやや低い沈着が、なんとなく認められる、というのが一般的です。ただし、これも症例によって異なりますから、電顕写真を見ながら多様性を認識することも面白いと思います。 蛍光抗体法は、腎臓病の診断には非常に重要ですので、その質と信頼度は高くなくては診断に役立ちません。そう言う意味でも、IF標本の質が何より重要であることは言うまでもありません。
 |
 |
| 写真1.抗基底膜抗体腎炎のIgG染色パターン http://kidney2.blogspot.jp/2012/06/glomerulonephritis-quiz_22.html | 写真2.LCDD, HCDDでは、特徴的なpowder-likeな沈着が、lamina lala internaに帯状にみられる。 |
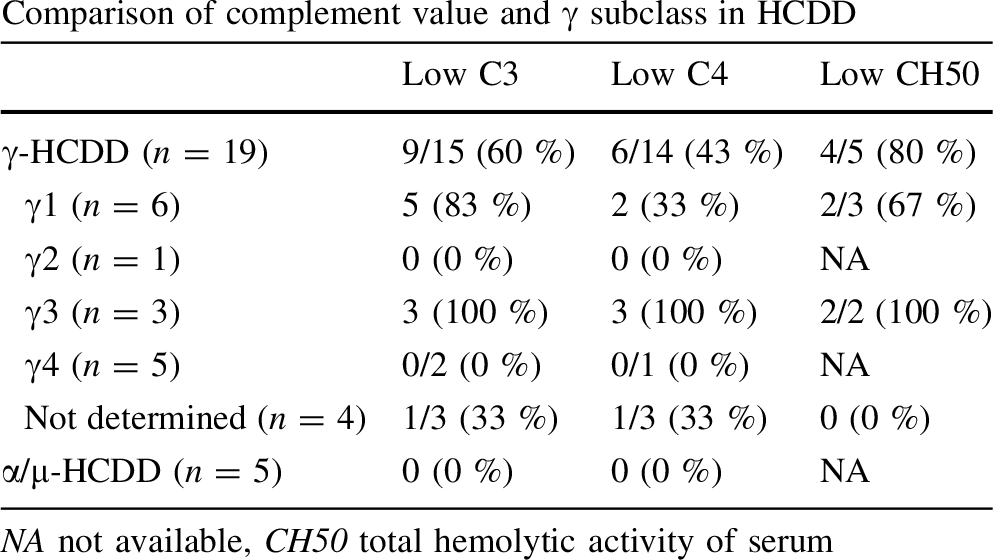
表1.重鎖沈着症では、約60%に低補体がみられるが、それは単クローンの重鎖によって補体結合能が異なるためと考えられる。γ1、γ3にその傾向が強いため、サブクラス染色を行い、補体活性とサブクラスの関連について調べると参考になる。(Oe et al, Clin Exp Nephrol. 2013 Dec;17(6):771-8.)
