捻曲性骨異形成症
(Diastrophic Dysplasia)
[Synonyms:Diastrophic Dwarfism]
Gene Reviews著者: Sheila Unger, MD and Andrea Superti-Furga, MD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2021.12.23. 日本語訳最終更新日: 2023.2.8.
要約
疾患の特徴
捻曲性骨異形成症(DTD)は、四肢の短小化、正常な頭のサイズ、ヒッチハイカー拇指、脊椎変形(脊柱側彎,過度の腰椎前彎、頸椎後彎)、変形と早発性変形性関節症を伴う大関節の拘縮を特徴とする。その他の典型的所見としては、手指の尺側偏位、第1・第2趾間のギャップ、内反足などがある。出生時に死亡に至る例も時にみられるものの、罹患者の大多数は新生児期を乗り切り、身体的制限はあっても正常な知能をもって発育する。
診断・検査
発端者におけるDTDの診断は、本疾患に特徴的な臨床症候とX線写真症候を有すること、ないしは分子遺伝学的検査でSLC26A2の両アレルに病的バリアントが検出されることをもって確定する。分子遺伝学的検査でSLC26A2の病的バリアントが検出されない稀な例については、線維芽細胞ないし軟骨細胞の生化学的検査を行うことも考えられる。
臨床的マネジメント
症候に対する治療:
乳児期の頸椎の手術は、脊髄圧迫の臨床症候あるいは神経生理学的症候がみられる場合に限って行う。早期に生じる関節拘縮については、理学療法で予防できる可能性がある。小児期においては、関節を正しい位置に保つとともに可動性を可能な限り維持するため、理学療法やギプス固定を行う。歩行が不可能になった場合は、内反足の外科的改善を行う。変形は再発しやすいため、整形外科手術は慎重に行う。重度の脊椎変形により呼吸障害や神経症状がみられるといった場合は別として、脊柱側彎に対する外科的改善は、思春期を過ぎてから行うことが推奨される。比較的若い成人については、疼痛軽減や可動性拡大を目的として、股関節・膝関節の全置換術を行う。嚢胞性の耳の腫脹については保存的治療を行う。
定期的追跡評価:
脊椎彎曲や関節拘縮に関し、年に1度のモニタリングを行う。
避けるべき薬剤/環境:
肥満は、大きな荷重関節に過大な負荷をかけることにつながるので、これを避ける。
遺伝カウンセリング
DTDは、常染色体潜性の遺伝形式をとる。両親がともにSLC26A2の病的バリアントをヘテロで有していることが判明している場合であれば、発端者の同胞は、受胎の段階で、罹患者である可能性が25%、無症状の保因者である可能性が50%、罹患者でも保因者でもない可能性が25%である。家系内に存在するSLC26A2の複数の病的バリアントが判明している場合は、リスクを有する血縁者に対する保因者検査や、出生前検査、着床前遺伝学的検査が可能である。
診断
捻曲性骨異形成症(DTD)に関する合意済の臨床診断基準は、今のところ公表されていない。ただ、嚢胞性の耳の腫脹がみられる場合、これが本疾患を強く示唆するものとなる。
本疾患を示唆する所見
以下のような臨床所見、X線写真所見を有する例については、DTDを疑う必要がある。
臨床所見
- 四肢の短小化
- 正常な頭のサイズ
- 体幹のわずかな短小化
- ヒッチハイカー拇指(図1)
- 指節間皮線の欠損を伴う指節癒合症
- 小さな胸郭
- 腹部の突出
- 大関節の拘縮
- 橈骨の脱臼
- 口蓋裂(罹患者の3分の1近くにみられる)
- 新生児期にみられる嚢胞性の耳の腫脹(罹患者の3分の2近くにみられる)
- 多くみられるその他の所見:手指の尺側偏位,第1・第2趾間のギャップ,内反足,前額部の平坦な血管腫
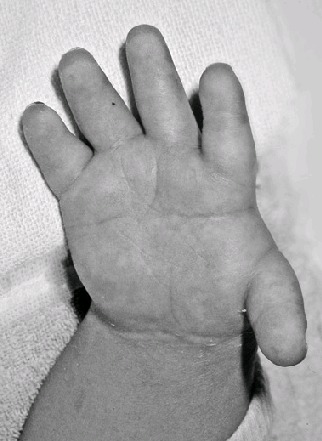
図1:捻曲性骨異形成症新生児の手
短指(指が短い状態)、指の指節間皮線の欠如、近位付着でかつ外転した「ヒッチハイカー拇指」。変形のため、拇指は握り合わせることができず、筆記や開栓といった動作に影響が及ぶ。X線写真所見
- 頭蓋の大きさは正常で、骨格が不均衡型の短縮を示す。
- 大多数の新生児や小児に頸椎後彎がみられる。
- 頸椎脊柱管の幅の拡大(「コブラ様」外観)を伴って、上部胸椎に骨化不全がみられる場合がある。
- 腰椎と下部胸椎に冠状裂がみられる場合がある。
- L1からL5にかけての椎弓根間距離の狭小化が常にみられる。
- 肋骨は頭側寄りほど短く、胸郭が釣り鐘状になることがある。
- 胸骨は、骨化核の重複を示すことがある。
- 腸骨は低形成で、寛骨臼は平坦になる。
- 長骨はいくぶん短小化傾向で、骨幹端はやや末広がりとなる。
- 上腕骨遠位端は、時に二分ないしV字形、時に低形成で尖形を呈する。
- 大腿骨遠位部は丸みを帯びる。
- 膝蓋骨は細片状ないし多層状にみえることがある。
- 橈骨や脛骨は彎曲することがある。
- 出生時に、橈骨近位関節の脱臼がみられることがある。
- 手は、特徴的形態を示すことがある(図2)。
- 第2-5指の尺側偏位を伴うヒッチハイカー拇指
- 第1中手骨の短小化
- Δ(デルタ)形の基節骨・中節骨
- 指節癒合
- 重度例の中には、新生児期に、骨年齢亢進を思わせるような2,3個の骨化した手根骨の出現を示す例がみられる。
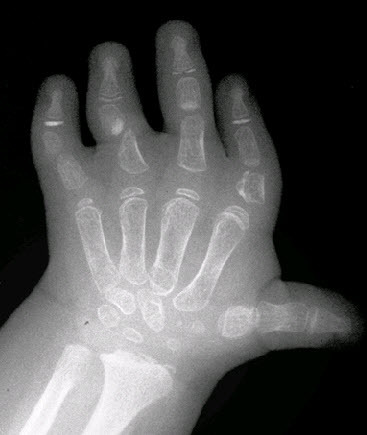
図2:捻曲性骨異形成症の3歳児の手のX線写真
指節骨は短く、一部、Δ(デルタ)形の変形を示すものがある。手根骨の骨化は年齢の割に進んでおり、骨年齢の「偽性亢進」として知られる現象を示骨年齢の高さはホルモンの状態とは関係がなく、捻曲性骨異形成症に内在する生化学的異常に伴うものであることが、「偽性」たる所以である。
診断の確定
発端者におけるDTDの診断は、「本疾患を示唆する所見」にある特徴的臨床症候とX線写真症候を示すこと、ないし分子遺伝学的検査にてSLC26A2の両アレルに病的バリアント(pathogenicとlikely pathogenicの両方を含む)が検出されることをもって確定する(表1参照)。
注:アメリカ臨床遺伝ゲノム学会(ACMG)のバリアントの解釈に関するガイドラインによると、「pathogenic」のバリアントと「likely pathogenic」のバリアントとは臨床の場では同義であり、ともに診断に供しうるものであると同時に、臨床的な意思決定に使用しうるものとされている。本セクションで「病的バリアント」と言うとき、それは、あらゆるlikely pathogenicまでを包含するものと理解されたい。
分子遺伝学的検査のアプローチとしては、表現型や臨床的状況に合わせて、遺伝子標的型検査(単一遺伝子検査、マルチ遺伝子パネル)と網羅的ゲノム検査(エクソームシーケンシング,ゲノムシーケンシング)を組み合わせるやり方が考えられる。
遺伝子標的型検査の場合、臨床医の側で関与が疑われる遺伝子の目星をつけておく必要があるが、ゲノム検査の場合、その必要はない。「本疾患を示唆する所見」に記載した特徴的所見を有する例については遺伝子標的型検査(「方法1」参照)で診断がつくものと思われるが、表現型だけではその他数多く存在する骨系統疾患と判別できないような例については、ゲノム検査(「方法2」参照)で診断がなされることになろう。
方法1
- 単一遺伝子検査
SLC26A2の配列解析を行うことで、遺伝子内の小欠失/挿入、ミスセンス・ナンセンス・スプライス部位バリアントが検出される。配列解析でバリアントが全く検出されない、あるいは1つしか検出されない場合、その次に行うステップは、通常エクソン単位あるいは遺伝子全体の欠失や重複を検出するための遺伝子標的型欠失/重複解析である。ただ、現在のところ、そうした欠失/重複により本疾患が生じたことが確認された例は存在しない。
- マルチ遺伝子パネル
現況の表現型と直接関係のない遺伝子の意義不明バリアントや病的バリアントの検出を抑えつつ、疾患の遺伝的原因を特定することに最もつながりやすいと思われるのは、SLC26A2ならびにその他の関連遺伝子(「鑑別診断」の項を参照)を含むマルチ遺伝子パネルである。
注:(1)パネルに含められる遺伝子の内容、ならびに個々の遺伝子について行う検査の診断上の感度については、検査機関によってばらつきがみられ、また、経時的に変更されていく可能性がある。
(2)マルチ遺伝子パネルによっては、このGeneReviewで取り上げている状況と無関係な遺伝子が含まれることがある。
(3)検査機関によっては、パネルの内容が、その機関の定めた定型のパネルであったり、表現型ごとに定めたものの中で臨床医の指定した遺伝子を含む定型のエクソーム解析であったりすることがある。
(4)ある1つのパネルに対して適用される手法には、配列解析、欠失/重複解析、ないしその他の非配列ベースの検査などがある。
マルチ遺伝子パネル検査の基礎的情報についてはここをクリック。遺伝学的検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
方法2
表現型からだけでは、その他の骨系統疾患と区別がつきにくいような場合であれば、網羅的ゲノム検査(この場合、臨床医の側で疑わしい遺伝子の目星をつけておく必要はない)が最適の選択肢となる。エクソームシーケンシングが広く用いられているが、ゲノムシーケンシングを使用することも可能である。
網羅的ゲノム検査の基礎的情報についてはここをクリック。ゲノム検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
表1:捻曲性骨異形成症(DTD)で用いられる分子遺伝学的検査
| 遺伝子1 | 方法 | その手法で病的バリアント2が検出される発端者の割合 |
|---|---|---|
| SLC26A2 | 配列解析3 | 90%超4 |
| 遺伝子標的型欠失/重複解析5 | 報告例なし6 |
- 染色体上の座位ならびにタンパク質に関しては、表A「遺伝子とデータベース」を参照。
- この遺伝子で検出されているバリアントの情報については、「分子遺伝学」の項を参照のこと。
- 配列解析を行うことで、benign、likely benign、意義不明、likely pathogenic、pathogenicといったバリアントが検出される。バリアントの種類としては、遺伝子内の小さな欠失/挿入、ミスセンス・ナンセンス・スプライス部位バリアントなどがあるが、通常、エクソン単位あるいは遺伝子全体の欠失/重複については検出されない。 配列解析の結果の解釈に際して留意すべき事項についてはこちらをクリック。
- SLC26A2の病的バリアントの中で最も多くみられる4種(p.Arg279Trp,c.-26+2T>C (IVS1+2T>C),p.Arg178Ter,p.Cys653Ser)で、DTDの疾患関連アレルの約65%を占める。DTDのX線写真所見や組織学的所見を有する例については、配列解析でアレルの90%が検出される[Rossi & Superti-Furga 2001]。
- 遺伝子標的型欠失/重複解析では、遺伝子内の欠失や重複が検出される。具体的手法としては、定量的PCR、ロングレンジPCR、MLPA法、あるいは単一エクソンの欠失/重複の検出を目的に設計された遺伝子標的型マイクロアレイなど、さまざまなものがある。
- データは、ヒト遺伝子変異データベース(HGMD)の購読ベースの専門家向けデータ[Stensonら2020]を基にしたもの。
その他の検査
病理組織検査
軟骨の状態は、病理組織学的には、軟骨マトリックス中に硫酸プロテオグリカンが少ないという点で、骨発生不全症2型(atelosteogenesis type 2;AO2)や軟骨無発生症1B型(achondrogenesis type1B;ACG1B)でみられるものと類似している。嚢胞状の無細胞領域と正常な細胞が存在する領域との中間部に、糸状の原線維を伴う異常な細胞外マトリックスが存在するといった形での、細胞外マトリックスの異常がみられる。一部の軟骨細胞は、同心円状の層状物質で取り囲まれているが、こうしたものは、症例によっては、ACG1Bでみられるコラーゲンリングと区別がつかないこともある。成長板は、柱状配列の乱れや、肥大細胞層への骨幹端毛細血管の不規則な侵入や線維化を示す。こうした軟骨マトリックスの異常は、長骨や、気管軟骨、喉頭軟骨、気管支周囲軟骨においてもみられるが、膜性骨の骨化に異常はみられない[Superti-Furga 2001,Superi-Furga 2022]。
生化学的検査
3H-グリシンと35S-硫酸ナトリウムの二重標識により、培養軟骨細胞ないし皮膚線維芽細胞において、高分子化合物への硫酸塩の取り込み状況を調べるといった検査も可能である。こうした化合物とインキュベーションを行って精製の後、培地中のプロテオグリカンの電気泳動を行うと、硫酸塩の取り込みがみられないことがわかる。全高分子化合物中への取り込みについてみても、やはり同様の所見が得られる。
注:(1)硫酸塩の取り込みの判定作業は煩雑であるため、これを診断目的に用いることはない。
(2)培養皮膚線維芽細胞(あるいは軟骨細胞)を用いた硫酸塩取り込みのアッセイは、DTDの診断が強く疑われるにもかかわらず、分子遺伝学的検査でSLC26A2に病的バリアントが検出されないといった稀な例においてのみ推奨される[Rossiら2003]。
臨床的特徴
臨床像新生児呼吸障害
捻曲性骨異形成症(DTD)の新生児は、小さな胸郭、ならびに気管の不安定性と易虚脱性のため、呼吸不全に陥りやすい。機械換気が必要となる乳児がかなりの割合に上る。誤嚥性肺炎等の肺炎をはじめとする呼吸器系の合併症を中心に、生後数ヵ月のうちに死亡する例も多い。
筋骨格症候
腱、靱帯、関節包が通常より硬く短いため、関節可動性の制限が生じる。Peltonenら[2003]は、膝関節半月板と十字靱帯の先天性無形成が多くみられることを報告している。子宮内運動の減少に起因するものと思われる脛骨前小陥凹がみられることもある。
関節拘縮や脊椎変形は、年齢とともに悪化していく傾向にある。若い成人には、有痛性の股関節変形性関節症が多くみられる。腰椎前彎の結果として骨盤の前傾が生じ、これがまた腰椎前彎を悪化させるという状況がみられることがある。脊椎は、過度の腰椎前彎、胸腰椎後彎、側彎といったものがしばしばみられる。腰椎X線写真前-後像において、椎弓根間距離の減少が必ずと言ってよいほどみられるが、それに関連した神経症状が現れることは稀である[Remesら2004,Shafiら2021]。
小児期には膝が不安定になることがある。進行性の外反膝や膝蓋骨外側偏位を伴いつつ、屈曲拘縮が進行する。膝蓋骨の発生状況や位置によって、大腿四頭筋の収縮が膝の伸展という形で正常に働くか、膝の屈曲という形で異常な働きをするかが決まる可能性がある。屈曲が生じるようであれば、歩行に重大な支障が生じることになる[Remesら2004]。
足の変形(内反足)と腱の短縮のため、DTDの成人の多くは踵を地面につけることができず、中足部とつま先だけで立つ形となる。
大きな機能障害を伴う第2-5指の短指、尺側偏位、指節癒合、強直がみられることがある。指節癒合は、多くの場合、基節骨と中節骨の間で生じ、出生時に、適切な大きさの関節腔をもたないいわゆるΔ(デルタ)形指節骨をはじめとする指節パターンの異常を示す指に発生する。DTDの新生児は、しばしば指節間皮線を欠くが(図1参照)、これは、発生の初期段階ですでに関節の可動性が顕著に失われていたことを示す1つのサインである。拇指は通常より近位に付着する場合があり、筋緊張が弱く、力が入らないことがある。その結果、一部の罹患者は拇指と人差し指を合わせて物をつまむ動作ができない。年長の小児や成人では、第2指の尺側偏位と同時に、しばしば第5指の橈側偏位(彎指)が生じ、特徴的な「()形[括弧形]」外観を呈する。
骨格異常に加えて、大腿・下肢の筋に軽度の低形成が多くみられる。
顔面症候
額は、前頭部毛髪線が高く、横幅も広い。眼瞼裂は斜下することがある。鼻は長く、鼻翼の低形成を伴って、厚みが薄い。顔面の組織は緊張が強い。口は小さく、下顎の発達は正常である。嚢胞性の耳の腫脹がしばしばみられ、炎症や疼痛を伴うことがある[Cushingら2011]。
成人期の身長
アメリカ人とヨーロッパ人のDTD罹患者を調べた初期のレビューでは、成人期の身長は100cmから140cmの間とされていた。1982年の研究で、成人期の平均身長は118cmと報告されている[Horntonら1982]一方で、フィンランド人DTD罹患者(SLC26A2の座位に関して遺伝学的に均質な試料)の研究では、成人期の平均身長は男性で136cm、女性で129cmとされている[Mäkitie & Kaitila 1997]。古い研究と新しいフィンランドの研究との間にみられる平均身長の差は、バリアントの異質性の違いに起因するものであるかもしれないし、また、古いほうの研究の試料が重症例の側に偏った確認バイアスに起因するものである可能性も考えられる。こうした成長曲線を成人期の身長の予測に用いるにあたっては、多くの異なるアレルの組み合わせが存在するため、その有用性には限界があることに注意が必要である。
神経関連の合併症
特に頸椎領域を中心に、神経関連の合併症が生じることがある。側面X線写真で、大多数の新生児に頸椎後彎がみられる。脊椎後彎は、多くの場合、3歳から5歳にかけ、次第に軽度になっていく。ただ、一部には、重度の脊椎後彎により脊髄圧迫に至ることもある。これは、自然にそうなる例もあれば、頸部の過伸展を要する気管内挿管時にこれが生じることもある。重度の脊柱後彎を有するDTDの1新生児で、呼吸不全のため出生直後に死亡した例がある。この例では、出生前に発生していた頸髄の神経細胞変性とグリオーシスが剖検で明らかになっている。
DTD罹患者について行ったMRIで、大孔の大きさに異常はみられないものの、頸椎の脊柱管が狭小化していることが確認されている。個々の頸椎の椎体(通常はC3からC5)は低形成であるものの、しばしばみられる後彎の成因はこうした椎体の変形では説明がつかず、椎間板の異常が背景にある可能性も考えられる。頸椎後彎については、自然に改善する率が比較的高い。MRIでは、椎間板に水分量の減少をうかがわせる信号異常がみられることが判明している。この信号異常はプロテオグリカンの硫酸化障害に起因するもののように思われる。
DTD罹患者では、頸椎の潜在性二分脊椎がしばしば報告されている。
精神発達と知能
精神発達や知能に異常はみられない。数多くのDTD罹患者が、学術的、社会的に高い評価を得たり、芸術分野で成功を収めたりしている。
難聴
DTD罹患者に難聴が現れることは多くないが、少数のコホートを用いた研究では、難聴が過大に評価される危険性が考えられる[Tunkelら2012]。
視覚障害
視覚障害はほとんどみられないが、近視の傾向を指摘した報告が存在する。
遺伝型-表現型相関
疾患のスペクトラムは、致死性の軟骨無発生症1B型(ACG1B)から軽度型の多発性骨端異形成症潜性型(EDM4/rMED)(訳注:「multiple epiphyseal dysplasia, autosomal recessive」を略したのが「rMED」、「EDM4」はOMIMの分類に従った名称で「epiphyseal dysplasia, multiple, 4」の略)まで大きな幅を示すが、遺伝型-表現型相関として言われていることは、残存している硫酸イオントランスポーター活性の大小によって表現型が決まってくるということである。ACG1Bを引き起こすのは、停止コドンが予測される病的バリアント、あるいは硫酸イオントランスポーターの膜貫通ドメインの構造に係わる病的バリアントのホモ接合ないし複合ヘテロ接合である。一方、軽度型の表現型を引き起こすのは、細胞外ループ内の病的バリアント、タンパク質の細胞質尾部の病的バリアント、遺伝子の5’隣接調節領域の病的バリアントといったものである[Superti-Furgaら1996,Karniskiら2001,Maedaら2006]。
フィンランド以外の地域でSLC26A2のバリアントとして最も多くみられる(アレルの45%)のは、p.Arg279Trpの病的バリアントである。これは、ホモ接合の場合は軽度型のEDM4の表現型となり、複合ヘテロ状態の場合は、ほとんどがDTDならびに骨発生不全症2型(AO2)の表現型となる[Barbosaら2011]。
p.Arg178Terの病的バリアントはその次に多くみられる(アレルの9%)バリアントで、p.Arg279Trpバリアントとトランスで組み合わさった場合などは特に、比較的重度型のDTDとして現れたり、周産期致死性のAO2の表現型として現れるようなこともある。
3番目に多いのは、p.Cys653Ser、ならびにc.-26+2T>Cの病的バリアントである(アレルの8%)。
p.Cys653Serは、ホモ接合の場合はEDM4/rMED、他の病的バリアントがトランスでみられる場合はEDM4/rMEDもしくはDTDとなって現れる[Czarny-Ratajczakら2010]。
c.-26+2T>Cの病的バリアントは、フィンランドでの出現がフィンランド以外の全世界での出現を上回るため、時に「フィンランド型」バリアントと呼ばれることもある。
これにより正しくスプライスされたmRNAの量が減少し、ホモ接合の場合はDTDとなって現れる。これは、軽度型(EDM4/rMEDとDTD)アレル、あるいは重度型(AO2とACG1B)アレルとの複合ヘテロ接合の形で、SLC26A2関連疾患の4つの型すべてで同定されている唯一のバリアントである[Dwyerら2010]。
ACG1Bの表現型でみられるのと同一の病的バリアントが、より軽度の表現型(AO2やDTD)においてもみられることがある。それは、他方のアレルが比較的軽度のバリアントだった場合である。実際に、硫酸イオントランスポーターの膜貫通ドメインの外側のミスセンスバリアントについては、いくぶんかの活性が残ることがしばしばあり、ヌルアレルの影響を「救済」しうる可能性をもつ[Rossi & Superti-Furga 2001]。
命名法について
DTDを独立疾患として認識したのは、Lamy & Maroteaux [1960]である。彼らはこの論文で、「新生児期には軟骨無形成症に似るが、その後は全く異なる経過をたどる」1疾患を報告した。捻曲性骨異形成症という名称は、重度罹患例において脊椎や四肢が「捻れた」ような外観を呈することを表現するために選ばれたものである。捻曲性骨異形成症の臨床症候、X線写真症候は非常に特徴的であるため、本疾患には別の名称は存在しない。
臨床症候には広いばらつきの幅が存在することが早くから認識されていた。「重度」あるいは「致死性」DTDの例は、現在では骨発生不全症2型(AO2)として分類され、より軽度の例については、かつては「捻曲性バリアント」と呼ばれたが、現在では多発性骨端異形成症潜性型(EDM4/rMED)として分類されている。
DTDは、現行の「骨系統疾患国際分類」では「硫酸化障害」グループに分類されている[Mortierら2019]。
頻度
DTDの発生頻度に関する信頼性のあるデータは存在しない。DTDの発生頻度を他の遺伝性疾患の発生頻度と比較しうるだけの規模をもった遺伝性・代謝性疾患センターの経験値で言うと、一般に、DTDはだいたい100,000人に1人程度のレベルであろうと考えられている。
遺伝学的に関連のある疾患(同一アレル疾患)
捻曲性骨異形成症(DTD)は、SLC26A2関連常染色体潜性骨疾患のスペクトラムにあって、重度型表現型に分類されるものの1つである(表2)。
表2:SLC26A2関連骨疾患のスペクトラム
| 疾患名1 | コメント |
|---|---|
| 軟骨無発生症1B型 |
|
| 骨発生不全症2型 |
|
| 捻曲性骨異形成症 | 本GeneReviewで取り扱っているもの。 |
| 多発性骨端異形成症,潜性型(かつては「捻曲性バリアントと呼ばれた」) |
|
- 疾患の掲載順は、重症度の高いものから低いものへの順とした。
鑑別診断
出生前の段階における要鑑別疾患としては、SLC26A2関連骨疾患スペクトラム(表2参照)、その他の骨系統疾患、ならびに、体長の減少や拘縮を呈する疾患を含める必要がある(表3参照)。
注:拇指の橈側偏位(ヒッチハイカー拇指)は捻曲性骨異形成症(DTD)を示唆する所見ではあるが、DTDに特異的な所見というわけではない。
表3:捻曲性骨異形成症との鑑別診断に関係してくる遺伝子
| 遺伝子 | 疾患名 | 遺伝形式 | DTDと重なる症候 |
|---|---|---|---|
| BPNT2 (IMPAD1) |
軟骨異形成症gPAPP型 | AR | 新生児,乳児にみられる手根骨の早期骨化と指趾奇形。 |
| CANT1 XYLT1 |
Desbuquois骨異形成症 (OMIM PS251450) |
AR | |
| ERGIC1 LGI4 SCYL2 SYNE1 TOR1A |
先天性多発性関節拘縮症 | AR | 先天性の拘縮がみられるものの、骨格奇形は軽度。 |
| FLNA | X連鎖性耳口蓋指スペクトラム障害 | XL | 新生児,乳児にみられる手根骨の早期骨化と指趾奇形。 |
| FLNB | Larsen症候群/骨発生不全1型スペクトラム(「FLNB疾患」のGeneReviewを参照) | AD | |
| FZD2 GPC6 |
肩骨異形成症(OMIM PS258315) | AD AR |
DTDを思わせる拘縮と中間肢節短縮。 |
AD=常染色体顕性;AR=常染色体潜性;XL=X連鎖性
臨床的マネジメント
最初の診断に続いて行う評価
捻曲性骨異形成症(DTD)と診断された罹患者については、疾患の範囲やニーズを把握するため、診断に至る過程ですでに実施済でなければ、表4にまとめた評価を行うことが推奨される。
表4:捻曲性骨異形成症罹患者の最初の診断後に行うことが推奨される評価
| 系/懸念事項 | 評価 | コメント |
|---|---|---|
| 呼吸器 | 呼吸数、ならびに誤嚥の徴候に関するチェック | 何らかの懸念がある場合は、小児呼吸器科医へ紹介する。 |
| 筋骨格 | 頸部のX線写真(前後像,側面像,屈曲時,伸展時) | |
| 骨格に関する詳細な調査 | 診断に至る前の段階で行っていなかった場合。 | |
| 整形外科医への紹介 | ||
| 理学療法への紹介 | ||
| 遺伝カウンセリング | 遺伝の専門医療職1の手で行う。 | 医学的、個人的な意思決定の用に資するべく、本人や家族に対し、DTDの本質、遺伝形式、そのもつ意味についての情報提供を行う。 |
1.臨床遺伝医、認定遺伝カウンセラー、認定上級遺伝看護師をいう。
症候に対する治療
表5:捻曲性骨異形成症罹患者の症候に対する治療
| 症候/懸念事項 | 治療 | 考慮事項/その他 |
|---|---|---|
| 頸椎後彎 | 乳児期の頸椎の手術は、脊髄圧迫の臨床症候あるいは神経生理学的症候がみられる場合に限って行う。 | 自然に改善する率が比較的高い。 |
| 拘縮 |
|
関節包や靱帯が硬いと、ギプスやその他の物理的手段での改善が難しくなる。 |
| 内反足 | 足の変形により歩行不能の場合、外科的改善が適応となる。 |
|
| 脊柱側彎 | 整形外科の専門医による治療1 |
|
| 早発性の変形性関節症 | 関節形成術 | フィンランド人成人群で、股関節・膝関節全置換術により、疼痛の軽減と可動性の改善が報告されている[Heleniusら2003a,Heleniusら2003b]。 この著者らは、「比較的若い成人」のDTD罹患者については関節形成術が適応となると結論づけている。 |
| 嚢胞性の耳の腫脹 | 保存的治療 | Cushingら[2011] |
- 手術的改善の適応についても、また、手術を成功とする基準についても、今のところ確立されたものは存在しない[Matsuyamaら1999,Remesら2001]。手術を受けた群は、必然的に重度例のほうに偏っていることに注意が必要である。大切なことは、側彎の彎曲度が急激に悪化していく罹患者を早期に特定することであるように思われる。
定期的追跡評価
表6:捻曲性骨異形成症罹患者で推奨される定期的追跡評価
| 系/懸念事項 | 評価 | 実施頻度 |
|---|---|---|
| 筋骨格 |
|
年に1度 |
避けるべき薬剤/環境
肥満は、大きな荷重関節に過大な負荷をかけることにつながるので、これを避ける。
リスクを有する血縁者の評価
リスクを有する血族に対して行う遺伝カウンセリングを目的とした検査関連の事項については、「遺伝カウンセリング」の項を参照されたい。
妊娠に関する管理
DTD特異的というわけではないが、重度の脊柱後側彎を有する女性は、妊娠の後半で胸髄圧迫関連の合併症をきたす可能性があるため、注意深く追跡評価を行うことが必要である。脊柱後側彎は、脊髄くも膜下麻酔にあたって合併症を引き起こす可能性があるため、分娩に先立って麻酔科医と十分に話し合っておくことが推奨される。
妊娠中に使用する薬剤に関するその他の情報については、「MotherToBaby」を参照されたい。
研究段階の治療
さまざまな疾患・状況に対して進行中の臨床試験に関する情報については、アメリカの「Clinical Trials.gov」、ならびにヨーロッパの「EU Clinical Trials Register」を参照されたい。
注:現時点で本疾患に関する臨床試験が行われているとは限らない。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
曲性骨異形成症(DTD)は、常染色体潜性の遺伝形式をとる。
家族構成員のリスク
発端者の両親
- 罹患児の両親は、絶対ヘテロ接合者である(すなわち、SLC26A2に関するそれぞれの家系固有の病的バリアントを1つ有する保因者と目される)。
- 発端者について分子遺伝学的診断が確定している場合は、発端者の両親についても分子遺伝学的検査を行って、両者ともSLC26A2の病的バリアントをヘテロで有していることを確認し、信頼性のある再発リスク評価につなげることが推奨される。もし、病的バリアントが片親からしか検出されず、しかも、親子鑑定の結果、真正の生物学的父・母であることが確認されているということであれば、可能性として次のようなことが考えられる。
- 発端者で同定された病的バリアントのうちの1つが、発端者にde novoのイベントとして生じた可能性、もしくは、モザイクの片親において、接合後のde novoのイベントとして生じた可能性[Jónssonら2017]。
- 病的バリアントを有しているほうの片親の染色体に片親性ダイソミーが生じて、発端者が病的バリアントのホモ接合を有するに至った可能性。
- ヘテロ接合者(保因者)は通常、無症状で、身長も正常である。保因者について、変性関節疾患に至るリスクが高いというデータも存在しない。
発端者の同胞
- 両親とも、SLC26A2の病的バリアントをヘテロで有していることが判明している場合、罹患者の同胞は、受胎の段階で、罹患者である可能性が25%、無症状の保因者である可能性が50%、罹患者でも保因者でもない可能性が25%である。
- ヘテロ接合者(保因者)は通常、無症状で、身長も正常である。
発端者の子
DTD罹患者の子は、SLC26A2の病的バリアントに関し、絶対ヘテロ接合者(絶対保因者)となる。
他の家族構成員
発端者の両親の同胞はそれぞれ、SLC26A2の病的バリアント保因者であることに関し、50%のリスクを有する。
保因者の検出
リスクを有する血縁者に対して保因者の検査を行うためには、家系内に存在するSLC26A2の病的バリアントを事前に同定しておくことが必要となる。
ヘテロ接合者の生殖上のパートナーについては、保因者の検査を行うことが可能である。
関連する遺伝カウンセリング上の諸事項
家族計画
- 遺伝的リスクの確定、出生前/着床前遺伝子検査を受けるかどうかの話し合いに最も適しているのは、妊娠前の時期である。
- 罹患者、保因者、あるいは、保因者であるリスクを有する若い成人に対しては、遺伝カウンセリング(子に生じる可能性のあるリスクや、子を儲ける上での選択肢についての説明を含む)を提供することが望ましい。
DNAバンキング
検査の手法であるとか、遺伝子・病原メカニズム・疾患等に対するわれわれの理解が、将来はより進歩していくことが予想される。そのため、分子診断の確定していない(すなわち、原因となった病原メカニズムが未解明の)発端者のDNAについては、保存しておくことを検討すべきである。
出生前検査ならびに着床前遺伝学的検査
高リスクの妊娠
分子遺伝学的検査
家系内に存在するSLC26A2の病的バリアントが同定されている場合は、出生前検査や着床前遺伝学的検査を行うことが可能である。
超音波検査
DTD胎児の大多数は、超音波検査で確認可能な何らかの奇形を有している。ただ、再発リスクを避けるための診断手法としては、超音波検査は信頼に値しない。
「低リスクの妊娠」の「ルーチンで行う超音波検査」の「注」を併せて参照されたい。
低リスクの妊娠
ルーチンで行う超音波検査
ルーチンで行われた超音波検査の結果、胎児の四肢短小、羊水過多、小さな胸郭といったことが明らかになり、もともと有リスクと思われていなかった胎児にDTDの可能性が生じることがある。拇指の橈側偏位(「ヒッチハイカー拇指」)は、DTD特異的所見ではないものの、DTDを示唆する所見ではある。第1三半期の段階で行った超音波検査でごく軽微な所見が見つかるようなこともあろうが、低リスクの妊娠における骨系統疾患の診断は、ふつう、第2三半期になるまで行うことができない。
注:超音波検査でDTDの早期発見に「成功」したとする文献が散見されるものの、文献として現れているものは、結果として陽性であったものに大きく偏したバイアスがかかっている[Tongsongら2002,Severiら2003,Waxら2003]。著者ら自身の経験では、低リスクの妊娠において超音波検査でDTD胎児が正しく判定された例はごく少数であり、大多数は、どの疾患とも特定できないものの何らかの骨系統疾患がありそうといった診断や、DTD以外の何らかの疾患であるといった診断がなされている。
分子遺伝学的検査
DTDが疑われた場合に出生前の段階で行う分子レベルの解析は、包括的パネル検査(骨系統疾患用ならびに関節拘縮症用)、エクソームシーケンシング、ゲノムシーケンシングとすべきである。
関連情報
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- MedlinePlus
- American Cleft Palate-Craniofacial Association
Phone: 919-933-9044
Fax: 919-933-9604
Email: info@acpa-cpf.org
www.acpa-cpf.org
- Child Growth Foundation
United Kingdom
Phone: 0208 995 0257
Email: nfo@childgrowthfoundation.org
www.childgrowthfoundation.org
- Face Equality International
United Kingdom
Email: info@faceequalityinternational.org
www.faceequalityinternational.org
- Human Growth Foundation
- Little People of America
Phone: 888-LPA-2001; 714-368-3689
Fax: 707-721-1896
Email: info@lpaonline.org
www.lpaonline.org
- MAGIC Foundation
Phone: 800-362-4423; 630-836-8200
Fax: 630-836-8181
Email: contactus@magicfoundation.org
www.magicfoundation.org
- UCLA International Skeletal Dysplasia Registry (ISDR)
Phone: 310-825-8998
International Skeletal Dysplasia Registry
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A:捻曲性骨異形成症:遺伝子とデータベース
| 遺伝子 | 染色体上の座位 | タンパク質 | HGMD | ClinVar |
|---|---|---|---|---|
| SLC26A2 | 5q32 | 硫酸イオントランスポーター | SLC26A2 | SLC26A2 |
データは、以下の標準資料から作成したものである。遺伝子についてはHGNCから、染色体上の座位についてはOMIMから、タンパク質についてはUniProtから。リンクが張られているデータベース(Locus-Specific,HGMD,ClinVar)の説明についてはこちらをクリック。
表B:捻曲性骨異形成症関連のOMIMエントリー(閲覧はすべてOMIMへ)
| 222600 | DIASTROPHIC DYSPLASIA; DTD |
| 606718 | SOLUTE CARRIER FAMILY 26 (SULFATE TRANSPORTER), MEMBER 2; SLC26A2 |
分子レベルでの病原
SLC26A2の病的バリアントが原因となって、軟骨無発生症1B(ACG1B)、骨発生不全症2型(AO2)、捻曲性骨異形成症(DTD)、潜性型多発性骨端異形成症(rMED/EDM4)など、一連の軟骨異形成症ファミリーが発生する。軟骨細胞や線維芽細胞中の硫酸イオントランスポーター活性が低下すると、硫酸化されていない、もしくは硫酸化の不完全なプロテオグリカンが合成されることになる[Rossiら1998,Satohら1998]。その背景として、細胞内の硫酸枯渇が係わっている可能性が高いように思われる[Rossiら1996,Gualeniら2010]。プロテオグリカンの低硫酸化は、細胞外マトリックスの組成に影響を及ぼすことになり、軟骨内骨化が正常に進んでいく上で必要なプロテオグリカンの沈着が障害を受ける結果となる[Corsiら2001,Forlinoら2005,Dawsonら2011]。臨床的重症度は、病的バリアントそれぞれの、残存硫酸イオントランスポーター活性の大小と相関している可能性が考えられる[Rossiら1996,Rossiら1997,Corsiら2001,Rossi & Superti-Furga 2001,Rossiら2003,Karniski 2004,Maedaら2006]。
アフリカツメガエル卵母細胞モデルにて、p.Arg178Terの病的バリアントにより硫酸イオントランスポーター活性が完全に失われること、p.Val341delの病的バリアントにより、検出可能なレベルは保たれるものの、硫酸イオントランスポーター活性が非常に低レベル(野生型の17%)になることがわかっている[Karniski 2001]。ACG1Bの表現型を示す罹患者でみられるものと同じバリアントが、より軽度の表現型(AO2やDTD)でもみられることがある。その場合は、他方のアレルが比較的軽度のバリアントになっている。実際に、膜貫通ドメインの外側の部分のミスセンスバリアントでは、いくらか活性が残存することが多く、言わばヌルアレルの影響をこれが「救済する」形となる。アフリカツメガエルにおけるその他の研究結果は、ヒトでみられる臨床的状況と一致しない部分がある。そうした相違は、おそらく、アフリカツメガエル卵母細胞とヒト卵母細胞との温度差(20℃と37℃)や細胞調整の違いといったところに起因するものであろうと思われる[Superti-Furgaら1996,Rossi & Superti-Furga 2001,Superti-Furga 2001,Superti-Furga 2002]。一方、哺乳類の細胞を用いて行われた同様の研究[Karniski 2004]では、ヒトでみられる遺伝型-表現型相関に非常に近い結果が得られている。こうした研究でわかった重要な点は、ACG1Bを引き起こすバリアントではトランスポーターとしての活性が全く残っていない一方で、軽度型の表現型の場合は、一方はヌルアレル、他方はいくらか活性が残るアレルというという組み合わせか、もしくは、両アレルとも活性が残るという組み合わせのどちらかだということである。オリジナルの論文で出された結論は以下のようなものである。
(1)p.Gly678Valのバリアントでは、細胞内に硫酸イオントランスポータータンパク質が残る。
(2)p.Gln454Proについては、硫酸イオントランスポーター分子量に異常が生じ、これがおそらくプロテアーゼの感受性の変化、ないしグリコシル化異常を招いている。
疾患の発症メカニズム
機能喪失型である。
表7:SLC26A2の注目すべき病的バリアント
| 参照配列 | DNAヌクレオチドの変化(別表記1) | 予測されるタンパク質の変化(別表記1) | コメント[参考文献] |
|---|---|---|---|
| NM_000112.3 | c.-26+2T>C (IVS1+2T>C) |
-- | フィンランドでみられる創始者バリアント。SLC26A2関連の4型すべてで確認される唯一のバリアント。rMEDとDTDでは軽度型アレルとの複合ヘテロ接合、AO2とACG1Bでは重度型アレルとの複合ヘテロ接合を示す[Dwyerら2010]。 |
| NM_000112.3 NP_000103.2 |
c.532C>T (559C>T) |
p.Arg178Ter | 2番目に多くみられるバリアント(アレルの9%)。p.Arg279Trpとトランスで組み合わさった場合は特に、比較的重度型のDTDや周産期致死性のAO2の表現型として現れる。 |
| c.835C>T (c.862C>T) |
p.Arg279Trp | フィンランド以外では、このバリアントが最も多くみられる(アレルの45%)。ホモ接合の場合は軽度型のEDM4、複合ヘテロ状態の場合はほとんどがDTDやAO2となる[Barbosaら2011]。 | |
| c.1020_1022delTGT (1045-1047delGTT) |
p.Val341del (Val340del) |
「分子レベルでの病原」の項を参照。 | |
| c.1361A>C (1388A>C) |
p.Gln454Pro | 「分子レベルでの病原」の項を参照。 | |
| c.1957T>A (1984T>A) |
p.Cys653Ser | 3番目に多くみられるバリアント(アレルの8%)。ホモ接合の場合はEDM/rMED、他の病的バリアントとトランスで組み合わさった場合はEDM/rMEDあるいはDTDとなる[Czarny-Ratajczakら2010]。 | |
| c.2033G>T (2060G>T) |
p.Gly678Val | 「分子レベルでの病原」の項を参照。 |
上記のバリアントは報告者の記載をそのまま載せたもので、GeneReviewsのスタッフが独自に変異の分類を検証したものではない。GeneReviewsは、Human Genome Variation Society(varnomen.hgvs.org)の標準命名規則に準拠している。
命名規則の説明については、Quick Referenceを参照のこと。
- 現在の命名規則に従わない別の変異表記法
更新履歴:
- Gene Reviews著者: Sheila Unger, MD and Andrea Superti-Furga, MD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2021.12.23. 日本語訳最終更新日: 023.2.8.[in present]