常染色体顕性頭蓋骨幹端異形成症
(Craniometaphyseal Dysplasia, Autosomal Dominant)
[Synonyms:ADPKD]
Gene Reviews著者: Ernst Reichenberger, PhD and I-Ping Chen, DDS, MS, PhD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2020.6.11. 日本語訳最終更新日: 2023.2.1.
原文: Craniometaphyseal Dysplasia, Autosomal Dominant
要約
疾患の特徴
常染色体顕性頭蓋骨幹端異形成症(本稿ではAD-CMDと表記する)は、頭蓋骨の進行性、びまn性の骨増殖症を特徴とする疾患で、臨床的には幅広の鼻梁、鼻周囲の突出、左右頰骨弓間距離の拡大を伴う眼間開離、下顎の突出といった形で現れる。歯槽骨の骨増殖と骨硬化により、歯列の発達が遅延したり、歯の萌出不全をきたしたりすることがある。頭蓋顔面骨の進行性の肥厚は、生涯にわたって継続的に進行し、しばしば大後頭孔を含む頭蓋部の孔全般の狭小化を招く結果となる。未治療のまま経過すると、脳神経の圧迫により、顔面神経麻痺、失明、聾(伝音性ないし感音性難聴)といった障害に至る場合がある。合併症を伴わない一般的なAD-CMD罹患者の寿命は正常である。ただ、重度のAD-CMD罹患者については、大後頭孔の圧迫により寿命が短くなる可能性が考えられる。
診断・検査
診断は、頭蓋底・頭蓋冠・顔面骨・下顎骨のびまん性骨増殖症、長管骨骨幹端の幅の拡大やX線透過性といった臨床所見、X線所見を基に行われる。臨床像だけで診断の確定にまで至らない例については、分子遺伝学的検査でANKHの病的バリアントのヘテロ接合を同定することで診断の確認を行うことが可能である。
臨床的マネジメント
症候に対する治療:
頭蓋顔面チームによる摂食や呼吸の問題に関する治療、ならびに、脳神経の圧迫や、大後頭孔レベルでの脳幹/脊髄の圧迫を軽減するための外科的介入を行う。顔面骨の重度の過成長に対しては、形態修正術が行われることがある。ただ、手術は手技的に難しく、骨が再度、成長してしまうことが多い。補聴器の使用、視神経埋入に対する視覚補助具の使用や外科的治療、言語治療、咬合異常に対する外科的介入なども考えられる。
定期的追跡評価:
摂食や呼吸の問題に関する評価を少なくとも年に1度行う。大後頭孔を含む頭蓋の孔の狭小化に伴う徴候や症候を調べるための評価を、少なくとも年に1度行う。聴覚に関する評価、ならびに眼科的評価を、少なくとも年に1度行う。
遺伝カウンセリング
名が示す通り、AD-CMDは常染色体顕性の遺伝形式をとる。AD-CMDと診断された罹患者の大多数は親からの継承例で、de novoの病的バリアントに起因してAD-CMDに至った例の割合は非常に低いと考えられている。AD-CMD罹患者の子が病的バリアントを継承する可能性は50%である。家系内に存在するAD-CMDの原因となった病的バリアントが同定済の場合は、高リスクの妊娠に備えた出生前検査や着床前遺伝学的検査を行うことが可能である。
診断
今のところ、AD-CMDに関する公式の診断基準は確立していない。
本疾患を示唆する所見
以下のような臨床所見、X線写真所見、検査所見を有する例については、AD-CMDを疑う必要がある。
臨床所見
- 鼻腔の閉塞
- 特徴的顔貌
幅広の鼻梁,鼻周囲の突出,左右頰骨弓間距離の拡大を伴う眼間開離,下顎の突出(図1参照)
- 前頭-後頭部の骨増殖症に起因する長頭
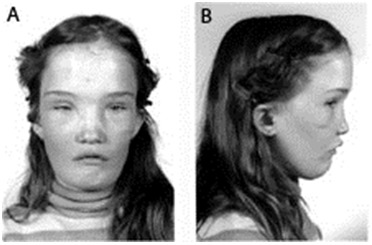
図1:13歳女性AD-CMD罹患者の顔面症候
Elsevier社の許諾を得て、Reichenbergerら[2001]より転載。
X線写真所見
- 頭蓋底
- 頭蓋底の瀰漫性の骨増殖症が進行することで大後頭孔の狭小化が生じることがある。
- 頭蓋
- 長骨
- 肋骨ならびに鎖骨
乳児期の段階で骨硬化が始まるような例もみられる(図2参照)。
疾患の進行に伴い、頭蓋冠、顔面骨、下顎骨のびまん性骨増殖症が悪化し[Lamazzaら2009]、頭蓋の孔が閉塞に至る。
骨幹端の皮質の菲薄化と骨密度の低下を伴う骨幹端の幅の拡大(三角フラスコ状あるいは棍棒状と表現される)が、生後早期に見つかることがある。ただ、骨幹端の変化は、通常は幼児期に始まる。末広がりの形状が最も顕著に現れるのは、大腿骨遠位部と脛骨である(図3)。乳児に骨幹の骨硬化/骨増殖がみられることがあるが、これは年齢とともに消失する。小児や成人においては、骨幹の骨密度は正常であるが、皮質の厚みの拡大がみられる場合もある。
小児期初期には肋骨や鎖骨(内側部[すなわち、置換骨の部分])に硬化がみられることがあるものの、5歳までに正常な骨密度になる[Richardsら1996]。
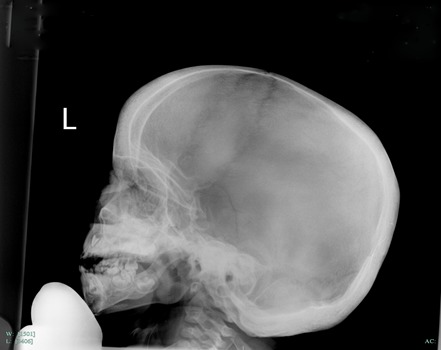
図2:3歳のAD-CMD罹患児にみられた頭蓋顔面骨の厚みの拡大
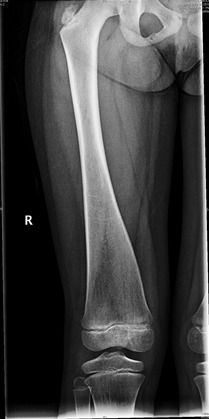
図3:特に膝関節で顕著にみられる長管骨骨幹端の幅の拡大
検査所見
- 血中カルシウム・リン濃度
- 血清アルカリホスファターゼ活性
- 副甲状腺ホルモンレベル
- オステオカルシン
血中カルシウム・リン濃度は正常範囲[Cheungら1997]、もしくは低下[Sheppardら2003]を示す。
血清アルカリホスファターゼ活性の上昇がみられる場合がある[Sheppardら2003,Wuら2016]。
副甲状腺ホルモンレベルは正常、もしくは軽度上昇ないし一過性の上昇をみることがある[Fanconiら1988,Cheungら1997,Sheppardら2003,Wuら2016]。
オステオカルシンは低下する[Yamamotoら1993]。
注:限られた数のデータに基づく所見であることに注意が必要。ここで述べたパラメーターについても、ばらつきが存在するものと考えられる。パラメーターでみられる異常値は、一過性のものであることも考えられる。
診断の確定
発端者におけるAD-CMDの診断は、特徴的な頭蓋顔面の骨増殖症に加えて、長管骨の末広がり形状や骨梁形成不全がみられること、ないし、分子遺伝学的検査にてANKHの病的バリアントのヘテロ接合が確認されることをもって確定する(表1参照)。
注:ANKHに意義不明のバリアントのヘテロ接合が検出された場合、それは本疾患の診断を確定するものでも否定するものでもない。
分子遺伝学的検査のアプローチとしては、表現型に合わせて、遺伝子標的型検査(単一遺伝子検査、マルチ遺伝子パネル)と網羅的ゲノム検査(エクソームシーケンシング,エクソームアレイ,ゲノムシーケンシング)を組み合わせるやり方が考えられる。
遺伝子標的型検査の場合、臨床医の側で関与が疑われる遺伝子の目星をつけておく必要があるが、ゲノム検査の場合、その必要はない。AD-CMDの表現型の幅は広く、「本疾患を示唆する所見」に記載した特徴的所見を有する例については遺伝子標的型検査(「方法1」参照)で診断がつくものと思われるが、表現型だけではその他数多く存在する骨増殖疾患と判別できないような例については、ゲノム検査(「方法2」参照)で診断がなされることになろう。
方法1
表現型や検査所見からAD-CMDの診断が示唆される場合であれば、考えられる分子遺伝学的検査のアプローチは、単一遺伝子検査、もしくはマルチ遺伝子パネルの使用ということになろう 。
- 単一遺伝子検査
最初に、遺伝子内の小欠失/挿入、ミスセンス・ナンセンス・スプライス部位バリアントといったものを検出するためのANKHの配列解析を行う。
注:使用する配列解析の手法によっては、1エクソン、複数エクソン、遺伝子全体といったサイズの欠失/重複が検出されないことがある。そのため、配列解析でバリアントが検出されなかった場合は、次のステップとして、エクソン単位や遺伝子全体の欠失/重複を検出するための遺伝子標的型欠失/重複解析を行うようにする。
注:現在のところ、本疾患の原因としてそのようなバリアントが特定された例はない。
- マルチ遺伝子パネル
現況の表現型と直接関係のない遺伝子の意義不明バリアントや病的バリアントの検出を抑えつつ、最も安価でかつ疾患の遺伝的原因を特定することに最もつながりやすいと思われるのは、ANKHならびにその他の関連遺伝子(「鑑別診断」の項を参照)を含むマルチ遺伝子パネルである。
注:(1)パネルに含められる遺伝子の内容、ならびに個々の遺伝子について行う検査の診断上の感度については、検査機関によってばらつきがみられ、また、経時的に変更されていく可能性がある。
(2)マルチ遺伝子パネルによっては、今このGeneReviewで取り上げている状況と無関係な遺伝子が含まれることがある。
(3)検査機関によっては、パネルの内容が、その機関の定めた定型のパネルであったり、表現型ごとに定めたものの中で臨床医の指定した遺伝子を含む定型のエクソーム解析であったりすることがある。
(4)ある1つのパネルに対して適用される手法には、配列解析、欠失/重複解析、ないしその他の非配列ベースの検査などがある。
マルチ遺伝子パネル検査の基礎的情報についてはここをクリック。遺伝学的検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
方法2
表現型からだけでは、その他数多く存在する骨増殖症を伴う遺伝性疾患と区別がつきにくいような場合は、網羅的ゲノム検査(この場合、臨床医の側で疑わしい遺伝子の目星をつけておく必要はない)が、診断に至る可能性の最も高い選択肢となる。エクソームシーケンシングが広く用いられているが、ゲノムシーケンシングを使用することも可能である。エクソームシーケンシングで診断がつかないような場合、とりわけ常染色体顕性遺伝を示唆するデータがある場合は、配列解析では検出できないエクソン単位の欠失/重複を調べるためのエクソームアレイ(利用可能であればの話)も検討対象になりうる。
注:現在のところ、本疾患の原因としてそのようなバリアントが特定された例はない。
網羅的ゲノム検査の基礎的情報についてはここをクリック。ゲノム検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
表1:常染色体顕性頭蓋骨幹端異形成症で用いられる分子遺伝学的検査
| 遺伝子1 | 方法 | その手法で病的バリアント2が検出される発端者の割合 |
|---|---|---|
| ANKH | 配列解析3 | 90%近く4 |
| 遺伝子標的型欠失/重複解析5 | 報告例なし6。 | |
| 不明7 | 検査法なし。 | 10%近く。 |
- 染色体上の座位ならびにタンパク質に関しては、表A「遺伝子とデータベース」を参照。
- この遺伝子で検出されているアレルバリアントの情報については、「分子遺伝学」の項を参照のこと。
- 配列解析を行うことで、良性、おそらく良性、意義不明、おそらく病的、病的といったバリアントが検出される。バリアントの種類としては、遺伝子内の小さな欠失/挿入、ミスセンス・ナンセンス・スプライス部位バリアントなどがあるが、通常、エクソン単位あるいは遺伝子全体の欠失/重複については検出されない。配列解析の結果の解釈に際して留意すべき事項についてはこちらをクリック。
- Nürnbergら[2001],Reichenbergerら[2001]
- 遺伝子標的型欠失/重複解析では、遺伝子内の欠失や重複が検出される。具体的手法としては、定量的PCR、ロングレンジPCR、MLPA法、あるいは単一エクソンの欠失/重複の検出を目的に設計された遺伝子標的型マイクロアレイなどがある。
- AD-CMDは、機能獲得型/ドミナントネガティブ作用によって引き起こされること、ならびに、これまでに遺伝子内の大きな欠失/重複が報告されていないことから考えて、遺伝子標的型欠失/重複解析によって疾患原因となったバリアントが検出される可能性は低いように思われる。
- 頭蓋骨幹端異形成症孤発例の中には、ANKH内に病的バリアントが検出されない例もみられる。このことから、座位異質性の存在が示唆される。
臨床的特徴
臨床像
AD-CMDは、後鼻孔狭窄(鼻腔の狭小化)に起因する呼吸や摂食の問題がもととなって、生後数週のうちに発見されることがしばしばある[Haverkampら1996,Cheungら1997,Taggartら2014]。
初期段階のAD-CMDは、X線写真でみられる頭蓋底の硬化という形で把握される。頭蓋底、頭蓋冠、顔面骨、下顎骨で徐々に骨増殖症が進行していく。下顎の過成長(下顎の骨増殖症)、ならびに中顔面の劣成長(中顔面の後退)がしばしばみられる[Hayashibaraら2000]
頭蓋顔面の骨の肥厚は、生涯にわたって続き、しばしば大後頭孔を含む頭蓋の孔の狭窄を引き起こすことになる。未治療で経過すると、頭蓋の骨増殖症や骨硬化が進行するにつれ、脳神経の圧迫により顔面神経麻痺、失明、聾(伝音性ないし感音性難聴)などの障害をきたすことがある[Beightonら1979,Richardsら1996]。鼻閉や下顎骨の骨増殖症は、スピーチの調音に影響を及ぼすことになる。
ChiariⅠ型奇形の併発により、重度の頭痛を招く場合がある[Tanakaら2013]。
歯槽骨の骨増殖や骨硬化の結果、歯列の発達に遅れが生じ、歯が萌出できないようなこともある[Chenら2014]。
顎骨の過成長により、咬合異常や前歯部反対咬合が生じる場合がある[Hayashibaraら2000]。
寿命
合併症を有しない典型的AD-CMD罹患者の寿命は正常である。頭蓋骨幹端異形成症(訳注:「AD-CMD」ではなく「CMD」)の孤発例(すなわち、家系内で1人だけの発生例)については、表現度に大きな幅がみられる。
遺伝型-表現型相関
これまでに遺伝型-表現型相関として報告されたものはない。
AD-CMDの表現型の重症度(表現度)は、同一家系内の罹患者間にあっても幅がみられる。
浸透率
浸透率は100%である。罹患者の男女比は1:1である。
命名法について
AD-CMDは以前、「頭蓋骨幹端異形成症-Jackson型」と呼ばれていた。
発生頻度
頭蓋骨幹端異形成症は非常に稀で、疫学に関するデータは得られていない。
遺伝学的に関連のある疾患(同一アレル疾患)
表2:ANKHの同一アレル疾患
| 疾患名 | 遺伝形式 | コメント |
|---|---|---|
| 軟骨石灰症2 (OMIM 118600) |
AD | AD-CMDと軟骨石灰症の共分離を示す1家系が報告されている1。 |
| 知的障害-聾-強直症候群 | AR | 両アレルに病的バリアントを有する例で、難聴、知的障害、脊椎強直、小関節周囲の石灰化(ヘテロ接合性病的バリアントの例では軽度の関節症)がみられる1家系が報告されている2。 |
AD=常染色体顕性;AR=常染色体潜性
- Baynamら[2009]
- Moravaら[2011]
鑑別診断
表3:常染色体顕性頭蓋骨幹端異形成症との鑑別診断に関係してくる遺伝子
| 遺伝子 | 疾患名 | 遺伝形式 | 臨床的特徴 | 鑑別の鍵となる症候 |
|---|---|---|---|---|
| AMER1 | 頭蓋骨硬化を伴う骨線条症 | XL | 長管骨の縦の硬化性線条と頭蓋顔面骨の骨硬化との組合せ。 | 低身長,大泉門閉鎖遅延,小下顎症,女性でみられる長骨の線条。 |
| FLNA | 前頭骨幹端異形成症1型 (「耳口蓋指スペクトラム障害」のGeneReviewを参照) |
XL | 骨格所見は、前頭骨の骨増殖症と骨幹端異形成(Pyle病類似のもの)。 | 尿性器奇形,手・肘・膝・足首の拘縮。 |
| GJA1 | 常染色体潜性頭蓋骨幹端異形成症(AR-CMD) (OMIM 218400) |
AR | AD-CMD類似の頭蓋底・頭蓋冠の骨増殖症と末広がりの骨幹端。 | 典型的なAD-CMDより骨格症候は軽度。 |
| LRP5 | 常染色体顕性大理石骨病1型(OMIM 607634) | AD | 脆弱性の亢進を伴わない頭蓋骨の骨硬化と骨量上昇。 | びまん性骨硬化症。 末広がりの骨幹端はみられない。 |
| SFRP4 | Pyle病(OMIM 265900) | AR | 骨幹端異形成。 | Pyle病では頭蓋骨にはほとんどあるいは全く症状が現れない。 |
| SOST | 頭蓋骨幹異形成症(CDD) (OMIM 218300) |
AD | ・神経絞扼を伴う頭蓋顔面骨の進行性過成長により、聾、顔面神経麻痺、視覚障害が生じる。 ・臨床的に重要な合併症として後鼻孔狭窄がある。 ・X線写真にて、頭蓋顔面骨の骨増殖症がみられる一方で、四肢の骨の骨幹は拡大し、皮質は菲薄化する。 |
頭蓋顔面骨の肥厚は、一般に、頭蓋骨幹端異形成症よりCDDのほうがより重度。 |
| 硬化性骨症 (「SOST関連硬化性骨異形成症」のGeneReviewを参照) |
AR | ・進行性の骨格過成長(頭蓋骨と下顎骨で最も顕著)、ならびにさまざまな程度の合指趾。 ・前額部の突出と下顎の過成長に起因する顔の変形が小児期にみられるようになり、成人期にかけて進行していく。 ・頭蓋骨の骨増殖症により孔の狭小化や第Ⅶ脳神経の絞扼(顔面神経麻痺に至る)が生じ、これより低頻度ながら、その他の神経絞扼症候群もみられる。 ・頭蓋冠の骨増殖症により頭蓋内容積が減少し、頭蓋内圧の亢進により死亡に至るリスクが高まる。 ・高齢になるまで生存することは稀であるが、例がないわけではない。 |
脊椎や骨盤の骨硬化症,第2-3指の合指,爪形成不全がみられるが、末広がりの骨幹端はみられない。 巨人症。 |
|
| Van Buchem病 (「SOST関連硬化性骨異形成症」のGeneReviewを参照) |
AR | ・進行性の骨格過成長。 ・一般に、Van Buchem病のほうが硬化性骨症より軽度。 合指はみられない。 ・寿命は正常と思われる。 |
鎖骨や肋骨などの骨硬化症。 高ホスファターゼ血症 |
|
| TGFB1 | 進行性骨幹異形成症 | AD | 頭蓋骨の骨増殖症により孔の狭小化が生じ、顔面神経麻痺や聾につながる。 | 長管骨骨幹の骨増殖症が顕著にみられる。 |
AD=常染色体顕性;AR=常染色体潜性;XL=X連鎖性
骨幹端異形成症,Braun-Tinschert型(OMIM 605946)
骨幹端異形成症,Braun-Tinschert型は、常染色体顕性の遺伝形式をとる。変異を生じる原因遺伝子は不明である[Braunら2001]。
臨床的マネジメント
最初の診断に続いて行う評価
AD-CMDと診断された罹患者については、疾患の範囲やニーズを把握するため、診断に至る過程ですでに実施済でなければ、表4にまとめた評価を行うことが推奨される。
表4:常染色体顕性頭蓋骨幹端異形成症罹患者の最初の診断後に行うことが推奨される評価
| 系/懸念事項 | 評価 | コメント |
|---|---|---|
| 乳児期の呼吸と摂食の問題 | 耳鼻咽喉科的評価を含めた頭蓋顔面チームによる評価を目的とした紹介。 | 後鼻孔狭窄の評価を含むものとする。 |
| 骨格の骨増殖症 |
|
|
| 脳神経の圧迫 | 神経学的診査 | |
| 耳鼻咽喉科的評価 | 聴覚系の評価を目的として行う。 | |
| 聴覚評価 | 難聴の評価を目的として行う。 | |
| 眼科的診査 | 視力障害の評価を目的として行う。 | |
| 内分泌/代謝 |
|
骨代謝の評価を目的として行う。 |
| スピーチ | 言語治療士による評価 | 幼児期には、進行性難聴、顔面神経麻痺、骨増殖症によりスピーチの問題が引き起こされることがある。 |
| 歯の萌出遅延と咬合異常 | 歯科医師による評価 | 埋伏歯や歯の萌出遅延の発見を目的として、乳歯萌出開始以降に行う。 |
| 遺伝カウンセリング | 遺伝の専門医療職1の手で行う。 | 医学的、個人的な意思決定の用に資するべく、本人や家族に対し、AD-CMDの本質、遺伝形式、そのもつ意味についての情報提供を行う。 |
1.臨床遺伝医、認定遺伝カウンセラー、認定上級遺伝看護師をいう。
症候に対する治療
表5:常染色体顕性頭蓋骨幹端異形成症罹患者の症候に対する治療
| 症候/懸念事項 | 治療 | 考慮事項/その他 |
|---|---|---|
| 新生児,乳児における摂食と呼吸の問題 | 頭蓋顔面チームにより行う。 | |
| 脳神経の圧迫 | 外科的介入。 | 脳神経圧迫に起因する重度の症状を軽減する目的で行う。 |
| 大孔の狭窄 | 外科的介入。 | 頭痛や、Chiari奇形関連のリスクを軽減する目的で行う。 |
| 顔面骨の骨増殖症 | 顔面骨、ならびに鼻・前額・頭蓋領域の重度の骨過成長に対し、形態修正が行われる場合がある。 |
|
| 難聴 | 補聴器。 | 人工内耳が可能な場合あり。 |
| 視覚障害 |
|
進行性の視力障害を見越して、子どものうちから点字を学ぶこともありうる。 |
| スピーチの問題 | 言語治療を検討。 | |
| 咬合異常 | 重度の咬合異常に対する外科的介入。 | 矯正歯科治療の立案にあたっては、歯の萌出遅延を頭に入れておく必要あり。 |
定期的追跡評価
表6:常染色体顕性頭蓋骨幹端異形成症罹患者で推奨される定期的追跡評価
| 系/懸念事項 | 評価 | 実施頻度 |
|---|---|---|
| 新生児・乳児の摂食・呼吸の問題 | 頭蓋顔面チーム | 年に1度、あるいは必要ならより高頻度に。 |
| 大孔を含む頭蓋の孔の狭窄 | 神経学的評価 | |
| 難聴 | 聴覚評価 | |
| 視力障害 | 眼科的診査 |
リスクを有する血縁者の評価
早期治療や予防処置を行うことで利益が得られる人を可能な限り早期に特定するため、リスクを有する血縁者については、評価を行うことが望ましい。リスクを有する血縁者を早期に診断することは、進行性の骨増殖症の合併症を管理していく上で有益な場合がある。
評価の具体的内容は以下のようなものになろう。
- 家系内に存在する病的バリアントが既知の場合は分子遺伝学的検査。
- 家系内に存在する病的バリアントが未知の場合は、臨床的評価、ならびに頭蓋骨と長管骨のX線写真。
リスクを有する血族に対して行う遺伝カウンセリングを目的とした検査関連の事項については、「遺伝カウンセリング」の項を参照されたい。
研究段階の治療
さまざまな疾患・状況に対して進行中の臨床試験に関する情報については、アメリカの「Clinical Trials.gov」、ならびにヨーロッパの「EU Clinical Trials Register」を参照されたい。
注:現時点で本疾患に関する臨床試験が行われているとは限らない。
その他
カルシトニンは、骨代謝を抑制することから、有効であろうと考えられてきた。ただ、これまでの報告を見る限り、頭蓋骨幹端異形成症罹患者の頭蓋顔面骨の骨増殖症を治療する上で、カルシトニン治療は有効ではないとの結果が出ている[Fanconiら1988,Haverkampら1996]。
カルシトリオールと低カルシウム食により、破骨細胞の形成を促進して骨吸収を促すやり方は、かつて顔面神経麻痺の改善に有効とされてきたが、現在、骨幹端の変形には無効とされている[Keyら1988,Wuら2016]。
骨塩密度の上昇を伴う疾患の治療にアセタゾラミドを使用することが考えられている。
González-Rodríguezら[2016]は、骨幹端異形成症類似の表現型を示す例にアセタゾラミドを使用した例を報告しているが、この例がAD-CMDであるとの確認まではなされていない。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
名が示す通り、AD-CMDは常染色体顕性の遺伝形式をとる。
家族構成員のリスク
発端者の両親
- AD-CMD罹患者の大多数は、片親からの継承例である。
- AD-CMD罹患者の中には、de novoの病的バリアントに起因して本疾患に至った例もみられる。de novoの病的バリアントに起因してAD-CMDに至った例の占める割合は、非常に低いものと考えられているものの、統計的データは存在しない。
- 発端者の有するANKHの病的バリアントが既知で、なおかつ、見かけ上、発端者が家系内で唯一の罹患者(すなわち孤発例)であると思われる場合は、発端者の両親に対して分子遺伝学的検査を行うことが推奨される
- 発端者で同定された病的バリアントが、両親いずれの白血球DNAからも検出されないということであれば、考えられることは、発端者に生じたde novoの病的バリアント、もしくは、片親の生殖細胞系列モザイクのいずれかということになる*。理論的にはありうることながら、これまで実際に生殖細胞系列モザイクの片親から病的バリアントを継承した例は報告されていない。
- AD-CMD罹患者の家族歴については、血縁者が本疾患を有していることを見逃してしまったために、まるで陰性であるかのようにみえる場合がある。そのため、見かけ上、家族歴が陰性であっても、発端者の両親に対して適切な臨床的評価ないし分子遺伝学的検査(両親とも、発端者で同定された病的バリアントのヘテロ接合者ではないということを確かめる検査)を行わない限り、その確定はできない。
*見かけ上、de novoの病的バリアントと目される場合は、もう1つの可能性として、両親が実際の生物学的父・母ではなかったという可能性も調べていく必要がある。
発端者の同胞
発端者の同胞の有するリスクは、発端者の両親の臨床的/遺伝的状態によって変わってくる。
- 発端者の片親が罹患者である、ないし、発端者で同定されている病的バリアントを片親も有しているということがわかっている場合は、同胞の有するリスクは50%である。AD-CMDの浸透率は100%であるため、病的バリアントを継承した同胞にはAD-CMDの表現型が現れる。ただ、その際の表現型の重症度は一様ではない。
- 発端者の有するANKHの病的バリアントが既知で、それが両親いずれの白血球DNAからも検出されない場合は、同胞への再現リスクは1%と推定される。それは、理論上、親の生殖細胞系列モザイクの可能性が考えられるからである[Rahbariら2016]。
- 両親の遺伝的状態は不明ながら、臨床的には両親とも非罹患者と目される場合は、発端者の同胞の有するリスクは低いながら、一般集団よりは高くなるものと思われる。それは、理論上、親の生殖細胞系列モザイクの可能性が残っているからである。
発端者の子
AD-CMD罹患者の子が、原因となった病的バリアントを継承する可能性は50%である。
他の家族構成員
他の血縁者の有するリスクは、発端者の両親の状態によって変わってくる。仮に片親が罹患者であったとすると、その血族にあたる人はすべてリスクを有することになる。
関連する遺伝カウンセリング上の諸事項
早期診断・早期治療を目的としてリスクを有する血縁者に対して行う評価関連の情報については、「臨床的マネジメント」の「リスクを有する血縁者の評価」の項を参照されたい。
家族計画
- 遺伝的リスクの確定、出生前/着床前遺伝子検査を受けるかどうかの話し合いとに最も適しているのは、妊娠前の時期である。
- 罹患者である若い成人に対しては、遺伝カウンセリング(子に生じる可能性のあるリスクや、子を儲ける上での選択肢についての説明を含む)を提供することが望ましい。
出生前検査ならびに着床前遺伝学的検査
家系内に存在するAD-CMDを引き起こす病的バリアントが判明している場合には、高リスクの妊娠に備えた出生前検査や、着床前遺伝学的検査を行うことが可能である。
出生前検査の利用に関しては、医療者間でも、また家族内でも、さまざまな見方がある。
現在、多くの医療機関では、出生前検査を個人の決断に委ねられるべきものと考えているようであるが、こうした問題に関しては、もう少し議論を深める必要があろう。
関連情報
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- American Society for Deaf Children
Phone: 800-942-2732 (ASDC)
Email: info@deafchildren.org
www.deafchildren.org
- Children's Craniofacial Association
Phone: 800-535-3643
Email: contactCCA@ccakids.com
www.ccakids.org
- Face Equality International
United Kingdom
Email: info@faceequalityinternational.org
www.faceequalityinternational.org
- National Association of the Deaf
Phone: 301-587-1788 (Purple/ZVRS); 301-328-1443 (Sorenson); 301-338-6380 (Convo)
Fax: 301-587-1791
Email: nad.info@nad.org
www.nad.org
- UCLA International Skeletal Dysplasia Registry (ISDR)
Phone: 310-825-8998
International Skeletal Dysplasia Registry
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A:常染色体顕性頭蓋骨幹端異形成症:遺伝子とデータベース
| 遺伝子 | 染色体上の座位 | タンパク質 | Locus-Specificデータベース | HGMD | ClinVar |
|---|---|---|---|---|---|
| ANKH | 5p15.2 | 進行性強直症タンパク質ホモログ | ANKH @ LOVD | ANKH | ANKH |
データは、以下の標準資料から作成したものである。遺伝子についてはHGNCから、染色体上の座位についてはOMIMから、タンパク質についてはUniProtから。リンクが張られているデータベース(Locus-Specific,HGMD,ClinVar)の説明についてはこちらをクリック。
表B:常染色体顕性頭蓋骨幹端異形成症関連のOMIMエントリー(閲覧はすべてOMIMへ)
| 123000 | CRANIOMETAPHYSEAL DYSPLASIA, AUTOSOMAL DOMINANT; CMDD |
| 605145 | ANKH INORGANIC PYROPHOSPHATE TRANSPORT REGULATOR; ANKH |
分子レベルの病原性
ANKHは、進行性強直症タンパク質ホモログをコードしている。このタンパク質は、細胞の外膜に位置して、細胞内ピロリン酸を細胞外マトリックスへと輸送するマルチスパンの膜貫通タンパク質である。ピロリン酸は、マトリックス(骨)石灰化の調節因子である。進行性強直症タンパク質ホモログの配列は、脊椎動物間で高度に保存されている。
進行性強直症タンパク質ホモログの頭蓋骨幹端異形成症関連バリアントは、おそらく、骨芽細胞から骨基質への細胞内ピロリン酸の輸送能が低下しているものと考えられる[Hoら2000]。
疾患の発症メカニズム
最も多くみられる病的バリアントは1アミノ酸の欠失である。その他には、ミスセンスバリアント、小さなインフレームの欠失/挿入といったものがある[Nürnbergら2001,Reichenbergerら2001,Kornakら2010,Zajacら2010,Dutraら2012]。大多数の病的バリアントは、膜貫通ループ構造の細胞内ドメインと目される領域をコードする塩基に生じている。ノックアウトマウスやノックインマウスの研究から、ANKHの病的バリアントは、ピロリン酸輸送機能の喪失と並んで、ドミナントネガティブな機能獲得を生じると考えられている。こうした形でマウスモデルで共通した表現型が現れる理由は、病的ANKタンパク質の迅速な分解が生じているということで説明されよう[Kanaujiyaら2018]。疾患発症のメカニズムについては、現在のところ、これ以外の情報は得られていない。
更新履歴:
-
Gene Reviews著者: Ernst Reichenberger, PhD and I-Ping Chen, DDS, MS, PhD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2020.6.11. 日本語訳最終更新日: 2023.2.1.[in present]