胸腺Thymusとは
胸腺は胸骨裏面の前縦隔に位置する免疫担当臓器で、Tリンパ球が成熟する場所である。胸腺においてリンパ球が最も多く含まれる時期は思春期であり、重量にして30-40gに達するが、その後は加齢とともに退縮し脂肪組織に置き換わってゆく。胸腺は、上皮細胞、成熟過程のリンパ球である胸腺細胞、マクロファージと樹状細胞などから構成され、皮質と髄質に分かれている。骨髄から胸腺に移入した未熟なT細胞は、上記の胸腺間質細胞の働きにより、自己のMHCと適度な親和性のあるT細胞を選択し(正の選択)、自己抗原に反応するT細胞を消去し(負の選択)、体に有益なT細胞のみが末梢血液中に放出される。すなわち、胸腺は細胞性免疫機能の維持と自己免疫疾患発症の抑制に関与している重要な臓器といえる。胸腺上皮細胞から発生する腫瘍としては、胸腺腫、胸腺がん、カルチノイド、胚細胞性腫瘍、胸腺嚢胞などがあり、非上皮性腫瘍としては悪性リンパ腫などがある。
胸腺腫Thymomaについて
胸腺腫は胸腺上皮細胞から発生する腫瘍で、増大速度は緩徐なことが多く、リンパ節転移や血行性遠隔転移はまれである。腫瘍内には正常胸腺に見られる未熟なTリンパ球である胸腺細胞が豊富に含まれていることが多い。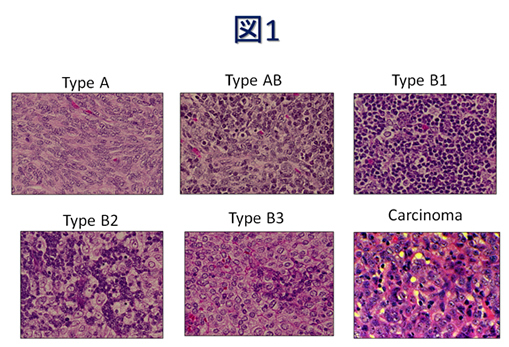
World Health Organization 分類 (図1)
| Type A | 紡錘形ないし卵円形腫瘍細胞から構成され、リンパ球は少ない。胸腺腫の中では、最も悪性度が低い。 |
| Type AB | リンパ球が少なく紡錘形ないし卵円形腫瘍細胞のtype A領域と、リンパ球に富み小型の多角形ないし卵円形腫瘍細胞のtype B領域が二相性に混在する。 |
| Type B1 | 正常胸腺皮質のように未熟なリンパ球が密に存在し、腫瘍上皮細胞はまばらである。髄質様構造をとる部分もある。 |
| Type B2 | やや大型の多角形腫瘍細胞とtype B1よりやや少ないが多くの未熟なリンパ球から構成される。 |
| Type B3 | わずかな異型性を伴う中型の円形なし多角形腫瘍細胞と、少なめの未熟リンパ球から構成される。胸腺腫の中では最も悪性度が高く、播種や隣接臓器浸潤を伴うこともある。 |
正岡病期
| I期 | 腫瘍は被膜に包まれている |
| II期 | 周囲の胸腺・脂肪組織・縦隔胸膜への肉眼的浸潤,または病理学的被膜浸潤あり |
| III期 | 心膜・肺・大血管への浸潤あり |
| IV期 | IVa: 心膜播種または胸膜播種あり,IVb: リンパ行性または血行性転移あり |
UICC-TNM病期第9版
| T―原発巣 | |
| TX | 原発巣不明 |
| T0 | 原発巣消失 |
| T1 | 胸腺内に限局あるいは,縦隔脂肪,胸膜被膜に浸潤しているが,その他の縦隔構造への直接浸潤はない(Level1) |
| T1a | 最大径5cm以下 |
| T1b | 最大径5cmより大きい |
| T2 | 隣接臓器浸潤:心膜,肺,横隔神経(Level2) |
| T3 | 隣接臓器浸潤:腕頭静脈,上大静脈,胸壁,心膜外の肺門部血管(Level3) |
| T4 | 隣接臓器浸潤:大動脈(上行,弓部,下行),大動脈弓の分枝血管,心膜内の肺血管,心筋,気管,食道 |
| N―所属リンパ節 | |
| NX | 所属リンパ節の検索できず |
| N0 | リンパ節転移なし |
| N1 | 前縦隔リンパ節転移 |
| N2 | 深部胸腔または頸部リンパ節転移 |
| M―遠隔転移 | |
| MX | 胸膜・心膜播種,遠隔転移の検索できず |
| M0 | 胸膜・心膜播種,および遠隔転移なし |
| M1a | 胸膜あるいは心膜播種 |
| M1b | 肺内転移あるいは遠隔転移 |
| Ⅰ期 | T1 | N0 | M0 |
| Ⅱ期 | T2 | N0 | M0 |
| Ⅲ期a | T3 | N0 | M0 |
| b | T4 | N0 | M0 |
| Ⅳ期a | T any | N1 | M0 |
| T any | N0,1 | M1a | |
| b | T any | N2 | M0,1a |
| T any | N any | M1b |
現在はTNM分類が国際標準であるが、国内データとの整合性の観点から正岡分類と併記する。
診断
- ①
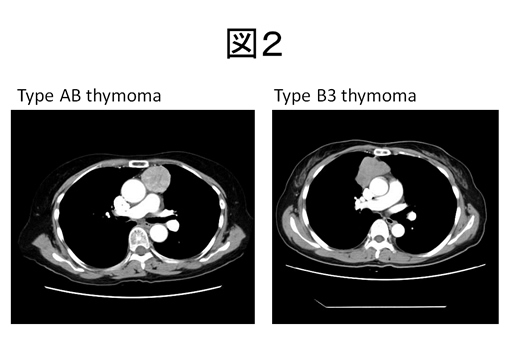
- 胸部CT検査:前縦隔の比較的辺縁明瞭な腫瘤で、内部は比較的均一で造影効果を認める。Type A、 AB、 B1では円形ないし卵円形の形状を呈し境界は明瞭であるが、Type B2、B3では扁平で分葉を認め、境界不明瞭で凹凸不正や周囲臓器への浸潤を疑う所見を認めることもあり、時には石灰化を認める。
- ②
- PET-CT検査:SUVmax 軽度~中等度の集積を認めることが多い。
- ③
- 重症筋無力症を合併するか、抗アセチルコリン受容体抗体陽性患者で縦隔腫瘍を認めた場合は確率的に胸腺腫を強く疑う。
- ④
- 組織学的確定診断にはCTまたは超音波ガイド下経皮針生検を要するが、浸潤性胸腺腫で術前治療が必要な症例や手術に高いリスクを伴う症例を除き、一期的完全切除が可能な場合はいずれにしても手術適応となるため必ずしも経皮生検は必要ない。
治療
- ①
- 外科的切除が第一選択であり、I-II期では完全切除により完治する可能性が高い。低悪性度腫瘍のため、播種病巣も可及的切除の適応となることがある。手術アプローチとしては、I-II期では低侵襲手術(ロボット支援手術を含む)が安全有用で普及してきている。
- ②
- 放射線感受性が高く、切除不能な症例では放射線照射も選択肢となる。
- ③
- 化学療法については、プラチナ製剤を含む多剤併用が用いられる。代表的なレジメンとしてADOC療法(シスプラチン,ドキソルビシン,ビンクリスチン,シクロフォスファミド)やPAC(シスプラチン,ドキソルビシン,シクロフォスファミド)などがある。切除不能浸潤性胸腺腫には完全切除を目的とした術前化学療法が行われることもある。
- ④
- 未熟なT細胞を多く含むType B1およびB2胸腺腫はステロイド感受性が高く、大量メチルプレドニゾロンによるパルス治療やCAMP療法(シスプラチン,ドキソルビシン,メチルプレドニゾロン)が選択肢となりうる。カルボプラチン+パクリタキセル療法が選択される場合があるが、過去に重篤な筋炎関事象が報告されており慎重な選択が求められる。
- ⑤
- 胸腺腫に対する免疫チェックポイント阻害薬は、自己免疫関連有害事象の発生頻度が高く(50–70%程度との報告がある)、重篤な筋炎や心筋炎を惹起することがある。がんゲノムプロファイル検査などにより、免疫チェックポイント阻害剤が推奨された場合などでも、その適応は極めて慎重に判断すべきである。
予後
日本の胸腺腫データベース解析では、胸腺腫・胸腺癌・胸腺カルチノイドを含め、他病死を除いた疾患特異的10年生存率は正岡I期99.4%、II期98.0%、III期82.9%、IVa期71.8%、IVb期54.0%と報告されている。胸腺腫に合併する自己免疫疾患
- ①
- 重症筋無力症は胸腺腫患者の20-30%に合併し、胸腺腫に伴う重症筋無力症では抗アセチルコリン受容体抗体は陽性である。重症筋無力症の症状がなくとも、抗アセチルコリン受容体抗体が陽性である胸腺腫患者も少なくなく、潜在的な重症筋無力症の可能性がある。胸腺腫の切除に際しては,抗アセチルコリン受容体抗体値を測定し、その陽性例では重症筋無力症に準じた拡大胸腺摘出術を行うことが望ましいとされている。
- ②
- 赤芽球癆は胸腺腫患者の3-5%に合併し、赤芽球癆患者の20-50%に胸腺腫が合併する。胸腺腫の摘出による赤芽球癆の改善効果は乏しく、シクロスポリンやステロイドによる全身治療が効果的である。
- ③
- 低γグロブリン血症の合併は比較的まれであり、胸腺腫に合併し免疫不全をきたす病態をGood症候群という。胸腺腫の摘出による低γグロブリン血症の改善はあまり期待できない。
- ④
- その他、血小板減少症、白血球減少症,シェーグレン症候群、全身性エリテマトーデス(SLE)、甲状腺機能異常、円形脱毛症、皮膚筋炎、自己免疫性肝炎、自己免疫性脳炎、GVHD様皮膚炎など様々な自己免疫病態を呈する。
胸腺がんについて
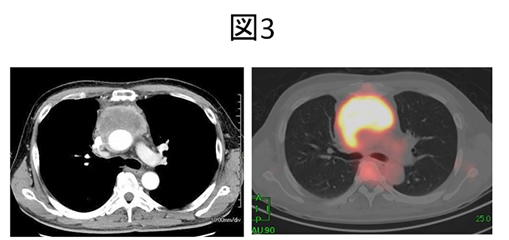
胸腺がんは比較的稀な縦隔腫瘍で、胸腺腫と同様に悪性胸腺上皮性腫瘍であるが、胸腺腫に比し腫瘍細胞の異型性が強く、腫瘍内には未熟なT細胞を認めない。重症筋無力症などの自己免疫疾患も合併も見られない。発見時には局所進行癌であることが多く、リンパ節転移や血行性転移も珍しくない。胸腺腫に比し胸部圧迫症状が早期に出現する。CTでは周囲臓器への浸潤を認めることが多く、PET検査ではFDGの高集積が特徴的である(図3)。化学療法・放射線治療・外科的切除を組み合わせた集学的治療が行われる。完全切除例では長期生存が期待でき、耐術能がある症例では隣接臓器合併切除を含む拡大手術が適応される。胸腺腫と異なり亜全摘術や播種切除の治療的意義は不明である。切除不能例では、局所進行であれば根治目的で放射線治療を基軸として、抗悪性腫瘍薬を併用する。また、転移性ないしは根治治療不能と判断された場合、薬物療法は、保険承認されている治療として、従来から用いられてきたカルボプラチン+パクリタキセル併用療法に免疫チェックポイント阻害薬であるアテゾリズマブの追加が有効であることが示され、分子標的治療薬としては、マルチキナーゼ阻害薬であるレンバチニブが用いられる。肺癌学会診療ガイドライン(第3部.胸腺腫瘍診療ガイドライン)には保険承認されていない治療薬について記載されているが、各医療機関の判断により治療をされている実態がある。また、胸腺カルチノイドについては、2004年のWHO分類においては胸腺癌の一亜型となっている神経内分泌腫瘍であり*、時に多発性内分泌腫瘍症I型に合併することがある。ソマトスタチン受容体シンチグラフィでソマトスタチン受容体陽性と診断された場合、放射性医薬品であるルテチウムオキソドトレオチドが保険適用となっている。
なお、胸腺上皮性腫瘍は「希少がん」に分類され、「標準的な治療法が確立されていない」。治療への到達が低いものの(10%以下と公表)、「D006-19 がんゲノムプロファイリング検査 (2) 標準治療がない固形がん」に該当するため、がんゲノムプロファイリング検査(がん遺伝子パネル検査)を未治療例でも実施することができる。頻度は少ないが、分子標的治療薬や免疫チェックポイント阻害剤が推奨される遺伝子異常が検出される可能性がある。
*2015年のWHO分類(第4版)では、Thymic neroendocrine tumorsに分類
重症筋無力症と胸腺摘出術
重症筋無力症は神経筋接合部のニコチン作動性アセチルコリン受容体に対する自己抗体により発症する自己免疫疾患である。2006年の全国調査で人口10万人あたり11.8人の有病率とされ、やや女性に多い。症状
眼瞼下垂、複視などの眼症状、四肢筋力の低下、嚥下・構音障害,重症例では呼吸不全となり生命を脅かすことがある。症状には日内変動があり,夕方に悪化する傾向がある。診断
抗アセチルコリン受容体抗体価の上昇、エドロホニウム(アンチレックス)試験、誘発筋電図によるWaning現象)などにより確定診断が得られる。重症筋無力症の確定診断には胸部CT検査により胸腺腫や胸腺過形成の有無を調べる必要がある。Myasthenia Gravis Foundation of America(MGFA)重症度分類
| I | 眼筋型、眼輪筋の筋力低下、四肢筋力に低下なし |
| II | 眼以外の筋力が軽度低下 IIa 四肢・体幹優位 IIb 口腔・咽頭・呼吸筋優位 |
| III | 眼以外の筋力が中等度低下 IIIa 四肢・体幹優位 IIIb 口腔・咽頭・呼吸筋優位 |
| IV | 眼以外の筋力が高度低下 IVa 四肢・体幹優位 IVb 口腔・咽頭・呼吸筋優位 |
| V | 挿管管理 |
治療
- ●
- 胸腺腫を合併する重症筋無力症は拡大胸腺摘出術の絶対的適応である。
- ●
- 現在、重症筋無力症に対する胸腺摘出術は、美容的にも優れ、回復の早いロボット支援手術を含む低侵襲胸腔鏡手術で行われていることが多い。60歳以上の高齢患者ではすでに胸腺は萎縮しており胸腺摘出術の効果は少ないとされその手術適応は慎重に判断する必要がある。また、抗MuSK抗体陽性例では胸腺摘出術の効果はなく手術適応とはならない。
- ●
- 眼筋型ではコリンエステラーゼ阻害薬の投与で日常生活に支障がなければ経過観察されることが多いが、比較的早期にステロイド治療が導入されることもある。抗アセチルコリン受容体抗体高値の症例では胸腺摘出術の適応とされることもある。
- ●
- 全身型では、その重症度に応じて胸腺摘出術と抗コリンエステラーゼ阻害薬、プレドニゾロン、カルシニューリン阻害薬、ガンマグロブリン製剤、遺伝子組換え抗補体薬やFc受容体抗体薬などを組み合わせて治療がなされる。重症筋無力症診療ガイドライン2022では発症時に早期速効性治療戦略を積極的に行うことが推奨されている。胸腺摘出術による改善率は80%と高く、特に若年発症の全身型重症筋無力症では、プレドニゾロンを用いた薬物療法とともに自己抗体を産生している胸腺を摘除することで、慢性期のプレドニゾロン内服量は半分に減らすことができ、88%の患者で日常生活を制限なくおくれるようになったことが国際共同臨床試験で示されている。ただし、嚥下困難や咀嚼障害、構音障害などの球症状が強い全身型では、胸腺摘出術後の人工呼吸器離脱が困難となるクリーゼをきたすことがあり、あらかじめ薬物療法や血漿交換などで筋無力症状を安定化させた後に手術を行うことが望ましい。
- ●
- 呼吸不全を呈するいわゆるクリーゼに対しては、血漿交換、免疫グロブリン大量療法が有効である。メチルプレドニゾロン・パルス治療も有効であるが、投与後の一過性増悪に注意を要する。これら非経口速効性治療(血漿交換、免疫グロブリン大量療法、メチルプレドニゾロン・パルス治療)がクリーゼ治療の中心となる。クリーゼを脱した後はプレドニゾロン、カルシニューリン阻害薬、遺伝子組換え抗補体薬、Fc受容体抗体薬による症状のコントロールを目指す。

