医師主導治験
NF2に対するベバシズマブの有効性及び安全性を検討する医師主導治験
この度、皆様のご協力のもと、神経線維腫症2型(NF2)に対するベバシズマブの有効性及び安全性を検討する多施設共同医師主導治験を2019年10月から開始することになりました。
ベバシブマブはVEGF(血管内皮増殖因子)に対する抗体で、癌や悪性神経膠腫(悪性の脳腫瘍)に対する分子標的薬として用いられています。このベバシズマブがNF2患者さんのうち約半数に有効で、腫瘍が縮小したり聴力が改善すると報告され、患者様からベバシズマブ治療を望む声が多く寄せられていました。この医師主導治験は、ベバシズマブの安全性を確認し有効性を正しく評価して、NF2の皆様が保険診療として用いることができるようにすることを目指して行います。
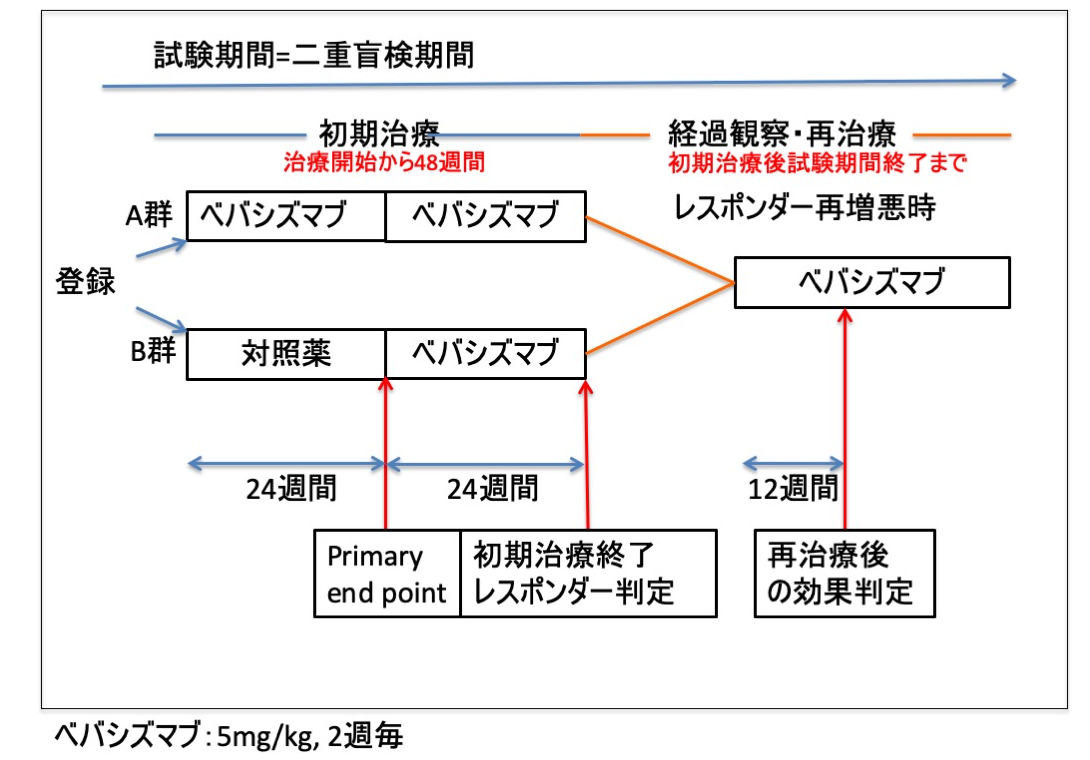
この治験では60人のNF2患者様を対象として、二重盲検無作為化プラセボ対照試験を行います。この試験では、ベバシズマブ(=実薬:本当の薬)を用いる人と、プラセボ薬(=偽薬:生理的食塩液)を用いる人を、くじ引きのように無作為に選んで、しかも、投与している医者も投与されている患者も、どちらの薬が投与されているのかわからないようにして治療をすすめることで、実薬が本当に偽薬よりも良い結果が得られるのかを証明します。この治験では、ベバシズマブ 5mg/kgを2週間間隔で繰り返し投与いたしますが、この投与法は、すでに海外から有効性と安全性を示す報告が複数あります。また、この治療に期待する声が多いことから、倫理的側面への配慮として、当初の24週間(約6ヶ月)は上記のようにプラセボ薬を用いますが、以後の24週間についてはすべての人に実薬のベバシズマブ投与を行います(下図参照)。なお二つの期間を合わせた48週間の治療を「初期治療」と呼んでいます。
効果については、聴力の改善で評価を行います。したがって、聴力が全く正常の方や、両側聴力が消失した方は参加できません。初期治療終了時点で聴力の改善がみられた方については、その後の経過観察の期間中に、聴力が再び悪くなるようなことがあれば、ベバシズマブの治療を再開します(この場合も全員実薬を用います)。
現在(2020年6月17日)、治験は順調な滑り出しており、北海道大学、福島県立医科大学、日本医科大学、藤田医科大学、大阪市立大学、広島大学、香川大学、熊本大学の8大学で実施中です。治験についてのお問い合わせなど、お気軽に下記まで連絡をいれていただければと存じます。なお東京大学でも、なるべく早く実施が可能となるよう準備をすすめて頂いております。
ご質問がございましたら、下記のメールアドレスにお気軽にご連絡ください。また、受診の詳細は各施設にご確認ください。
メールアドレス:beatnf2#fmu.ac.jp(#の部分には@が入ります)
皆様のご協力とご支援を賜りますよう、是非とも宜しくお願い致します。



