H-4.
視神経膠腫
Optic Glioma
1.概要
1.視神経膠腫とは?
視神経膠腫(optic glioma)とは、視覚系を担当する細胞やその周囲から発生する脳腫瘍のひとつで、視路神経膠腫(optic pathway glioma : OPG)とも呼ばれています。ここでは,OPGと呼ぶことにします。
視覚系とは、目から入った情報を脳に送る一連の情報システムのことで、このシステムのおかげで私達は“見る”ことができます。
このシステムには、視神経、視交叉、視索、視放線が含まれています。
視覚系のどこかにOPGが発生すると、腫瘍が情報の流れを阻害して、視力低下や視野障害などの眼の症状が発生します。
その程度は、OPGの発生部位や腫瘍増大速度などによって決まります。
OPGは、約5%が失明すると報告されていますが、治癒率が高い腫瘍であることも事実です。
2.OPGの発生率は?
OPGは、小児脳腫瘍の3〜5%を占める腫瘍です。
OPGの70%程度は10歳までに発症し、多くの症例では5歳以下で診断されます。過去の報告によると、症状が出現した時の平均年齢は8.8歳で、
男女間に発生率の差はありませんでした。神経線維腫症1型(NF1)はこの腫瘍が発生するリスクが高く、 NF1の子ども達の20%程度がOPGを罹患するといわれています。
◆ 医療者向け ◆
視神経に発生する原発性腫瘍は少なく、以下の腫瘍が発生することがあります。
- 視神経膠腫
- 視神経鞘髄膜腫
- 神経節膠腫
- 原発性リンパ腫
3.神経節膠腫と 4.原発性リンパ腫は非常にまれです。視神経膠腫と視神経鞘髄膜腫は、
眼腫瘍の4%程度を占めると報告されています。
視神経膠腫は、毛様細胞性星細胞腫が主体の低悪性度神経膠腫に分類されます。
【病 因】
視神経膠腫は、大脳皮質までの視路に発生する低悪性度神経膠腫で、正確には視路神経膠腫(optic pathway glioma: OPG)と呼ばれます。本解説ではOPGと呼ぶことにします。
視路は、視神経、視交叉、視索、視放線、更に視床下部が含まれます。
OPGは、散発性にあるいは神経線維腫症(neurofibromatosis type 1: NF1)に関連して発生します(参考文献:1)。
散発性に発生する場合、MAPK伝達経路に関わる遺伝子異常を認めることが特徴です。
代表的なものは、BRAF遺伝子(7q)異常で、異常形態としてBRAF-KIAA1549融合遺伝子発現が70%に認められます(参考文献:2)。
その他は、BRAF V600E遺伝子変異、その他のBRAF融合遺伝子発現、FGFR1遺伝子変異、NF1遺伝子変異などです。これまでの報告によると、
MAPK伝達回路に関わる遺伝子異常が相互排他的に発現していることが特徴で、single pathway diseaseと呼ばれています(参考文献:3)。
NF1に発生するOPGの場合、17番長腕染色体上にあるneurofibrominが不活性化され、RAS経路活性が上昇、
その結果RAS誘発腫瘍が生じることになります(参考文献:4)。
【疫 学】
一般的にOPGの発生は10歳以下の小児に多く、小児脳腫瘍の3~5%を占めます(参考文献:4)。
71%は10歳までに、20歳までに90%が発生し、平均発症時年齢は8.8歳とされています。我が国の全国脳腫瘍統計では、全脳腫瘍の0.01〜0.02%を占めます。
およそ15〜20%のNF1でOPGが発生するといわれていますが、症候性となるのは30〜50%と見積もられています(参考文献:1,5)。
OPGの発生頻度は男女で変わりありませんが、視神経に発生するOPGでは女児に多いとされています。
視神経のみに限局するOPGは全体の25%、残りの75%は視交叉を含むことになります。
【参考文献】
- Robert-Boire V, Rosca L, Samson Y, Ospina LH, Perreault S. Clinical Presentation and Outcome of Patients With Optic Pathway Glioma. Pediatr Neurol. 2017 Oct;75:55-60.
- Chen YH, Gutmann DH. The molecular and cell biology of pediatric low-grade gliomas. Oncogene. 2014 Apr 17;33(16):2019-26.
- David T W Jones, Barbara Hutter, Natalie Jager, et al., Recurrent somatic alterations of FGFR1 and NTRK2 in pilocytic astrocytoma. Nat Genet. 2013 Aug;45(8):927-32.
- Fried I, Tabori U, Tihan T, Reginald A, Bouffet E. Optic pathway gliomas: a review. CNS Oncol. 2013 Mar;2(2):143-59.
- Campen CJ, Gutmann DH. Optic Pathway Gliomas in Neurofibromatosis Type 1. J Child Neurol. 2018 Jan;33(1):73-81.
2.症状
一般的に、脳腫瘍では年齢や腫瘍の発生部位によって様々な症状が出現します。OPGも同様です。
OPGの症状の特徴として次の3つが重要です。
- 眼の問題:斜視、視力低下、視野障害などが出現します。
- 眼球突出:眼窩内に発生した場合、眼球が前方へ押し出されることがあります。
- ホルモンの問題:発達の異常、体重増加や減少、尿崩症や思春期早発などの内分泌障害が出現することがあります。
そのため,次の症状が手がかりになることがあります。
- 成長がゆっくり
- 頭を傾けたり揺すったりする行動
- 眼球突出
- ホルモン産生障害
- 食欲低下
- 睡眠障害
- 不安定な歩行、バランスが取れない
◆ 医療者向け ◆
視力低下や視野障害、眼球突出、頭痛などの症状で発症します。
乳幼児では、視力低下を訴えることが困難なので、視力検査で初めて指摘されることがあります。
非NF1症例では90%、NF1症例では72%で視力低下を示すと報告されています(参考文献:1)。
眼球突出は、NF1で多く20〜30%、非NF1では5〜12%とされています(参考文献:1)。
脳脊髄液流路閉塞による水頭症症状は約25%で認められます。その他、視床下部〜間脳下垂体症状としてホルモン異常や思春期早発、
間脳症候群を認めることがあり、注意が必要です。
【参考文献】
- Iris Fried, Uri Tabori, Tarik Tihan, Arun Reginald, Eric Bouffet Optic pathway gliomas: a review CNS Oncol. 2013 Mar;2(2):143-59.
3.検査・診断
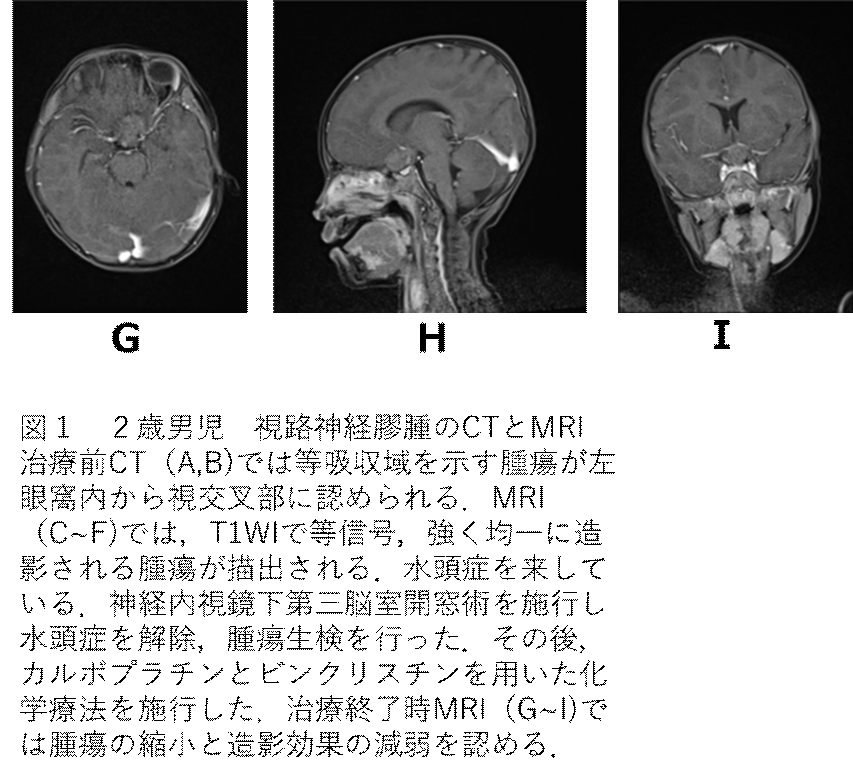
OPGを治療する際、最初に行わなければならないことは正確な診断です。通常、OPGはMRIやCTなどの画像検査(図1,2)
や眼科の検査などを組み合わせて診断されます。
画像検査では、腫瘍の部位や進展具合を見極めます。造影剤を用いて脳と眼窩を含むMRIを施行すると、
約80%の症例で腫瘍がみつかると報告されています。造影剤の投与によって全体的に均一に造影される腫瘍が見つかったり、
不均一に造影される腫瘍が見つかったりと様々です。多くの場合は、画像検査の結果から診断することができます。


◆ 医療者向け ◆
MRIを中心とした画像検査が中心となります(上図1,2)。
Robert-Boireらは、MRIで腫瘍を指摘できるのは約80%と報告しています。
MRIでは、T1WIで等〜低信号、T2WIで高信号に描出され、50%以上で造影効果が認められるといわれています。
視路に沿った部位に腫瘍が認められ、腫瘍サイズは様々なことが多いようです。
NF1では、両側視神経にdouble-intensity tubular thickening(pseudo cerebrospinal fluid intensity signal)や視神経中央部が下方に
kinkingすることが特徴とされています。
CTでは、等吸収〜高吸収を示し、通常石灰化の頻度は低いと考えられています。石灰化がある場合,頭蓋咽頭腫や奇形腫が鑑別に上がります。
【参考文献】
- Robert-Boire V, Rosca L, Samson Y, Ospina LH, Perreault S. Clinical Presentation and Outcome of Patients With Optic Pathway Glioma. Pediatr Neurol. 2017 Oct;75:55-60
4.治療
OPGの増殖は非常にゆっくりですが、視神経、視交叉、正常脳組織などの周囲の構造物に確実に影響を及ぼします。 多くの症例では、視力は変わりなく安定とされていますが、40%の子ども達では腫瘍は大きくなり続けると報告されています。 そのため、OPGの治療方法の選択は、次の項目を考慮して総合的に判断する必要があります。
- 年齢、既往歴、生活歴
- 視力低下や視野障害の程度
- 腫瘍の予想される病理診断、発生部位、サイズ
- 腫瘍がどういうふうに進展しているか
- 患児が、処置、薬剤、治療などに耐えられるのか
- NF1の状況
現在、経過観察、化学療法、放射線治療、手術がOPGの主な治療法として用いられています。 どの治療法を選ぶのか、どれとどれを組み合わせて治療を行うのかは、様々な要因によって決まります。
1)経過観察
80%の子ども達は、はじめ視力低下が進みますが、その後視力低下は止まるといわれています。
しかし、それは必ずしも腫瘍の増大、進行が止まったことを意味しないことも重要です。経過観察でも、良好な長期的予後を示すことが報告されています。
2)化学療法
現在、多くの症例では化学療法(抗がん剤投与)が第一選択として用いられます。
化学療法は、腫瘍細胞の増殖や複製を阻害し、腫瘍が大きくならないようにしたり、視力の回復を期待したりする目的で用いられます。
ただし、化学療法の効果が出るまでには数ヶ月を要することがあります。
化学療法の適応は、画像上の腫瘍増大あるいは眼の症状や神経学的所見が進行する症例です。
10歳以上では、化学療法が第一選択としている報告もあります。
化学療法が視力改善に効果があるのかは依然として不明ですが、改善14%、悪化9%、不変77%というデータを発表している報告があります。
ホルモンに問題があると分かった場合、ホルモン補充を受けることがあります。
3)手術
現在、OPGに対しては腫瘍摘出術が第一選択になることはありません。しかし、腫瘍が大きい場合などには、
症状や視力の改善を目的として腫瘍の減量を外科的に行うことがあります。
一般的にOPGに対する手術の役割は次の3つといわれています。
- 腫瘍生検
- 腫瘍減量
- 救済的摘出

4)放射線治療
化学療法や手術で腫瘍が制御できない場合、放射線治療を行うことがあります。放射線治療は、
腫瘍細胞にダメージを加えて腫瘍を小さくしたりします。
OPGの場合、腫瘍の近辺には視神経、間脳下垂体、視床下部や血管などの重要な構造物が含まれるので、
放射線治療の副作用や晩期合併症を常に考えて置かなければなりません。血管病(もやもや病)はOPG放射線治療最大の合併症と考えられています。
◆ 医療者向け ◆
自然歴:
OPGは本来非常にゆっくり増大します。しかし、周囲の正常脳,構造物に浸潤する能力も持ち合わせています。
マネジメント:
経過観察を含めた治療を行うかどうかは、脳神経外科医や小児血液腫瘍科医などのスタッフが参集したtumor boardで決定されますが、
それは症状、視機能の状態、腫瘍の進行状況、患児の年齢などを参考に総合的に決定されます。
一般的には症状の進行や画像上の腫瘍増大がなければ、経過観察が第一選択となると報告されています(参考文献:1,2)。
1)経過観察
80%の症例では、視力低下が起こる初期段階をすぎると視力低下は止まると報告されています。
しかし、視力の安定化は必ずしも腫瘍の増大休止を意味しているわけではありません。
積極的な治療を行わず観察のみで経過を見た場合でも、良好な長期的生命予後が確保されるとされています(参考文献:1,2,3,4)。
2)手術
最近まで腫瘍摘出術は治療の選択肢の一つでした。しかし、近年では、外科介入の目的は腫瘍生検、腫瘍減量、
救済的手術に限定されるとの報告が多くなっています(参考文献:1,2)(上表1)。
現時点では、水頭症の解除、治療に抵抗する腫瘍増大がある時、3歳以下の進行例に対する救済目的などに手術が用いられています。
3)放射線治療
OPGに対する放射線治療は、現在でも議論の余地があるところです。再発症例に対し放射線治療を行う報告もありますが、
副作用や晩期合併症が懸念され、施行頻度は減少しています。
4)化学療法
概して、OPGは化学療法に反応し、化学療法によって腫瘍増殖や視機能悪化は軽減されるといわれます。
多くの症例で、化学療法で一過性あるいは永久的に腫瘍コントロールが可能ですが、完全消失は例外的であり、
治療数年後であってもMRIで残存腫瘍を認めることが多いといわれています。
多くの症例ではvincristineとcarboplatinを使用した化学療法が第一選択となります。5年PFS 約40%、
二次がん発生や治療関連有害事象などのリスク増大は見られないとされています。
その他のレジメンとして、
thioguanine + procarbazine + lomustine + vincristine (TPCV)、etoposide+cisplatin, temozolomideなどが使用されています。
OPGに対する化学療法の比較試験の報告は少なく、vincristine+carboplatin vs TPCVのランダム化比較試験が報告されているのみです。
その報告では、反応性は同等、5年PFSはTPCVで52±5%と、39±4%のvincristine+carboplatinより高かったものの有意差は認められませんでした(参考文献:5)。
VEGF阻害薬であるBevacizumabがOPGに対し有効との報告(参考文献:6)があり、今後の臨床研究が期待されます。
MAPK経路が活性化されていることに注目した分子標的薬の有効性が報告され始めています。
MEK阻害薬、selumetinibを用いた臨床試験で、再発OPGに対し2年PFS 69% を達成したことが報告されています(参考文献:7)。
化学療法が視力改善に効果があるのかは依然として不明です。Dodgeshun らは 改善 14%、悪化 9%、不変 77%と報告しています(参考文献:8)。
【参考文献】
- Iris Fried, Uri Tabori, Tarik Tihan, Arun Reginald, Eric Bouffet Optic pathway gliomas: a review CNS Oncol. 2013 Mar;2(2):143-59.
- Marshall Huang; Jay Patel; Bhupendra C. Patel. Optic Nerve Glioma. StatPearls [Internet].
- Sharon L Tow, Sidhartha Chandela, Neil R Miller, Anthony M Avellino Long-term outcome in children with gliomas of the anterior visual pathway Pediatr Neurol. 2003 Apr;28(4):262-70.
- Y Mikaeloff, Y Chaix, J Grill, C Adamsbaum, J Bursztyn, H Rubie, A Sevely, I Jambaque, C Kalifa, G Ponsot, J C Carriere, D Rodriguez [Optic pathway gliomas in neurofibromatosis type I. Longitudinal study of 30 cases in two multidisciplinary practices] Arch Pediatr. 2002 Aug;9(8):797-804.
- Joann L Ater, Tianni Zhou, Emiko Holmes, Claire M Mazewski, Timothy N Booth, David R Freyer, Ken H Lazarus, Roger J Packer, Michael Prados, Richard Sposto, Gilbert Vezina, Jeffrey H Wisoff, Ian F Pollack Randomized study of two chemotherapy regimens for treatment of low-grade glioma in young children: a report from the Children's Oncology Group J Clin Oncol. 2012 Jul 20;30(21):2641-7.
- Eugene I Hwang, Regina I Jakacki, Michael J Fisher, Lindsay B Kilburn, Marianna Horn, Gilbert Vezina, Brian R Rood, Roger J Packer Long-term efficacy and toxicity of bevacizumab-based therapy in children with recurrent low-grade gliomas Pediatr Blood Cancer. 2013 May;60(5):776-82.
- Anuradha Banerjee, Regina I Jakacki, Arzu Onar-Thomas, Shengjie Wu, Theodore Nicolaides, Tina Young Poussaint, Jason Fangusaro, Joanna Phillips, Arie Perry, David Turner, Michael Prados, Roger J Packer, Ibrahim Qaddoumi, Sridharan Gururangan, Ian F Pollack, Stewart Goldman, Lawrence A Doyle, Clinton F Stewart, James M Boyett, Larry E Kun, Maryam Fouladi. A phase I trial of the MEK inhibitor selumetinib (AZD6244) in pediatric patients with recurrent or refractory low-grade glioma: a Pediatric Brain Tumor Consortium (PBTC) study Neuro Oncol. 2017 Aug 1;19(8):1135-1144.
- Andrew J Dodgshun, James E Elder, Jordan R Hansford, Michael J Sullivan. Long-term visual outcome after chemotherapy for optic pathway glioma in children: Site and age are strongly predictive Cancer. 2015 Dec 1;121(23):4190-6.
5.予後
OPGの生存率は90%程度と報告されています。年長児やNF1症例では,より良好な生存率です。
失明する可能性は5%以下とされています。どれくらい視力が残るかは治療前の視力に比例すること、
診断時年齢が低い子ども達のほうが視力を温存する可能性が高いことも分かっています。
初期治療から長時間経過したあとでも腫瘍の再発は起こります。通常,腫瘍はもとの場所に再発しますが、
他の脳の部分や脊髄に再発することもあります。局所放射線治療や化学療法が治療法の選択肢となります。
長期的に必要なケアは?
OPGは再発したり、播種したりします。また、長期的には様々な問題に直面します。
これらのことから、定期的にMRIを撮影したり、眼科の検査や内分泌の検査を行ったりする必要があります。
◆ 医療者向け ◆
Khafaga らが報告した5年OS 87%、10年OS 75%(参考文献:1)という成績は、
より近年の報告では5年OS 95%、10年OS 91%と改善しています(参考文献:2,3)。
あらゆる部位のOPGの治療成績をまとめた総説では、腫瘍再発あるいは腫瘍増大は全体の38%に認められたとしています(参考文献:4)。
長期的にみると非NF1のほうがNF1と比べて視力低下となる可能性は高いといわれています。Wanらは、発症時若年、視神経蒼白、
腫瘍サイズ、眼窩錐内発生、視床下部発生が視力低下の危険因子と報告し、これらの危険因子がなければ、
最大90%の症例で治療後視力は安定化するとしています(参考文献:5)。
【参考文献】
- Yasser Khafaga, Maher Hassounah, Alaa Kandil, Imaduddin Kanaan, Ayman Allam, Gamal El Husseiny, Amani Kofide, Abdulaziz Belal, Mohammed Al Shabanah, Henrik Schultz, Derek Jenkin Optic gliomas: a retrospective analysis of 50 cases Int J Radiat Oncol Biol Phys. 2003 Jul 1;56(3):807-12.
- Fausto J Rodriguez, Kah Suan Lim, Daniel Bowers, Charles G Eberhart Pathological and molecular advances in pediatric low-grade astrocytoma Annu Rev Pathol. 2013 Jan 24;8:361-79.
- Josue Rakotonjanahary, Emilie De Carli, Matthieu Delion, Chantal Kalifa, Jacques Grill, Francois Doz, Pierre Leblond, Anne-Isabelle Bertozzi, Xavier Rialland, Brain Tumor Committee of SFCE Mortality in Children with Optic Pathway Glioma Treated with Up-Front BB-SFOP Chemotherapy PLoS One. 2015 Jun 22;10(6)
- J J Dutton. Gliomas of the anterior visual pathway Surv Ophthalmol. Mar-Apr 1994;38(5):427-52.
- Michael J Wan, Nicole J Ullrich, Peter E Manley, Mark W Kieran, Liliana C Goumnerova, Gena Heidary. Long-term visual outcomes of optic pathway gliomas in pediatric patients without neurofibromatosis type 1 J Neurooncol. 2016 Aug;129(1):173-8.
※ 引用文献や執筆時期が異なるため、脳腫瘍診療ガイドラインとは若干の齟齬があります。





